金屬的性質(zhì)和應(yīng)用是化學(xué)研究的重要課題。
【知識(shí)回顧】
(1)鐵絲在潮濕的空氣中會(huì)慢慢銹蝕,是鐵與 O2、H2OO2、H2O(填化學(xué)式)等物質(zhì)作用的過程。
【實(shí)驗(yàn)探究】(以下實(shí)驗(yàn)均在室溫和1標(biāo)準(zhǔn)大氣壓的環(huán)境中進(jìn)行)
(2)制作暖寶寶要用到鐵粉、活性炭、氯化鈉等物質(zhì)。
【實(shí)驗(yàn)1】如圖1所示,稱取2.0g鐵粉和2.5g活性炭,攪拌均勻,用濾紙包好,再滴入約1mL溶質(zhì)質(zhì)量分?jǐn)?shù)為5%的氯化鈉溶液,迅速用溫度傳感器測(cè)量,實(shí)驗(yàn)進(jìn)行到450s時(shí)搓揉一次濾紙包使表面結(jié)塊的混合物松散,實(shí)驗(yàn)過程中別得混合物溫度隨時(shí)間變化的曲線如圖2所示。
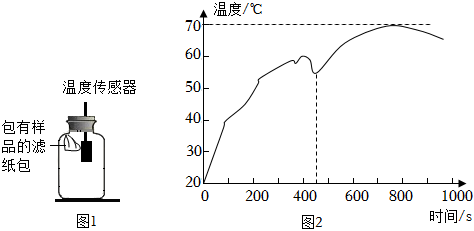
圖中450s后混合物溫度繼續(xù)升高的原因是 增加氣體與樣品的充分接觸,鐵生銹速率加快,放出熱量增加增加氣體與樣品的充分接觸,鐵生銹速率加快,放出熱量增加。
(3)無煙食品加熱劑(內(nèi)裝有鎂粉、鐵粉和氯化鈉等化學(xué)品)常用于野外加熱食物,使用時(shí)向化學(xué)品中加入一定量的水,能迅速反應(yīng)升溫使水沸騰,對(duì)食物進(jìn)行加熱。
【實(shí)驗(yàn)2】向加有100mL水的隔熱容器中分別加入下表各組物質(zhì),連續(xù)攪拌,每50s記錄一次溫度,測(cè)得溫度變化曲線如圖所示。
| 實(shí)驗(yàn) | 物質(zhì) | ||
| 鎂 | 鐵 | 氯化鈉 | |
| Ⅰ | 2.4g,條狀 | 2.8g粉末狀 | 5.85g粉末狀 |
| Ⅱ | 2.4g,顆粒狀 | ||
| Ⅲ | 2.4g,粉末狀 | ||
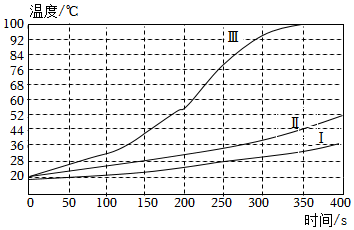
①分析上述實(shí)驗(yàn)可以發(fā)現(xiàn)影響鎂和水反應(yīng)速率的因素是
鎂條形狀
鎂條形狀
。②無煙食品加熱劑的成分不能用于制作暖寶寶的理由是
反應(yīng)后溫度過高,會(huì)燒傷皮膚
反應(yīng)后溫度過高,會(huì)燒傷皮膚
。③從上述實(shí)驗(yàn)可知,“無煙食品加熱劑”需密封保存的原因是與空氣中的
水
水
有關(guān)。④在實(shí)驗(yàn)2基礎(chǔ)上,若要證明溫度升高的主要原因是鎂參與了反應(yīng),設(shè)計(jì)實(shí)驗(yàn)方案是
向加有100mL水的隔熱容器中加入5.2g粉末狀鐵與5.85g粉末狀的氯化鈉,連續(xù)攪拌,每50s記錄一次溫度,測(cè)得溫度變化曲線
向加有100mL水的隔熱容器中加入5.2g粉末狀鐵與5.85g粉末狀的氯化鈉,連續(xù)攪拌,每50s記錄一次溫度,測(cè)得溫度變化曲線
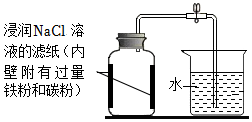
。(4)化學(xué)興趣小組按如圖所示裝置進(jìn)行實(shí)驗(yàn),瓶中的氧氣可以幾乎耗盡,測(cè)得實(shí)驗(yàn)數(shù)據(jù)如下表所示。
| 測(cè)量項(xiàng)目 | 實(shí)驗(yàn)前 | 實(shí)驗(yàn)后 | |
| 集氣瓶(扣除內(nèi)容物)和導(dǎo)管的容積 | 燒杯中水的體積 | 燒杯中水的體積 | |
| 體積/mL | 131.0 | 90.0 | 63.6 |
20.2%
20.2%
(計(jì)算結(jié)果精確到0.1%)。②銅能與空氣中氧氣、水和二氧化碳反應(yīng)而銹蝕,生成銅綠【主要成分為Cu2(OH)2CO3】,若將如圖裝置中的鐵粉換成足量的銅粉進(jìn)行實(shí)驗(yàn),
不能
不能
(選填“能”或“不能”)比較準(zhǔn)確的測(cè)定空氣中氧氣的含量,理由是 空氣中氧氣體積分?jǐn)?shù)是21%,二氧化碳含量只有0.03%,銅不能將裝置中的氧氣幾乎耗盡
空氣中氧氣體積分?jǐn)?shù)是21%,二氧化碳含量只有0.03%,銅不能將裝置中的氧氣幾乎耗盡
。(提示:銅與空氣中氧氣、水、二氧化碳反應(yīng)銹蝕時(shí),當(dāng)參加反應(yīng)的氧氣和二氧化碳的體積相等時(shí),反應(yīng)才能恰好完成。)【考點(diǎn)】探究金屬銹蝕的條件.
【答案】O2、H2O;增加氣體與樣品的充分接觸,鐵生銹速率加快,放出熱量增加;鎂條形狀;反應(yīng)后溫度過高,會(huì)燒傷皮膚;水;向加有100mL水的隔熱容器中加入5.2g粉末狀鐵與5.85g粉末狀的氯化鈉,連續(xù)攪拌,每50s記錄一次溫度,測(cè)得溫度變化曲線;20.2%;不能;空氣中氧氣體積分?jǐn)?shù)是21%,二氧化碳含量只有0.03%,銅不能將裝置中的氧氣幾乎耗盡
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:182引用:1難度:0.3
相似題
-
 1.在進(jìn)行“二氧化碳制取和性質(zhì)實(shí)驗(yàn)”時(shí),小明發(fā)現(xiàn)放置小蠟燭的銅架上出現(xiàn)了綠色物質(zhì),且綠色物質(zhì)只出現(xiàn)在下部(伸到燒杯下面的部分),上部和在燒杯外的部分沒有出現(xiàn),小明思考,銅也會(huì)生銹嗎?為什么只出現(xiàn)在下部呢?銅生銹的條件是什么?
1.在進(jìn)行“二氧化碳制取和性質(zhì)實(shí)驗(yàn)”時(shí),小明發(fā)現(xiàn)放置小蠟燭的銅架上出現(xiàn)了綠色物質(zhì),且綠色物質(zhì)只出現(xiàn)在下部(伸到燒杯下面的部分),上部和在燒杯外的部分沒有出現(xiàn),小明思考,銅也會(huì)生銹嗎?為什么只出現(xiàn)在下部呢?銅生銹的條件是什么?
【查閱資料】銅在一定條件下會(huì)銹蝕生成一種綠色的物質(zhì)(銅綠),其主要成分是堿式碳酸銅,化學(xué)式時(shí)候Cu2(OH)2CO3,受熱易分解.
【猜想與假設(shè)】依據(jù)銅綠的化學(xué)式,小明猜想銅生銹的條件可能是,銅與氧氣、共同作用,做出此猜想的依據(jù)是.
【設(shè)計(jì)實(shí)驗(yàn)】將四塊銅片分別按如圖放置半個(gè)月,觀察現(xiàn)象如下,A中銅片生銹且水面附近銹蝕最嚴(yán)重,B、C、D中銅片不生銹,D裝置中氫氧化鈉溶液的作用是,寫出該反應(yīng)的化學(xué)方程式.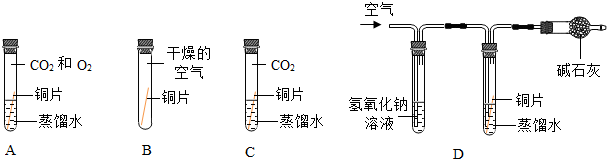
【得出結(jié)論】根據(jù)A和D中的實(shí)驗(yàn)現(xiàn)象可知銅生銹需要.
【反思與應(yīng)用】利用所得結(jié)論填空,依據(jù)本實(shí)驗(yàn)結(jié)合“二氧化碳澆滅蠟燭”的實(shí)驗(yàn)操作推測(cè)銅架下部容易生銹的原因是.
【實(shí)驗(yàn)拓展】有資料顯示,氧化銅也能加快過氧化氫溶液的分解速率.
(1)給你一支已經(jīng)產(chǎn)生銅綠的銅架,5%過氧化氫溶液,請(qǐng)你設(shè)計(jì)實(shí)驗(yàn)證明(儀器自選).
(2)請(qǐng)你試著寫出銅生成銅綠的化學(xué)方程式.發(fā)布:2024/11/10 8:0:1組卷:54引用:1難度:0.3 -
2.化學(xué)小組對(duì)鋼鐵的銹蝕進(jìn)行實(shí)驗(yàn)研究。
Ⅰ.探究鋼鐵銹蝕的基本條件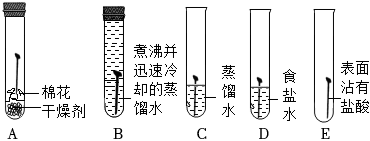
(1)一段時(shí)間后,C、D、E中鐵釘生銹,A、B中鐵釘無明顯銹蝕。由A、B、C的現(xiàn)象可知,鐵的銹蝕是鐵跟等物質(zhì)作用的過程。
(2)使用自來水重新進(jìn)行如圖實(shí)驗(yàn),一段時(shí)間后發(fā)現(xiàn)試管B中鐵釘生銹了,其可能的原因是。
Ⅱ.探究食鹽水濃度對(duì)鋼鐵腐蝕速率的影響
用如圖裝置進(jìn)行實(shí)驗(yàn),每組實(shí)驗(yàn)加入鐵炭總質(zhì)量為24g,食鹽水體積為7.5mL,恰好能將固體潤濕。測(cè)得的數(shù)據(jù)見下表:(提供資料:示數(shù)差3cm是指U型管左側(cè)液面上升3cm。)
(3)分析食鹽水濃度對(duì)鋼鐵腐蝕速率的影響應(yīng)對(duì)比實(shí)驗(yàn)序號(hào) 鐵炭質(zhì)量比 食鹽水濃度/% 示數(shù)差3cm所用時(shí)間/s 10分鐘時(shí)溫度升高值/℃ 實(shí)驗(yàn)① 2:1 26 90 7.8 實(shí)驗(yàn)② 4:1 26 170 4.2 實(shí)驗(yàn)③ 6:1 26 190 3.3 實(shí)驗(yàn)④ 2:1 13 140 6 實(shí)驗(yàn)⑤ 2:1 6.5 140 6 (填實(shí)驗(yàn)序號(hào))。有同學(xué)提出應(yīng)該再加一組實(shí)驗(yàn),研究鐵炭質(zhì)量比為2:1、食鹽水濃度為3.3%時(shí)的實(shí)驗(yàn)數(shù)據(jù),你覺得是否有必要,并說明理由。
(4)查閱資料得知,食鹽水中的氯離子能破壞鋼筋表面的鈍化膜,并促使鐵發(fā)生一系列反應(yīng)得到氫氧化鐵,它在空氣中風(fēng)化失水后變成氧化鐵。鋼筋銹蝕過程中生成氧化鐵的反應(yīng)方程式是。
Ⅲ.探究水樣的pH及溶解氧濃度對(duì)鋼鐵腐蝕速率的影響
步驟1:按如圖連接好裝置,檢查裝置氣密性。
步驟2:向三頸燒瓶中放入3.5g生鐵粉末,向分液漏斗內(nèi)加入10mL不同濃度的稀鹽酸。
步驟3:將稀鹽酸全部注入三頸燒瓶內(nèi),關(guān)閉分液漏斗活塞,一段時(shí)間后,至恢復(fù)到室溫時(shí),采集的數(shù)據(jù)見下表: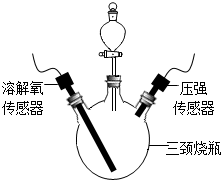
(5)步驟1中檢查裝置氣密性的方法為:先在分液漏斗中加水,再打開活塞,觀察到序號(hào) 鹽酸pH P反應(yīng)前 P反應(yīng)后 DO反應(yīng)前 DO反應(yīng)后 開始降低所需時(shí)間/s 實(shí)驗(yàn)① 2.0 90.8 91.8 5.2 4.3 131 實(shí)驗(yàn)② 3.0 90.8 91.5 5.0 3.7 68 實(shí)驗(yàn)③ 4.0 90.8 90.3 4.9 3.4 24 實(shí)驗(yàn)④ 5.0 90.8 90.5 4.9 3.7 98 實(shí)驗(yàn)⑤ 6.0 90.8 90.6 4.4 3.7 175 (填現(xiàn)象),表明裝置的氣密性良好。
(6)實(shí)驗(yàn)①和實(shí)驗(yàn)②反應(yīng)后壓強(qiáng)變大。進(jìn)行實(shí)驗(yàn)③時(shí),觀察到溶液中有氣泡冒出,反應(yīng)后體系內(nèi)壓強(qiáng)卻變小了,變小的原因是。
(7)分析表中數(shù)據(jù),在該實(shí)驗(yàn)條件下,下列說法正確的有(填字母)。
a.當(dāng)pH=2時(shí),鐵粉與氧氣的銹蝕速率最快
b.稀鹽酸中的溶解氧含量與鹽酸的pH有關(guān)
c.鐵粉和鹽酸,氧氣在剛接觸時(shí)不是同時(shí)發(fā)生反應(yīng)發(fā)布:2024/12/24 10:30:2組卷:225引用:4難度:0.5 -
3.化學(xué)小組對(duì)鋼鐵的銹蝕進(jìn)行實(shí)驗(yàn)研究。
Ⅰ.探究鋼鐵銹蝕的基本條件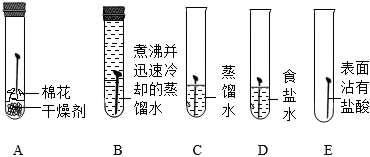
(1)一段時(shí)間后,C、D、E中鐵釘生銹,A、B中鐵釘無明顯銹蝕。由A、B、C的現(xiàn)象可知,鐵的銹蝕是鐵跟(填化學(xué)式)等物質(zhì)作用的過程。D中鐵釘比C中鐵釘銹蝕程度嚴(yán)重,說明。
(2)使用自來水重新進(jìn)行如圖實(shí)驗(yàn),一段時(shí)間后發(fā)現(xiàn)試管B中鐵釘生銹了,其可能的原因是。
Ⅱ.探究食鹽水對(duì)鋼鐵腐蝕速率的影響
用如圖裝置進(jìn)行實(shí)驗(yàn),錐形瓶中放生鐵粉末,滴管中預(yù)先加入2mL不同濃度的食鹽水,并用氧氣傳感器測(cè)定錐形瓶內(nèi)的氧氣濃度,數(shù)據(jù)如下表所示: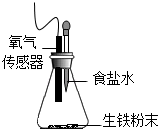
(3)該實(shí)驗(yàn)探究的是實(shí)驗(yàn)組 生鐵粉末質(zhì)量 食鹽水濃度 3min時(shí)瓶內(nèi)氧氣濃度 實(shí)驗(yàn)① 3.5g 4% 18.96% 實(shí)驗(yàn)② 3.5g 8% 18.56% 實(shí)驗(yàn)③ 3.5g 16% 18.28% 實(shí)驗(yàn)④ 3.5g 24% 17.99% 對(duì)鋼鐵腐蝕速率的影響,其實(shí)驗(yàn)結(jié)論是。
(4)查閱資料得知,食鹽水中的氯離子能破壞鋼筋表面的鈍化膜(其原理如圖所示),并促使鐵發(fā)生一系列反應(yīng)得到Fe(OH)3,F(xiàn)e(OH)3在空氣中風(fēng)化失水后變成氧化鐵。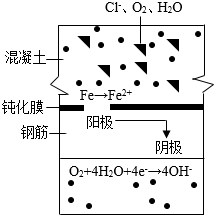
①氯離子破壞鋼筋表面的鈍化膜的過程中,從陽極向陰極轉(zhuǎn)移的微粒是。
②鋼筋銹蝕過程中得到氧化鐵的反應(yīng)方程式為。
Ⅲ.探究水樣的pH及溶解氧濃度對(duì)鋼鐵腐蝕速率的影響
步驟1:按如圖連接好裝置,檢查裝置氣密性。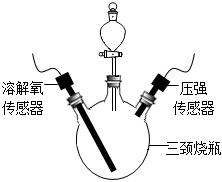
步驟2:向三頸燒瓶中放入3.5g生鐵粉末,向分液漏斗內(nèi)加入10mL不同濃度的稀鹽酸。
步驟3:將鹽酸全部注入三頸燒瓶內(nèi),關(guān)閉分液漏斗活塞,同時(shí)采集數(shù)據(jù)見下表:
(5)步驟1中檢查裝置氣密性的方法為序號(hào) 鹽酸pH 壓強(qiáng)p/kPa 溶解氧/mg?L-1 p反應(yīng)前 p反應(yīng)后 DO反應(yīng)前 DO反應(yīng)后 開始降低所需時(shí)間/s 實(shí)驗(yàn)① 2.0 90.8 91.8 5.2 4.3 131 實(shí)驗(yàn)② 3.0 90.8 91.5 5.0 3.7 68 實(shí)驗(yàn)③ 4.0 90.8 90.3 4.9 3.4 24 實(shí)驗(yàn)④ 5.0 90.8 90.5 4.9 3.7 98 實(shí)驗(yàn)⑤ 6.0 90.8 90.6 4.4 3.7 175 。
(6)實(shí)驗(yàn)1和實(shí)驗(yàn)2反應(yīng)后壓強(qiáng)變大的主要原因是(用化學(xué)方程式表示)。
(7)進(jìn)行實(shí)驗(yàn)3時(shí),觀察到溶液中有氣泡冒出,反應(yīng)后體系內(nèi)壓強(qiáng)卻變小了。其原因是。
(8)分析表中數(shù)據(jù),在該實(shí)驗(yàn)條件下,下列說法正確的有。
A.當(dāng)pH=2時(shí),鐵粉與氧氣的銹蝕速率最快
B.稀鹽酸中的溶解氧含量與鹽酸的pH有關(guān)
C.鐵粉和鹽酸,氧氣的反應(yīng)可以同時(shí)發(fā)生發(fā)布:2024/12/25 12:0:1組卷:264引用:3難度:0.7


