當(dāng)前位置:
試題詳情
 在進(jìn)行“二氧化碳制取和性質(zhì)實驗”時,小明發(fā)現(xiàn)放置小蠟燭的銅架上出現(xiàn)了綠色物質(zhì),且綠色物質(zhì)只出現(xiàn)在下部(伸到燒杯下面的部分),上部和在燒杯外的部分沒有出現(xiàn),小明思考,銅也會生銹嗎?為什么只出現(xiàn)在下部呢?銅生銹的條件是什么?
在進(jìn)行“二氧化碳制取和性質(zhì)實驗”時,小明發(fā)現(xiàn)放置小蠟燭的銅架上出現(xiàn)了綠色物質(zhì),且綠色物質(zhì)只出現(xiàn)在下部(伸到燒杯下面的部分),上部和在燒杯外的部分沒有出現(xiàn),小明思考,銅也會生銹嗎?為什么只出現(xiàn)在下部呢?銅生銹的條件是什么?
【查閱資料】銅在一定條件下會銹蝕生成一種綠色的物質(zhì)(銅綠),其主要成分是堿式碳酸銅,化學(xué)式時候Cu2(OH)2CO3,受熱易分解.
【猜想與假設(shè)】依據(jù)銅綠的化學(xué)式,小明猜想銅生銹的條件可能是,銅與氧氣、水和二氧化碳水和二氧化碳共同作用,做出此猜想的依據(jù)是銅綠中含有碳元素、氫元素和氧元素銅綠中含有碳元素、氫元素和氧元素.
【設(shè)計實驗】將四塊銅片分別按如圖放置半個月,觀察現(xiàn)象如下,A中銅片生銹且水面附近銹蝕最嚴(yán)重,B、C、D中銅片不生銹,D裝置中氫氧化鈉溶液的作用是除去空氣中的二氧化碳除去空氣中的二氧化碳,寫出該反應(yīng)的化學(xué)方程式CO2+2NaOH═Na2CO3+H2OCO2+2NaOH═Na2CO3+H2O.
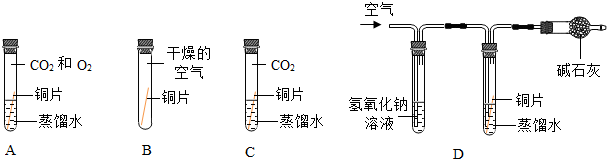
【得出結(jié)論】根據(jù)A和D中的實驗現(xiàn)象可知銅生銹需要二氧化碳二氧化碳.
【反思與應(yīng)用】利用所得結(jié)論填空,依據(jù)本實驗結(jié)合“二氧化碳澆滅蠟燭”的實驗操作推測銅架下部容易生銹的原因是操作過程中有少量水灑在銅片上,又向里面傾倒二氧化碳,小燒杯中本身就有氧氣,故滿足了銅生銹的條件操作過程中有少量水灑在銅片上,又向里面傾倒二氧化碳,小燒杯中本身就有氧氣,故滿足了銅生銹的條件.
【實驗拓展】有資料顯示,氧化銅也能加快過氧化氫溶液的分解速率.
(1)給你一支已經(jīng)產(chǎn)生銅綠的銅架,5%過氧化氫溶液,請你設(shè)計實驗證明(儀器自選).取2份等體積5%過氧化氫溶液,向其中一份加入經(jīng)過加熱變質(zhì)的銅綠,比較過氧化氫分解的速率取2份等體積5%過氧化氫溶液,向其中一份加入經(jīng)過加熱變質(zhì)的銅綠,比較過氧化氫分解的速率
(2)請你試著寫出銅生成銅綠的化學(xué)方程式2Cu+O2+CO2+H2O═Cu2(OH)2CO32Cu+O2+CO2+H2O═Cu2(OH)2CO3.
【答案】水和二氧化碳;銅綠中含有碳元素、氫元素和氧元素;除去空氣中的二氧化碳;CO2+2NaOH═Na2CO3+H2O;二氧化碳;操作過程中有少量水灑在銅片上,又向里面傾倒二氧化碳,小燒杯中本身就有氧氣,故滿足了銅生銹的條件;取2份等體積5%過氧化氫溶液,向其中一份加入經(jīng)過加熱變質(zhì)的銅綠,比較過氧化氫分解的速率;2Cu+O2+CO2+H2O═Cu2(OH)2CO3
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/11/10 8:0:1組卷:54引用:1難度:0.3
相似題
-
1.化學(xué)小組對鋼鐵的銹蝕進(jìn)行實驗研究。
Ⅰ.探究鋼鐵銹蝕的基本條件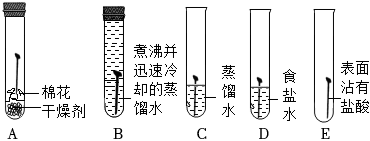
(1)一段時間后,C、D、E中鐵釘生銹,A、B中鐵釘無明顯銹蝕。由A、B、C的現(xiàn)象可知,鐵的銹蝕是鐵跟等物質(zhì)作用的過程。
(2)使用自來水重新進(jìn)行如圖實驗,一段時間后發(fā)現(xiàn)試管B中鐵釘生銹了,其可能的原因是。
Ⅱ.探究食鹽水濃度對鋼鐵腐蝕速率的影響
用如圖裝置進(jìn)行實驗,每組實驗加入鐵炭總質(zhì)量為24g,食鹽水體積為7.5mL,恰好能將固體潤濕。測得的數(shù)據(jù)見下表:(提供資料:示數(shù)差3cm是指U型管左側(cè)液面上升3cm。)
(3)分析食鹽水濃度對鋼鐵腐蝕速率的影響應(yīng)對比實驗序號 鐵炭質(zhì)量比 食鹽水濃度/% 示數(shù)差3cm所用時間/s 10分鐘時溫度升高值/℃ 實驗① 2:1 26 90 7.8 實驗② 4:1 26 170 4.2 實驗③ 6:1 26 190 3.3 實驗④ 2:1 13 140 6 實驗⑤ 2:1 6.5 140 6 (填實驗序號)。有同學(xué)提出應(yīng)該再加一組實驗,研究鐵炭質(zhì)量比為2:1、食鹽水濃度為3.3%時的實驗數(shù)據(jù),你覺得是否有必要,并說明理由。
(4)查閱資料得知,食鹽水中的氯離子能破壞鋼筋表面的鈍化膜,并促使鐵發(fā)生一系列反應(yīng)得到氫氧化鐵,它在空氣中風(fēng)化失水后變成氧化鐵。鋼筋銹蝕過程中生成氧化鐵的反應(yīng)方程式是。
Ⅲ.探究水樣的pH及溶解氧濃度對鋼鐵腐蝕速率的影響
步驟1:按如圖連接好裝置,檢查裝置氣密性。
步驟2:向三頸燒瓶中放入3.5g生鐵粉末,向分液漏斗內(nèi)加入10mL不同濃度的稀鹽酸。
步驟3:將稀鹽酸全部注入三頸燒瓶內(nèi),關(guān)閉分液漏斗活塞,一段時間后,至恢復(fù)到室溫時,采集的數(shù)據(jù)見下表: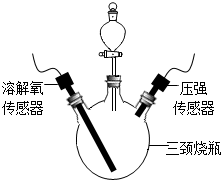
(5)步驟1中檢查裝置氣密性的方法為:先在分液漏斗中加水,再打開活塞,觀察到序號 鹽酸pH P反應(yīng)前 P反應(yīng)后 DO反應(yīng)前 DO反應(yīng)后 開始降低所需時間/s 實驗① 2.0 90.8 91.8 5.2 4.3 131 實驗② 3.0 90.8 91.5 5.0 3.7 68 實驗③ 4.0 90.8 90.3 4.9 3.4 24 實驗④ 5.0 90.8 90.5 4.9 3.7 98 實驗⑤ 6.0 90.8 90.6 4.4 3.7 175 (填現(xiàn)象),表明裝置的氣密性良好。
(6)實驗①和實驗②反應(yīng)后壓強變大。進(jìn)行實驗③時,觀察到溶液中有氣泡冒出,反應(yīng)后體系內(nèi)壓強卻變小了,變小的原因是。
(7)分析表中數(shù)據(jù),在該實驗條件下,下列說法正確的有(填字母)。
a.當(dāng)pH=2時,鐵粉與氧氣的銹蝕速率最快
b.稀鹽酸中的溶解氧含量與鹽酸的pH有關(guān)
c.鐵粉和鹽酸,氧氣在剛接觸時不是同時發(fā)生反應(yīng)發(fā)布:2024/12/24 10:30:2組卷:229引用:4難度:0.5 -
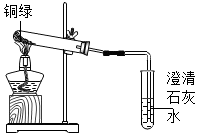 2.銅器長時間暴露在空氣中會生成銅綠[Cu2(OH)2CO3],銅綠不穩(wěn)定,受熱會生成三種氧化物。
2.銅器長時間暴露在空氣中會生成銅綠[Cu2(OH)2CO3],銅綠不穩(wěn)定,受熱會生成三種氧化物。
(1)根據(jù)銅綠的化學(xué)式,你認(rèn)為銅綠的形成是銅與、和氧氣共同作用的結(jié)果,你判斷的依據(jù)是。
(2)為探究銅綠的組成,小芳同學(xué)從銅器上取下適量的銅綠放入下圖所示的裝置中,加熱后,可能出現(xiàn)的現(xiàn)象是。
(3)請你設(shè)計一個實驗證明銅綠的組成中含有銅元素(寫出操作步驟、現(xiàn)象和結(jié)論)操作步驟 現(xiàn)象 結(jié)論 發(fā)布:2024/11/10 8:0:1組卷:28引用:1難度:0.4 -
3.化學(xué)小組對鋼鐵的銹蝕進(jìn)行實驗研究。
Ⅰ.探究鋼鐵銹蝕的基本條件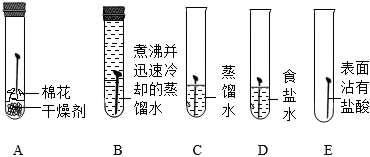
(1)一段時間后,C、D、E中鐵釘生銹,A、B中鐵釘無明顯銹蝕。由A、B、C的現(xiàn)象可知,鐵的銹蝕是鐵跟(填化學(xué)式)等物質(zhì)作用的過程。D中鐵釘比C中鐵釘銹蝕程度嚴(yán)重,說明。
(2)使用自來水重新進(jìn)行如圖實驗,一段時間后發(fā)現(xiàn)試管B中鐵釘生銹了,其可能的原因是。
Ⅱ.探究食鹽水對鋼鐵腐蝕速率的影響
用如圖裝置進(jìn)行實驗,錐形瓶中放生鐵粉末,滴管中預(yù)先加入2mL不同濃度的食鹽水,并用氧氣傳感器測定錐形瓶內(nèi)的氧氣濃度,數(shù)據(jù)如下表所示: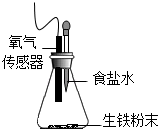
(3)該實驗探究的是實驗組 生鐵粉末質(zhì)量 食鹽水濃度 3min時瓶內(nèi)氧氣濃度 實驗① 3.5g 4% 18.96% 實驗② 3.5g 8% 18.56% 實驗③ 3.5g 16% 18.28% 實驗④ 3.5g 24% 17.99% 對鋼鐵腐蝕速率的影響,其實驗結(jié)論是。
(4)查閱資料得知,食鹽水中的氯離子能破壞鋼筋表面的鈍化膜(其原理如圖所示),并促使鐵發(fā)生一系列反應(yīng)得到Fe(OH)3,F(xiàn)e(OH)3在空氣中風(fēng)化失水后變成氧化鐵。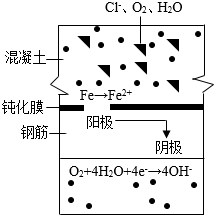
①氯離子破壞鋼筋表面的鈍化膜的過程中,從陽極向陰極轉(zhuǎn)移的微粒是。
②鋼筋銹蝕過程中得到氧化鐵的反應(yīng)方程式為。
Ⅲ.探究水樣的pH及溶解氧濃度對鋼鐵腐蝕速率的影響
步驟1:按如圖連接好裝置,檢查裝置氣密性。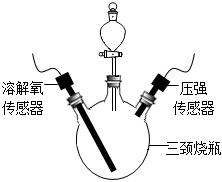
步驟2:向三頸燒瓶中放入3.5g生鐵粉末,向分液漏斗內(nèi)加入10mL不同濃度的稀鹽酸。
步驟3:將鹽酸全部注入三頸燒瓶內(nèi),關(guān)閉分液漏斗活塞,同時采集數(shù)據(jù)見下表:
(5)步驟1中檢查裝置氣密性的方法為序號 鹽酸pH 壓強p/kPa 溶解氧/mg?L-1 p反應(yīng)前 p反應(yīng)后 DO反應(yīng)前 DO反應(yīng)后 開始降低所需時間/s 實驗① 2.0 90.8 91.8 5.2 4.3 131 實驗② 3.0 90.8 91.5 5.0 3.7 68 實驗③ 4.0 90.8 90.3 4.9 3.4 24 實驗④ 5.0 90.8 90.5 4.9 3.7 98 實驗⑤ 6.0 90.8 90.6 4.4 3.7 175 。
(6)實驗1和實驗2反應(yīng)后壓強變大的主要原因是(用化學(xué)方程式表示)。
(7)進(jìn)行實驗3時,觀察到溶液中有氣泡冒出,反應(yīng)后體系內(nèi)壓強卻變小了。其原因是。
(8)分析表中數(shù)據(jù),在該實驗條件下,下列說法正確的有。
A.當(dāng)pH=2時,鐵粉與氧氣的銹蝕速率最快
B.稀鹽酸中的溶解氧含量與鹽酸的pH有關(guān)
C.鐵粉和鹽酸,氧氣的反應(yīng)可以同時發(fā)生發(fā)布:2024/12/25 12:0:1組卷:264引用:3難度:0.7


