(NH4)2Cr2O7用于有機合成催化劑,媒染劑,顯影液等。某化學興趣小組對(NH4)2Cr2O7的部分性質及組成進行探究。已知:Cr2O72-(橙色)+H2O?2Cr2O42-(黃色)+2H+。回答下列問題:
(1)在試管中加入少量(NH4)2Cr2O7固體,滴加足量濃KOH溶液,振蕩、微熱,觀察到的主要現象是固體溶解、有刺激性氣味氣體放出有刺激性氣味氣體放出、溶液變為黃色溶液變為黃色。
(2)為探究(NH4)2Cr2O7(摩爾質量252g/mol)的分解產物,按圖連接好裝置,在A中加入2.52g樣品進行實驗。

①C的作用是防止水蒸氣進入裝置B中防止水蒸氣進入裝置B中。
②實驗操作步驟:a.打開K1和K2,緩緩通入N2→b.點燃酒精燈,加熱→c.熄滅酒精燈→d.→e.關閉K1和K2→f.稱量A和B,則d的操作為繼續通入N2繼續通入N2。
③加熱A至恒重,觀察到D中溶液不變色,同時測得A、B中質量變化分別為1.00g、0.72g,寫出重鉻酸銨加熱分解反應的化學方程式(NH4)2Cr2O7 △ Cr2O3+N2↑+4H2O(NH4)2Cr2O7 △ Cr2O3+N2↑+4H2O。
(3)實驗室常用甲醛法測定含(NH4)2Cr2O7的樣品中氮的質量分數,其反應原理為:2Ba2++Cr2O72-+H2O═2BaCrO4+2H+;4NH4++6HCHO═3H++6H2O+(CH2)6N4H+;(CH2)6N4H+?(CH2)6N4+H+,K=7×10-6,然后用NaOH標準溶液滴定反應生成的酸。
實驗步驟:
Ⅰ.稱取樣品ag,配成250mL溶液。
Ⅱ.量取25.00mL樣品溶液,用氯化鋇溶液使Cr2O72-完全沉淀后,加入10mL 20%的中性甲醛溶液,搖勻、靜置5min。
Ⅲ.以酚酞作指示劑,用cmol?L-1標準NaOH溶液滴定,記錄數據。
Ⅳ.重復步驟Ⅱ、Ⅲ2~3次,處理數據。
①滴定終點的顏色變化無色變為淺紅色無色變為淺紅色。
②滴定操作使用的玻璃儀器主要有堿式滴定管堿式滴定管。
③步驟Ⅲ發生反應的離子方程式是H++OH-=H2O,(CH2)6N4H++OH-=(CH2)6N4+H2OH++OH-=H2O,(CH2)6N4H++OH-=(CH2)6N4+H2O。
④若實驗平均消耗NaOH溶液的體積為bmL,該樣品中氮的質量分數的計算式為7bca%7bca%。(用含a、b、c式子表示,需要化簡)
⑤下列情況會導致測定結果偏低的是bcbc。(填序號)
a.若實驗中使用的甲醛常混有微量甲酸
b.若步驟Ⅱ沒有靜置5min
c.若滴定終點讀數時,俯視標準液液面
△
△
7
bc
a
7
bc
a
【考點】探究物質的組成或測量物質的含量.
【答案】有刺激性氣味氣體放出;溶液變為黃色;防止水蒸氣進入裝置B中;繼續通入N2;(NH4)2Cr2O7 Cr2O3+N2↑+4H2O;無色變為淺紅色;堿式滴定管;H++OH-=H2O,(CH2)6N4H++OH-=(CH2)6N4+H2O;%;bc
△
7
bc
a
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:130引用:4難度:0.5
相似題
-
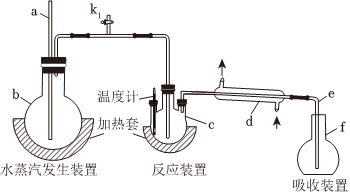 1.為測定某氟化稀土樣品中氟元素的質量分數進行如下實驗。利用高氯酸(高沸點酸)將樣品中的氟元素轉化為氟化氫(低沸點酸)蒸出,再通過滴定測量,實驗裝置如圖所示。(1)a的作用是 ,f儀器的名稱是(2)檢查裝置氣密性:首先(填操作),關閉k1,微熱c,f中有氣泡冒出;停止加熱,導管e內形成一段穩定的水柱,說明裝置氣密性良好。(3)c中加入一定體積高氯酸和mg氟化稀土樣品,f中盛有滴加酚酞的NaOH溶液。加熱b、c,使水蒸氣進入c。①下列物質可代替高氯酸的是(填序號)A.硝酸 B.鹽酸 C.硫酸 D.磷酸②實驗中除有HF氣體外,可能還有少量SiF4(易水解)氣體生成,若有SiF4生成,實驗結果將(填“偏高”“偏低”或”不受影響”)。③若觀察到f中溶液紅色褪去,需要向f中及時補加NaOH溶液,否則會使實驗結果偏低,原因是。(4)向餾出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA標準溶液滴定剩余的La3+(La3+與EDTA按1:1絡合),消耗EDTA標準溶液V2 mL,則氟化稀土樣品中氟的質量分數為。(F的相對原子質量為19)(5)用樣品進行實驗前,需要用0.084g氟化鈉代替樣品進行實驗,改變條件(高氯酸用量、反應溫度、蒸餾實驗),測量并計算出氟元素質量,重復多次。該操作的目的是。發布:2025/1/18 8:0:1組卷:24引用:1難度:0.5
1.為測定某氟化稀土樣品中氟元素的質量分數進行如下實驗。利用高氯酸(高沸點酸)將樣品中的氟元素轉化為氟化氫(低沸點酸)蒸出,再通過滴定測量,實驗裝置如圖所示。(1)a的作用是 ,f儀器的名稱是(2)檢查裝置氣密性:首先(填操作),關閉k1,微熱c,f中有氣泡冒出;停止加熱,導管e內形成一段穩定的水柱,說明裝置氣密性良好。(3)c中加入一定體積高氯酸和mg氟化稀土樣品,f中盛有滴加酚酞的NaOH溶液。加熱b、c,使水蒸氣進入c。①下列物質可代替高氯酸的是(填序號)A.硝酸 B.鹽酸 C.硫酸 D.磷酸②實驗中除有HF氣體外,可能還有少量SiF4(易水解)氣體生成,若有SiF4生成,實驗結果將(填“偏高”“偏低”或”不受影響”)。③若觀察到f中溶液紅色褪去,需要向f中及時補加NaOH溶液,否則會使實驗結果偏低,原因是。(4)向餾出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA標準溶液滴定剩余的La3+(La3+與EDTA按1:1絡合),消耗EDTA標準溶液V2 mL,則氟化稀土樣品中氟的質量分數為。(F的相對原子質量為19)(5)用樣品進行實驗前,需要用0.084g氟化鈉代替樣品進行實驗,改變條件(高氯酸用量、反應溫度、蒸餾實驗),測量并計算出氟元素質量,重復多次。該操作的目的是。發布:2025/1/18 8:0:1組卷:24引用:1難度:0.5 -
2.煤氣化是有效利用化石能源手段之一,有關反應如下:
①C+H2OCO+H2 ②CO+H2O高溫CO2+H2一定條件
獲得的氣體稱為水煤氣。某研究性學習小組為探究氣體的成分進行了如下實驗:
[實驗]使水蒸氣通過灼熱的焦炭,收集反應后流出的氣體。
[提出假設]對氣體的成分提出了三種假設。
假設1:該氣體是 CO、H2。
假設2:該氣體是 CO、H2、H2O。
(1)假設3:。
[設計實驗方案,驗證假設]
他們擬用下圖中提供的儀器,選擇必要的試劑,設計一個實驗,驗證上述假設(加熱裝置和導管等在圖中略去,實驗前裝置內部的空氣已經排盡)。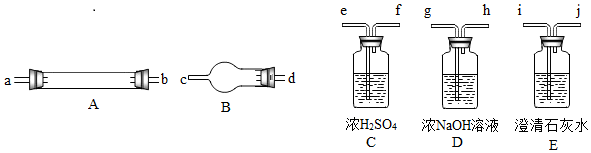
(2)按氣流從左至右連接各儀器,用題中小寫字母表示接口的連接順序(儀器可重復使用):
混合氣→dc→→→ij→→→→ij;
(3)儀器A中需加入試劑的是,其中反應的化學方程式是;
(4)儀器B中需加入試劑的名稱是,其作用是;
[思考與交流]
(5)本實驗的尾氣需要處理,處理的方法為。
(6)某同學認為增加焦炭的量可以提高化學反應①的速率,你是否同意他的說法,并簡述理由。發布:2024/12/30 14:0:1組卷:34引用:4難度:0.5 -
3.為探究礦石樣品X(僅含兩種元素)的組成和性質,某同學設計并完成如圖實驗:
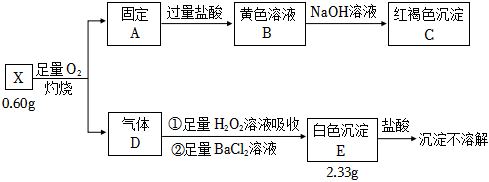
請回答:
(1)X含有的元素。
(2)X的化學式。
(3)紅褐色沉淀C是。
(4)氣體D通入足量H2O2中發生反應①的化學方程式。發布:2024/12/30 14:30:1組卷:15引用:3難度:0.7


