菠菜營養豐富,素有“蔬菜之王”之稱,在營養價值上還是一種高效的補鐵劑.長期以來民間流傳著“菠菜根比菠菜莖葉更有營養”、“菠菜不能與豆腐同食”等說法.
某校化學興趣小組的同學擬通過實驗來探究以下問題:
(1)菠菜中是否含有豐富的鐵.
(2)菠菜中是否含有某種酸類物質.
(3)菠菜根中鐵的含量是否比菠菜莖和葉高.
(4)菠菜為什么與豆腐不能同食.
該小組同學通過上網查詢,獲得以下資料:
①菠菜中確實含有一種有機酸,其化學名稱為乙二酸(化學式為C2H2O4),俗稱草酸.②草酸的酸性比醋酸強.③豆腐中含有豐富的鈣元素. ④草酸鈣是一種無色晶體,不溶于水,是尿道結石的主要成分.⑤Fe2+遇氧化性物質能轉化為Fe3+.⑥含Fe3+的溶液遇KSCN(硫氰化鉀)溶液呈血紅色,而含 Fe2+的溶液則不能.
該小組設計了如下實驗方案:
實驗Ⅰ:
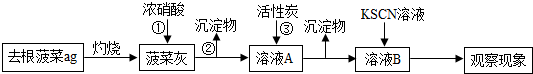
實驗Ⅱ:
取有根菠菜ag使用相同儀器和試劑,重復實驗Ⅰ的過程,觀察現象時發現溶液B的紅色比實驗Ⅰ中得到的溶液紅色深.
實驗Ⅲ:
另將菠菜在少量開水中煮沸2~3分鐘,濾去菠菜,得濾液C.向濾液C中加入足量的Ca(OH)2溶液,再加入足量的醋酸,觀察現象.
請回答下列問題:
(1)操作①中加入的濃硝酸具有強氧化性.由此推知溶液A中含有Fe3+Fe3+(填“Fe2+”或“Fe3+”).操作②的名稱為過濾過濾,操作過程中所需使用的玻璃儀器有燒杯燒杯、玻璃棒玻璃棒、漏斗漏斗.
(2)操作③中加入活性炭的作用吸附水中的可溶性雜質吸附水中的可溶性雜質.
(3)實驗Ⅱ中得到的溶液B的紅色比實驗Ⅰ中溶液B的紅色深,可以說明菠菜根中鐵元素的含量與菠菜莖、葉相比高高(填“高”、“低”或“相同”).
(4)實驗Ⅲ中向濾液C加入Ca(OH)2溶液后,再加入足量的醋酸,其目的是排除碳酸鈣的干擾.若醋酸的化學式可用HAc表示,寫出碳酸鈣與醋酸發生反應的化學方程式CaCO3+2HAc═CaAc2+H2O+CO2↑CaCO3+2HAc═CaAc2+H2O+CO2↑.在加入醋酸后發現仍有不溶性物質存在,你認為該物質可能是草酸鈣草酸鈣,則菠菜中含有含有(選填“含有”、“不含有”或“無法證明”)草酸.
(5)試解釋菠菜不能與豆腐同食的理由:與豆腐中含有豐富的鈣反應產生草酸鈣與豆腐中含有豐富的鈣反應產生草酸鈣.
【答案】Fe3+;過濾;燒杯;玻璃棒;漏斗;吸附水中的可溶性雜質;高;CaCO3+2HAc═CaAc2+H2O+CO2↑;草酸鈣;含有;與豆腐中含有豐富的鈣反應產生草酸鈣
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:27引用:6難度:0.5
相似題
-
1.碳酸氫鈉是一種應用廣泛的鹽,化學小組對其進行了探究。
(1)NaHCO3可稱為鈉鹽或碳酸氫鹽,它是由Na+和(填離子符號)構成,醫療上能用于治療胃酸(含有鹽酸)過多癥,反應的化學方程式為。
【提出問題】實驗室中如何制取少量NaHCO3?
【查閱資料】
材料一:侯氏制堿的原理:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。△
材料二:研究發現,NaHCO3溶于水時吸收熱量,Na2CO3溶于水時放出熱量。
【實驗制備】根據侯氏制堿原理設計如圖1所示裝置制取NaHCO3。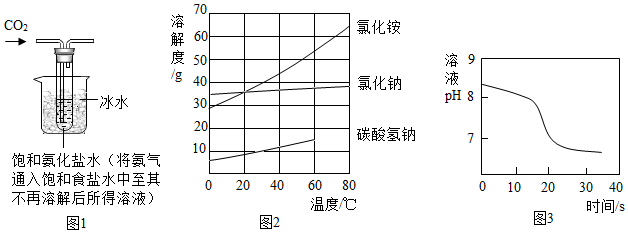
反應結束后,將試管中的混合物過濾洗滌,低溫烘干得白色固體。
(2)燒杯中冰水的作用是。
(3)能進一步確認該白色固體是NaHCO3的實驗方案是(須用到的儀器和藥品:試管、溫度計、水)。
(4)如圖2中碳酸氫鈉的溶解度在60℃后無數據的原因可能是。
【性質探究】
常溫下,取一定量的NaHCO3溶液于燒杯中,插入pH傳感器,向燒杯中持續滴加CaCl2溶液,有白色沉淀生成,當溶液的pH變為6.68時開始有無色氣體產生。反應過程中溶液的pH隨時間變化如圖3所示。
【查閱資料】
材料三NaHCO3溶于水后,少量的能同時發生如下變化:HCO-3
變化①:+H2O→H2CO3+OH-;HCO-3
變化②:→HCO-3+H+。CO2-3
材料四:溶液的酸堿性與溶液中H+和OH-數目的相對大小有關。常溫下,當單位體積溶液中OH-的數目大于H+的數目時溶液的pH>7,反之pH<7;單位體積溶液中所含的H+數目越大,溶液的pH越小。
【交流反思】
(5)NaHCO3溶液顯(填“酸”“堿”或“中”)性,結合材料三、四從微觀角度說明原因:。
(6)根據本實驗,下列說法錯誤的是(填字母)。
a.pH<6.68時生成的無色氣體為CO2
b.從0~30s,單位體積溶液中H+數目不斷增大
c.不能用CaCl2溶液鑒別Na2CO3和NaHCO3溶液發布:2024/12/25 15:30:1組卷:589引用:4難度:0.5 -
2.關于鹽的性質研究是一項重要的課題,某興趣小組以“探究碳酸氫鈉的性質”為主題開展項目式學習。
【任務一】認識碳酸氫鈉
(1)下列關于碳酸氫鈉的說法正確的是。
A.碳酸氫鈉是由Na+和構成HCO-3
B.碳酸氫鈉俗稱純堿
C.碳酸氫鈉醫療上能用于治療胃酸過多癥
D.碳酸氫鈉難溶于水
【任務二】探究碳酸氫鈉的性質
(2)探究碳酸氫鈉與稀鹽酸反應:興趣小組取適量碳酸氫鈉粉末于甲試管中,加入稀鹽酸,如圖1所示,觀察到甲試管中有氣泡產生,乙中,說明碳酸氫鈉能與稀鹽酸反應生成CO2,寫出試管甲中反應的化學方程式。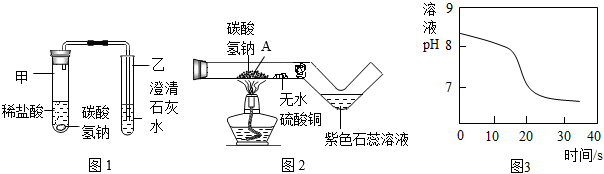
(3)探究碳酸氫鈉的熱穩定性:用酒精燈充分加熱玻璃管,如圖2所示。
資料:無水硫酸銅呈白色,遇水后呈藍色
①發現玻璃管內無水硫酸銅變藍,紫色石蕊溶液變紅,說明碳酸氫鈉受熱易分解,且有和二氧化碳生成。
②實驗后興趣小組同學猜想玻璃管A處固體產物僅是Na2CO3而不含有NaOH,請設計實驗證明(寫出具體步驟和現象):。
(4)常溫下,興趣小組同學取一定量的NaHCO3溶液于燒杯中,插入pH傳感器,向燒杯中持續滴加CaCl2溶液,有白色沉淀生成,當溶液的pH變為6.68時開始有無色氣體產生。反應過程中溶液的pH隨時間變化如圖3所示。
【查閱資料】
材料一:NaHCO3溶于水后,少量的能同時發生如下變化:HCO-3
變化①:+H2O→H2CO3+OH-HCO-3
變化②:→HCO-3+H+CO2-3
材料二:溶液的酸堿性與溶液中H+和OH-數目的相對大小有關。常溫下,當單位體積溶液中OH-的數目大于H+的數目時溶液的pH>7,反之pH<7;單位體積溶液中所含的H+數目越大,溶液的pH越小。
①根據上述實驗可知NaHCO3溶液顯堿性,結合材料一、二從微觀角度說明原因:。
②根據本實驗,可知從0~30s,單位體積溶液中H+數目不斷(填“增大”或“減小”)。發布:2024/12/25 17:0:2組卷:94引用:2難度:0.4 -
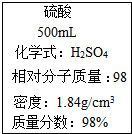 3.圖是一瓶濃硫酸標簽上的部分內容,某探究小組的同學對這瓶硫酸進行了如下探究,請你參與.
3.圖是一瓶濃硫酸標簽上的部分內容,某探究小組的同學對這瓶硫酸進行了如下探究,請你參與.
[查閱資料]濃硫酸有強腐蝕性,溶于水會放熱;硫酸鋇不溶于水也不溶于酸.
[探究一]濃硫酸稀釋時會放熱.
(1)稀釋濃硫酸時,所需儀器主要有,應如何稀釋濃硫酸?.測量稀釋前后溶液的溫度,有明顯升高的現象.結論:濃硫酸溶于水放熱.
[探究二]稀硫酸與氫氧化鈉溶液能發生反應.圖10
(2)稀硫酸與氫氧化鈉溶液反應的化學方程式為實驗步驟 實驗現象 實驗結論 先用pH試紙測定稀硫酸的pH,再逐滴加入氫氧化鈉溶液并不斷振蕩,同時測混合液的pH pH逐漸變大,
最后pH≥7稀硫酸與氫氧化鈉
溶液能發生反應.
(3)實驗中僅從溶液pH變大,而不強調pH≥7,不能得出稀硫酸與氫氧化鈉溶液一定發生反應的結論,理由是.
[探究三]由于該試劑瓶瓶口密封簽已破損,同學們懷疑該濃硫酸的質量分數與標簽不相符.
[提出問題]該濃硫酸的質量分數是否發生變化?
[實驗探究](4)取該濃硫酸和足量BaCl2溶液反應,過濾、洗滌、干燥沉淀.實驗中如何確定硫酸已完全反應.
(5)為達到實驗目的,實驗中必須要測知的數據是.
[探究結論](6)由實驗測得的數據計算出的硫酸的質量分數與標簽不符.該硫酸的質量分數應98%(填“大于”或“小于”).發布:2025/1/6 8:0:1組卷:38引用:1難度:0.5


