侯德榜發明的侯氏制堿法為中國民族化學工業贏得了聲譽。
(1)侯氏制堿的主要產品是Na2CO3,其俗名是 純堿或蘇打純堿或蘇打。
(2)實驗室模擬侯氏制堿,在濃氨水中加入NaCl粉末,配成飽和氨鹽水,用下列裝置制備NaHCO3,反應方程式為NaCl+NH3?H2O+CO2=NaHCO3↓+NH4Cl。
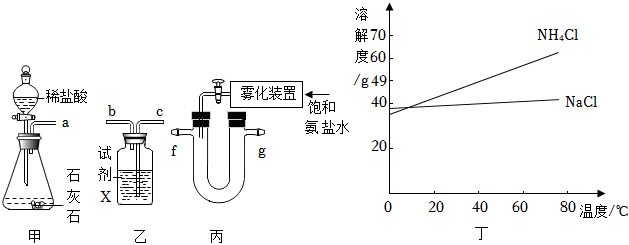
①甲裝置中分液漏斗的優點是 可控制反應的速率可控制反應的速率,甲裝置錐形瓶中發生反應的化學方程式為 CaCO3+2HCl=CaCl2+H2O+CO2↑CaCO3+2HCl=CaCl2+H2O+CO2↑。
②乙裝置中的試劑X用于吸收HCl,但不與CO2反應,則試劑X可為 DD(填序號)。
A.濃硫酸
B.NaOH溶液
C.Ca(OH)2溶液
D.NaHCO3溶液
③乙裝置氣流的進氣接口為 cc(填“b”或“c”)。
(3)分離丙裝置U形管內的混合物得到NaHCO3固體和NH4Cl溶液。
①灼燒NaHCO3發生反應2NaHCO3 △ Na2CO3+H2O↑+CO2↑,若灼燒前后固體質量減少0.62g,則產品Na2CO3的質量為 1.061.06g。(請寫出完整的計算過程)
②已知:NH4Cl和NaCl溶解度曲線如圖丁所示。
向NH4Cl溶液中加入NaCl粉末,可使NH4Cl結晶析出。為使剩余的NH4Cl和NaCl混合溶液中的NH4Cl充分結晶析出,比較適合采用的結晶方式是 降溫結晶降溫結晶。
△
【答案】純堿或蘇打;可控制反應的速率;CaCO3+2HCl=CaCl2+H2O+CO2↑;D;c;1.06;降溫結晶
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:97引用:1難度:0.7
相似題
-
1.侯德榜是我國著名的化學家,為純堿和氮肥工業技術的發展作出了杰出的貢獻,他發明的侯氏制堿法大大提高了原料的利用率,其工業流程大致如圖:
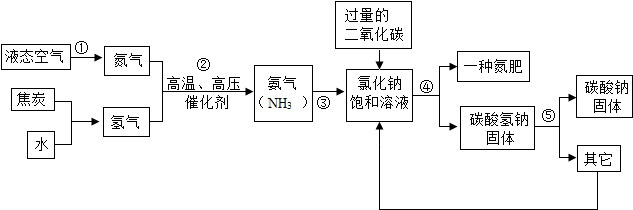
(1)上述流程中,用到的原料有空氣、焦炭、水、二氧化碳以及。
(2)若上述流程中,“一種氮肥”指的是一種銨態氮肥,則其化學式是。
(3)上述流程中,為了節約成本,可循環利用的物質是。發布:2024/11/15 8:0:2組卷:147引用:2難度:0.5 -
2.侯德榜是我國著名的化學家,為純堿和氮肥工業技術的發展做出了杰出的貢獻,他發明的侯氏制堿法大大提高了原料的利用率,其工藝流程大致如下圖所示:

(1)上述流程中,用到的原料有空氣、焦炭、水、二氧化碳、等;
(2)上述流程中,可循環利用的物質是;
(3)上述流程中,“一種氮肥”的化學式是。發布:2024/11/15 8:0:2組卷:22引用:1難度:0.5 -
3.海洋是人類寶貴的自然資源,海水“曬鹽”和海水“制堿”體現了人類利用和改造自然的智慧,請根據粗鹽“制堿”的流程圖(如圖)回答問題:

(1)步驟Ⅰ除雜中,常見的方法有兩種:一是物理方法,即用NaCl溶液浸洗粗鹽,溶解除去其中的可溶性雜質,則浸洗溶液應選用NaCl的(填“飽和”或“不飽和”)溶液;二是化學方法,操作步驟依次為:加水溶解→加過量試劑①→加過量試劑②→過濾→加適量鹽酸,以下試劑①②組合選用合理的是。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步驟Ⅲ先向飽和食鹽水中通入氨氣,再通入二氧化碳,這樣做的目的是,寫出步驟Ⅲ反應的化學方程式。
(3)步驟Ⅳ發生的反應屬于反應(填基本反應類型)。
(4)我國化學家侯德榜創立的聯合制堿法的優點有。
A.無“索爾維氨堿法”中的廢棄物CaCl2生成,有利于保護環境
B.大大提高了食鹽的利用率,節約了成本
C.將“制堿”與制氨生產聯合起來,同時析出的NH4Cl晶體可用作復合肥發布:2024/12/24 10:30:2組卷:552引用:9難度:0.5


