當前位置:
知識點挑題
請展開查看知識點列表
>
<
更多>>
 已完結
已完結
|
期末復習
典型試卷
考前必刷
瀏覽次數:960
更新:2025年06月03日
|
 已完結
已完結
|
熱點預測
高考復習
難題搶練
瀏覽次數:1199
更新:2025年05月26日
|
731.構造原理揭示的電子排布能級順序,實質是各能級能量高低順序.若以E表示某能級的能量,以下能量大小順序中正確的是( )
A.E(3s)>E(3p)>E(3d) B.E(3s)>E(2s)>E(1s) C.E(4f)<E(4s)<E(3d) D.E(5s)>E(4s)>E(4f) 發布:2024/12/30 16:30:2組卷:355引用:11難度:0.5732.下列各組元素按電負性大小排列正確的是( )
A.F>N>O B.O>Cl>F C.As>P>S D.Cl>S>As 發布:2024/12/30 16:30:2組卷:6引用:3難度:0.6733.下列敘述正確的是( )
A.同周期元素中第VIA族元素的第一電離能最大 B.主族元素的原子形成簡單離子時的化合價的絕對值都等于它的族序數 C.第IA、ⅡA族元素的原子半徑越大,元素的第一電離能越大 D.同一主族自上而下,元素的第一電離能逐漸減小 發布:2024/12/30 16:30:2組卷:6引用:3難度:0.5734.下列有關構造原理的說法錯誤的是( )
A.原子核外電子填充3p、3d、4s能級的順序一般為3p→4s→3d B.某基態原子部分核外電子的排布式為3s24s2 C.在多電子原子中,電子最后填入的能級不一定是原子最外層上的能級 D.從第三能層開始出現能級交錯現象,即電子填入能級的順序與能層順序不同 發布:2024/12/30 16:30:2組卷:14引用:2難度:0.7735.價電子滿足4s和3d為半滿的元素是( )
A.Mn B.V C.Cr D.Cu 發布:2024/12/30 16:30:2組卷:8引用:2難度:0.7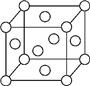 736.A、B、X、Y、Z是元素周期表前四周期中的常見元素,原子序數依次增大.A元素可形成自然界硬度最大的單質;B與A同周期,核外有三個未成對電子;X原子的第一電離能至第四電離能分別是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常溫常壓下,Y單質是固體,其氧化物是形成酸雨的主要物質;Z的一種同位素的質量數為63,中子數為34.請回答下列問題:
736.A、B、X、Y、Z是元素周期表前四周期中的常見元素,原子序數依次增大.A元素可形成自然界硬度最大的單質;B與A同周期,核外有三個未成對電子;X原子的第一電離能至第四電離能分別是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常溫常壓下,Y單質是固體,其氧化物是形成酸雨的主要物質;Z的一種同位素的質量數為63,中子數為34.請回答下列問題:
(1)AY2是一種常用的溶劑,為分子(填“極性”或“非極性”),分子中存在個σ鍵.
(2)X形成的單質與NaOH溶液反應的離子方程式為,超高導熱絕緣耐高溫納米XB在絕緣材料中應用廣泛,其晶體與金剛石類似,屬于晶體.B的最簡單氫化物容易液化,理由是.
(3)X、氧、B元素的電負性由大到小的順序為(用元素符號作答).
(4)Z的基態原子核外電子排布式為.元素Z與人體分泌物中的鹽酸以及空氣反應可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不僅是一種弱酸而且也是一種自由基,具有極高的活性.下列說法或表示不正確的是(填序號)
①氧化劑是O2
②HO2在堿中不能穩定存在
③氧化產物是HO2
④1mol Z參加反應有1mol電子發生轉移
(5)已知Z的晶胞結構如圖所示,又知Z的密度為9.00g/cm3,則晶胞邊長為cm.ZYO4常作電鍍液,其中的空間構型是YO2-4,Y原子的雜化軌道類型是雜化.發布:2024/12/30 16:30:2組卷:9引用:2難度:0.3737.已知:元素X的電負性數值為2.5,元素Y的電負性數值為3.5,元素Z的電負性數值為1.2,元素W的電負性數值為2.4。上述四種元素中,最容易形成離子化合物的兩種元素是( )
A.X與Y B.X與W C.Y與Z D.Y與W 發布:2024/12/30 16:30:2組卷:7引用:5難度:0.8738.已知X-X、Y-Y、Z-Z的鍵長分別為198 pm、74 pm、154 pm,則它們單質分子的穩定性是( )
A.X2>Y2>Z2 B.Z2>Y2>X2 C.Y2>X2>Z2 D.Y2>Z2>X2 發布:2024/12/30 16:30:2組卷:4引用:2難度:0.8739.圖①和圖②分別是1s電子的概率密度分布圖和電子云輪廓圖。下列認識正確的是( )

A.圖①中的每個小點表示1個電子 B.圖②表明1s電子云輪廓圖呈球形,有無數條對稱軸 C.圖②表示1s電子只能在球體內出現 D.不同能層的s電子云的半徑相等 發布:2024/12/30 16:30:2組卷:12引用:4難度:0.6740.下列有關核外電子排布的式子不正確的是( )
A.24Cr的電子排布式:1s22s22p63s23p63d54s1 B.K的簡化電子排布式:[Ar]4s1 C.N原子的電子排布圖: 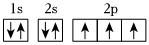
D.S原子的電子排布圖: 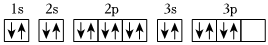 發布:2024/12/30 16:30:2組卷:169引用:17難度:0.7
發布:2024/12/30 16:30:2組卷:169引用:17難度:0.7



