當前位置:
知識點挑題
請展開查看知識點列表
>
<
更多>>
 已完結
已完結
|
期末復習
典型試卷
考前必刷
瀏覽次數:692
更新:2025年06月03日
|
 已完結
已完結
|
熱點預測
高考復習
難題搶練
瀏覽次數:1068
更新:2025年05月26日
|
2641.某放熱反應A+B=2C,在反應過程中,斷裂1molA中的化學鍵消耗的能量為Q1kJ,斷裂1molB中的化學鍵消耗的能量為Q2kJ,形成1molC中的化學鍵釋放的能量為Q3kJ。下列說法中正確的是( )
A.Q1+Q2<Q3 B.Q1+Q2>Q3 C.Q1+Q2<2Q3 D.Q1+Q2>2Q3 發布:2024/12/30 3:0:4組卷:56引用:5難度:0.62642.40℃時,在氨-水體系中不斷通入CO2,各種離子的變化趨勢如圖所示。下列說法不正確的是( )
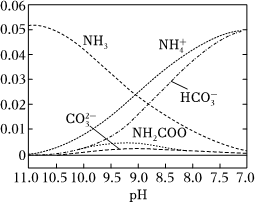
A.在pH=9.0時,c( )>c(NH+4)>c(NH2COO-)>c(HCO-3)CO2-3B.隨著CO2的通入, 不斷增大c(OH-)c(NH3?H2O)C.不同pH的溶液中存在關系:c( )+c(H+)═2c(NH+4)+c(CO2-3)+c(NH2COO-)+c(OH-)HCO-3D.在溶液中pH不斷降低的過程中,有含NH2COO-的中間產物生成 發布:2024/12/30 3:0:4組卷:76引用:4難度:0.72643.B3N3H6(無機苯)的結構與苯類似,也有大π鍵。下列關于B3N3H6的說法錯誤的是( )
A.其熔點主要取決于所含化學鍵的鍵能 B.形成大π鍵的電子全部由N提供 C.分子中B和N的雜化方式相同 D.分子中所有原子共平面 發布:2024/12/30 3:0:4組卷:784引用:17難度:0.52644.下列原電池裝置中,Cu作負極的是( )
A. 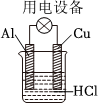
B. 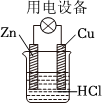
C. 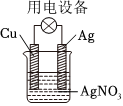
D. 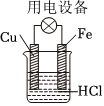 發布:2024/12/30 3:0:4組卷:83引用:2難度:0.9
發布:2024/12/30 3:0:4組卷:83引用:2難度:0.92645.MnCO3常用于醫藥、電焊條輔料等,以軟錳礦(主要成分為MnO2,還含有少量Fe2O3、Al2O3、SiO2、MgO、CaO等)為原料制備MnCO3的流程如圖:
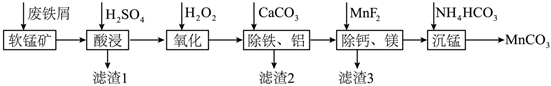
回答下列問題:
(1)廢鐵屑在使用前需要用熱的純堿溶液清洗表面油污,其清洗原理為(結合離子方程式和必要的語言解釋)。
(2)為了使廢鐵屑與軟錳礦在“酸浸”中充分反應,可采取的措施為;“酸浸”時主要發生反應的離子方程式為。
(3)“濾渣1”中含有的主要成分為。
(4)“氧化”過程中加入H2O2的量遠超理論量的原因為。
(5)加入CaCO3能“除鐵、鋁”的原因為。
(6)“沉錳”時發生反應的離子方程式為。
(7)MnO2的正交(棱與棱之間的夾角均為90°)晶胞結構如圖所示,晶胞參數分別為apm、bpm、cpm。其中Mn的配位數為;用NA表示阿伏加德羅常數的值,該晶體的密度為g?cm-3。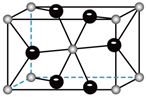 發布:2024/12/30 3:0:4組卷:16引用:3難度:0.6
發布:2024/12/30 3:0:4組卷:16引用:3難度:0.62646.在3個容積均為2.0L的恒容密閉容器中,反應H2O(g)+C(s)?CO(g)+H2(g)ΔH>0,分別在一定溫度下達到平衡,下列說法正確的是( )
容器溫度
(T1>T2)起始時物質的量/mol 平衡時物質的量/mol n(H2O) n(C) n(CO) n(H2) n(CO) Ⅰ T1 0.6 1.2 0 0 0.2 Ⅱ T1 1.2 1.2 0 0 x Ⅲ T2 0 0 0.6 0.6 y A.當溫度為T1時,該反應的化學平衡常數值為0.1 B.達到平衡時,容器Ⅱ中H2O的轉化率比容器Ⅰ中的小 C.若5min后容器Ⅰ中達到平衡,則H2O的平衡濃度為1.0mol/L D.達到平衡時,容器Ⅲ中CO的轉化率小于66.6% 發布:2024/12/30 3:0:4組卷:38引用:2難度:0.62647.下列說法中正確的是( )
A.氯化鈉水溶液在電流的作用下電離出Na+和Cl- B.硫酸鋇難溶于水,但硫酸鋇屬于強電解質 C.燃煤中加入CaO可以減少酸雨的形成及溫室氣體的排放 D.PM2.5是指粒徑不大于2.5nm的可吸入懸浮顆粒物 發布:2024/12/30 3:0:4組卷:32引用:2難度:0.62648.某化學興趣小組為了制取并探究氨氣性質,按下列裝置(部分夾持裝置已略去)進行實驗.[制取氨氣的反應原理:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O]△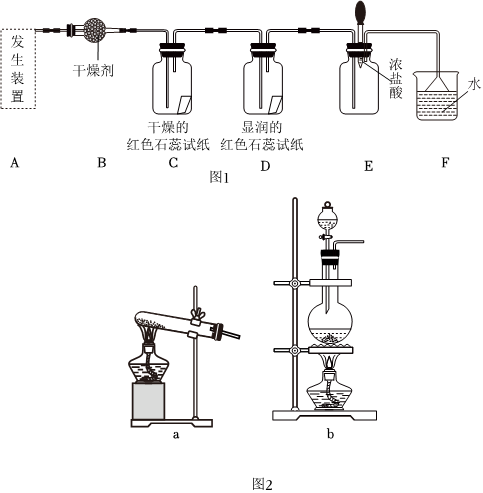
【實驗探究】
(1)利用上述原理,實驗室制取氨氣應選用圖2中發生裝置進行實驗.
(2)B裝置中的干燥劑可選用(填“堿石灰”或“濃硫酸”).
(3)用5.35g NH4Cl固體與足量Ca(OH)2反應,最多可制得標準狀況下氨氣的體積為L.(NH4Cl的摩爾質量為53.5g?mol-1)
(4)氣體通過C、D裝置時,試紙顏色會發生變化的是(填“C”或“D”).
(5)當實驗進行一段時間后,擠壓E裝置中的膠頭滴管,滴入1~2滴濃鹽酸,可觀察到的現象是.
(6)F裝置中倒置漏斗的作用.
【拓展應用】
(7)某同學用圖3所示裝置進行氨氣的性質實驗,根據燒瓶內產生紅色噴泉的現象,說明氨氣具有性質(填序號).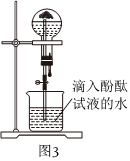
a.還原性 b.極易溶于水 c.與水反應生成堿性物質
(8)氨氣的用途很廣.如可用氨氣處理二氧化氮:8NH3+6NO2═7N2+12H2O該反應中氨氣體現(填“氧化性”或“還原性”).請你列舉出氨氣的另一種用途.發布:2024/12/30 3:0:4組卷:141引用:6難度:0.32649.設NA表示阿伏加德羅常數的值。下列說法正確的是( )
A.1molFeCl3在加熱條件下完全水解生成Fe(OH)3膠粒數為NA B.1L1mol?L-1NH4Br水溶液中 與H+離子數之和為NANH+4C.60g的乙酸和葡萄糖的混合物充分燃燒消耗O2分子數為2NA D.在標準狀況下,2.24L三氯甲烷中含有的共價鍵數目為0.4NA 發布:2024/12/30 3:0:4組卷:6引用:3難度:0.72650.化學在生產、生活和社會發展各方面發揮著關鍵性作用。下列敘述正確的是( )
A.純堿可用于治胃病 B.“靜電除塵”、“燃煤固硫”和“汽車尾氣凈化”的措施均涉及化學變化 C.工人將模具干燥后再注入熔融鋼水,是因為鐵與水高溫下會反應 D.太陽能電池的工作原理與原電池的相同 發布:2024/12/30 3:0:4組卷:7引用:3難度:0.7



