 消毒液、H2O2溶液都是常用消毒劑,興趣小組對兩種消毒劑進行了如下探究活動。
消毒液、H2O2溶液都是常用消毒劑,興趣小組對兩種消毒劑進行了如下探究活動。
【查閱資料】84消毒液的有效成分是次氯酸鈉(化學式為NaClO),則對應陰離子符號為 ClO-ClO-。
【異常現(xiàn)象】取少量84消毒液于試管中,滴加H2O2溶液,發(fā)現(xiàn)有大量氣泡產(chǎn)生。然后把帶火星的木條伸入試管中,帶火星的木條復燃,結果證明產(chǎn)生的氣體是氧氣。
【提出問題】在上述反應中,NaClO的作用是什么?
【作出猜想】
猜想一:作反應物,NaClO與H2O2溶液發(fā)生化學反應;
猜想二:作 催化劑催化劑,類似分解H2O2溶液制氧氣時MnO2的作用。
【實驗探究】
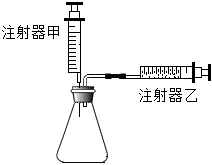
(1)按如圖所示組裝實驗裝置(固定裝置省略),加入藥品前檢查裝置氣密性,經(jīng)注射器甲向錐形瓶中注入10mL水,觀察到 注射器乙向外移動了10mL注射器乙向外移動了10mL則裝置的氣密性良好(忽略大氣壓、摩擦等其他因素對測量結果造成的影響,下同)。
(2)先向錐形瓶中加入20mL84消毒液,然后按如圖連接裝置,再將25mLH2O2溶液平均分5次經(jīng)注射器甲注入錐形瓶中,待注射器乙活塞不再向右移動后,記錄每次氣體的總體積,數(shù)據(jù)見表:
| / | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| H2O2溶液/mL | 5 | 5 | 5 | 5 | 5 |
| 注射器乙中氣體的總體積/mL | 105 | 210 | 300 | a | b |
猜想一
猜想一
(填“猜想一”或“猜想二”)是正確的,依據(jù)是 加入相同質量過氧化氫溶液,產(chǎn)生氣體體積不同
加入相同質量過氧化氫溶液,產(chǎn)生氣體體積不同
。【分析討論】
①NaClO與H2O2溶液反應除生成氧氣外,還生成氯化鈉和水。該反應的化學方程式為
NaClO+H2O2=O2↑+NaCl+H2O
NaClO+H2O2=O2↑+NaCl+H2O
。②表中數(shù)據(jù)b=
310
310
。③設過氧化氫溶液的密度為1g/mL,通常狀況下,氧氣密度為1.3g/L,則過氧化氫溶液中過氧化氫的質量百分數(shù)是
2.9%
2.9%
。【拓展反思】生活中常用消毒劑除84消毒液H2O2溶液外,還有75%酒精、過氧乙酸等。在使用各種消毒劑時,要考慮它們的性質。切記:科學使用,注意安全!
生活中下列使用消毒劑的做法正確的是
C
C
。A.不同的消毒劑可隨意混合使用
B.使用84消毒液的濃度越高越好
C.使用75%酒精消毒應遠離明火,防止火災
D.84消毒液、75%酒精等消毒劑不用密封保存
【答案】ClO-;催化劑;注射器乙向外移動了10mL;猜想一;加入相同質量過氧化氫溶液,產(chǎn)生氣體體積不同;NaClO+H2O2=O2↑+NaCl+H2O;310;2.9%;C
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:51引用:1難度:0.7
相似題
-
1.碳酸氫鈉是一種應用廣泛的鹽,化學小組對其進行了探究。
(1)NaHCO3可稱為鈉鹽或碳酸氫鹽,它是由Na+和(填離子符號)構成,醫(yī)療上能用于治療胃酸(含有鹽酸)過多癥,反應的化學方程式為。
【提出問題】實驗室中如何制取少量NaHCO3?
【查閱資料】
材料一:侯氏制堿的原理:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。△
材料二:研究發(fā)現(xiàn),NaHCO3溶于水時吸收熱量,Na2CO3溶于水時放出熱量。
【實驗制備】根據(jù)侯氏制堿原理設計如圖1所示裝置制取NaHCO3。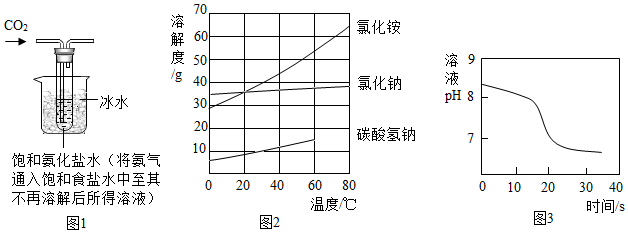
反應結束后,將試管中的混合物過濾洗滌,低溫烘干得白色固體。
(2)燒杯中冰水的作用是。
(3)能進一步確認該白色固體是NaHCO3的實驗方案是(須用到的儀器和藥品:試管、溫度計、水)。
(4)如圖2中碳酸氫鈉的溶解度在60℃后無數(shù)據(jù)的原因可能是。
【性質探究】
常溫下,取一定量的NaHCO3溶液于燒杯中,插入pH傳感器,向燒杯中持續(xù)滴加CaCl2溶液,有白色沉淀生成,當溶液的pH變?yōu)?.68時開始有無色氣體產(chǎn)生。反應過程中溶液的pH隨時間變化如圖3所示。
【查閱資料】
材料三NaHCO3溶于水后,少量的能同時發(fā)生如下變化:HCO-3
變化①:+H2O→H2CO3+OH-;HCO-3
變化②:→HCO-3+H+。CO2-3
材料四:溶液的酸堿性與溶液中H+和OH-數(shù)目的相對大小有關。常溫下,當單位體積溶液中OH-的數(shù)目大于H+的數(shù)目時溶液的pH>7,反之pH<7;單位體積溶液中所含的H+數(shù)目越大,溶液的pH越小。
【交流反思】
(5)NaHCO3溶液顯(填“酸”“堿”或“中”)性,結合材料三、四從微觀角度說明原因:。
(6)根據(jù)本實驗,下列說法錯誤的是(填字母)。
a.pH<6.68時生成的無色氣體為CO2
b.從0~30s,單位體積溶液中H+數(shù)目不斷增大
c.不能用CaCl2溶液鑒別Na2CO3和NaHCO3溶液發(fā)布:2024/12/25 15:30:1組卷:588引用:4難度:0.5 -
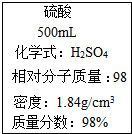 2.圖是一瓶濃硫酸標簽上的部分內容,某探究小組的同學對這瓶硫酸進行了如下探究,請你參與.
2.圖是一瓶濃硫酸標簽上的部分內容,某探究小組的同學對這瓶硫酸進行了如下探究,請你參與.
[查閱資料]濃硫酸有強腐蝕性,溶于水會放熱;硫酸鋇不溶于水也不溶于酸.
[探究一]濃硫酸稀釋時會放熱.
(1)稀釋濃硫酸時,所需儀器主要有,應如何稀釋濃硫酸?.測量稀釋前后溶液的溫度,有明顯升高的現(xiàn)象.結論:濃硫酸溶于水放熱.
[探究二]稀硫酸與氫氧化鈉溶液能發(fā)生反應.圖10
(2)稀硫酸與氫氧化鈉溶液反應的化學方程式為實驗步驟 實驗現(xiàn)象 實驗結論 先用pH試紙測定稀硫酸的pH,再逐滴加入氫氧化鈉溶液并不斷振蕩,同時測混合液的pH pH逐漸變大,
最后pH≥7稀硫酸與氫氧化鈉
溶液能發(fā)生反應.
(3)實驗中僅從溶液pH變大,而不強調pH≥7,不能得出稀硫酸與氫氧化鈉溶液一定發(fā)生反應的結論,理由是.
[探究三]由于該試劑瓶瓶口密封簽已破損,同學們懷疑該濃硫酸的質量分數(shù)與標簽不相符.
[提出問題]該濃硫酸的質量分數(shù)是否發(fā)生變化?
[實驗探究](4)取該濃硫酸和足量BaCl2溶液反應,過濾、洗滌、干燥沉淀.實驗中如何確定硫酸已完全反應.
(5)為達到實驗目的,實驗中必須要測知的數(shù)據(jù)是.
[探究結論](6)由實驗測得的數(shù)據(jù)計算出的硫酸的質量分數(shù)與標簽不符.該硫酸的質量分數(shù)應98%(填“大于”或“小于”).發(fā)布:2025/1/6 8:0:1組卷:38引用:1難度:0.5 -
3.關于鹽的性質研究是一項重要的課題,某興趣小組以“探究碳酸氫鈉的性質”為主題開展項目式學習。
【任務一】認識碳酸氫鈉
(1)下列關于碳酸氫鈉的說法正確的是。
A.碳酸氫鈉是由Na+和構成HCO-3
B.碳酸氫鈉俗稱純堿
C.碳酸氫鈉醫(yī)療上能用于治療胃酸過多癥
D.碳酸氫鈉難溶于水
【任務二】探究碳酸氫鈉的性質
(2)探究碳酸氫鈉與稀鹽酸反應:興趣小組取適量碳酸氫鈉粉末于甲試管中,加入稀鹽酸,如圖1所示,觀察到甲試管中有氣泡產(chǎn)生,乙中,說明碳酸氫鈉能與稀鹽酸反應生成CO2,寫出試管甲中反應的化學方程式。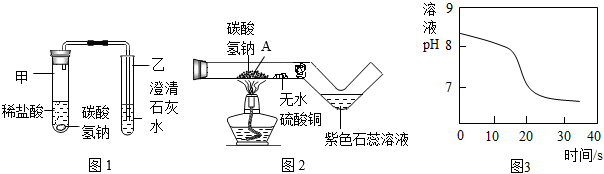
(3)探究碳酸氫鈉的熱穩(wěn)定性:用酒精燈充分加熱玻璃管,如圖2所示。
資料:無水硫酸銅呈白色,遇水后呈藍色
①發(fā)現(xiàn)玻璃管內無水硫酸銅變藍,紫色石蕊溶液變紅,說明碳酸氫鈉受熱易分解,且有和二氧化碳生成。
②實驗后興趣小組同學猜想玻璃管A處固體產(chǎn)物僅是Na2CO3而不含有NaOH,請設計實驗證明(寫出具體步驟和現(xiàn)象):。
(4)常溫下,興趣小組同學取一定量的NaHCO3溶液于燒杯中,插入pH傳感器,向燒杯中持續(xù)滴加CaCl2溶液,有白色沉淀生成,當溶液的pH變?yōu)?.68時開始有無色氣體產(chǎn)生。反應過程中溶液的pH隨時間變化如圖3所示。
【查閱資料】
材料一:NaHCO3溶于水后,少量的能同時發(fā)生如下變化:HCO-3
變化①:+H2O→H2CO3+OH-HCO-3
變化②:→HCO-3+H+CO2-3
材料二:溶液的酸堿性與溶液中H+和OH-數(shù)目的相對大小有關。常溫下,當單位體積溶液中OH-的數(shù)目大于H+的數(shù)目時溶液的pH>7,反之pH<7;單位體積溶液中所含的H+數(shù)目越大,溶液的pH越小。
①根據(jù)上述實驗可知NaHCO3溶液顯堿性,結合材料一、二從微觀角度說明原因:。
②根據(jù)本實驗,可知從0~30s,單位體積溶液中H+數(shù)目不斷(填“增大”或“減小”)。發(fā)布:2024/12/25 17:0:2組卷:94引用:2難度:0.4


