為認(rèn)識(shí)酸和堿的性質(zhì),某化學(xué)學(xué)習(xí)小組進(jìn)行了如下實(shí)驗(yàn)。
(1)20℃時(shí),配制80g溶質(zhì)質(zhì)量分?jǐn)?shù)為10%的NaOH溶液。
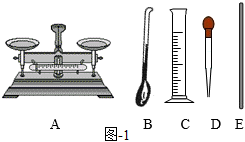
①用圖-1中儀器完成實(shí)驗(yàn),還缺少的玻璃儀器是 燒杯燒杯(填名稱),玻璃棒在配制實(shí)驗(yàn)中的作用是 攪拌,加快氫氧化鈉溶解速率攪拌,加快氫氧化鈉溶解速率。
②配制該溶液需要 7272g水。用量筒量取水時(shí),俯視讀數(shù)會(huì)導(dǎo)致所配溶液的溶質(zhì)質(zhì)量分?jǐn)?shù) 大于大于10%(填“大于”或“小于”)。
(2)向1~5號(hào)小試管中分別滴加少量稀鹽酸。
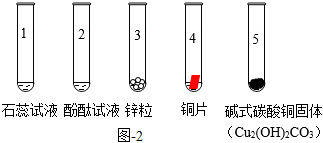
①試管1試管1中溶液變?yōu)榧t色(填“試管1”或“試管2”)。
②試管3中產(chǎn)生氣泡,試管4中無明顯現(xiàn)象,由此推斷金屬活動(dòng)性Cu比Zn 弱弱(填“強(qiáng)”或“弱”)。
③試管5中生成一種鹽和兩種氧化物,該反應(yīng)的化學(xué)方程式為 Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑。
(3)借助傳感器對(duì)稀NaOH溶液與稀鹽酸的中和反應(yīng)進(jìn)行研究,實(shí)驗(yàn)裝置如圖-3,三頸燒瓶中盛放溶液X,用恒壓漏斗勻速滴加另一種溶液。
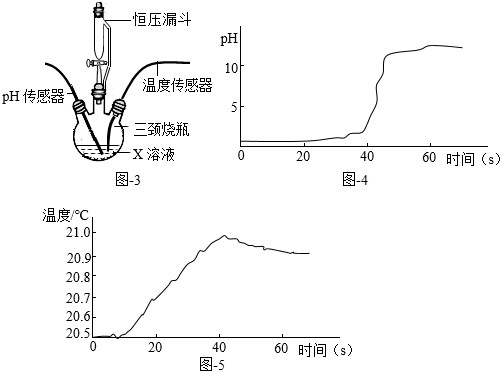
①甲同學(xué)用pH傳感器測(cè)得三頸燒瓶內(nèi)溶液pH的變化如圖-4,判斷溶液X是 稀鹽酸稀鹽酸,實(shí)驗(yàn)進(jìn)行到60s時(shí)溶液中的溶質(zhì)為 NaOH、NaClNaOH、NaCl(填化學(xué)式)。
②乙同學(xué)用溫度傳感器測(cè)得三頸燒瓶內(nèi)溫度變化如圖-5(實(shí)驗(yàn)過程中熱量散失忽略不計(jì)),據(jù)此可得出反應(yīng)過程中 釋放釋放能量的結(jié)論(填“吸收”或“釋放”)。
③丙同學(xué)提出,通過監(jiān)測(cè)三頸燒瓶內(nèi)壓強(qiáng)變化,也可以推導(dǎo)出乙同學(xué)的實(shí)驗(yàn)結(jié)論,其理由是 隨反應(yīng)的進(jìn)行,壓強(qiáng)增加隨反應(yīng)的進(jìn)行,壓強(qiáng)增加。
【考點(diǎn)】中和反應(yīng)相關(guān)實(shí)驗(yàn)與計(jì)算;酸的化學(xué)性質(zhì);溶液的酸堿性與pH的關(guān)系;固體配制一定質(zhì)量分?jǐn)?shù)溶液.
【答案】燒杯;攪拌,加快氫氧化鈉溶解速率;72;大于;試管1;弱;Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑;稀鹽酸;NaOH、NaCl;釋放;隨反應(yīng)的進(jìn)行,壓強(qiáng)增加
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/7/31 8:0:9組卷:643引用:5難度:0.4
相關(guān)試卷


