在10L的密閉容器中,進行如下化學反應:CO2(g)+H2(g)?CO(g)+H2O(g)
其化學平衡常數K與溫度t的關系如下表:
| t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)該反應為
吸熱
吸熱
(填“吸熱”或“放熱”)反應。(2)該反應的化學平衡常數表達式為K=
c
(
CO
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
(
H
2
)
c
(
CO
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
(
H
2
)
不變
不變
。(填“增大”、“減小”或“不變”)(3)下列措施可以提高H2的轉化率的是(填選項序號)
cd
cd
。a.選擇適當的催化劑
b.增大壓強
c.及時分離H2O(g)
d.升高溫度
(4)某溫度下,c(CO2)=2mol/L,c(H2)=3mol/L,開始反應,達到平衡時CO2轉化率為60%,則平衡常數K=
1
1
。(5)與(4)相同的溫度下,某時刻測得c(CO2)=0.5mol/L,c(H2)=1.5mol/L,c(CO)=0.5mol/L、c(H2O)=0.5mol/L,則此時反應是否達到平衡狀態
否
否
(填“是”或“否”)。此時,v(正) >
>
v(逆)(填“>”、“<”或“=”)。(6)該反應的反應速率 (v) 隨時間 (t) 變化的關系如圖所示,若t2、t4時刻只改變一個條件,下列說法正確的是(填選項序號)
bd
bd
。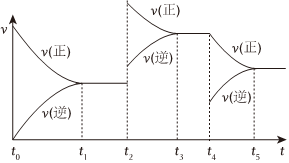
a.在t1-t2時,可依據容器內氣體的壓強保持不變判斷反應已達到平衡狀態
b.在t2時,采取的措施可以是升高溫度
c.在t4時,采取的措施可以是增加CO2的濃度。
d.在t5時,容器內CO的體積分數是整個過程中的最大值
【答案】吸熱;;不變;cd;1;否;>;bd
c
(
CO
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
(
H
2
)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:162引用:4難度:0.6
相似題
-
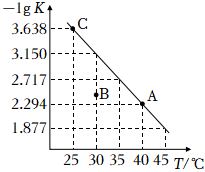 1.將一定量純凈的氨基甲酸銨固體置于密閉容器中,發生反應:NH2COONH4(s)?2NH3(g)+CO2(g)。該反應的平衡常數的負對數(-lgK)隨溫度(T)的變化如圖所示,下列說法不正確的是( )
1.將一定量純凈的氨基甲酸銨固體置于密閉容器中,發生反應:NH2COONH4(s)?2NH3(g)+CO2(g)。該反應的平衡常數的負對數(-lgK)隨溫度(T)的變化如圖所示,下列說法不正確的是( )A.該反應的ΔH>0 B.A點對應狀態的平衡常數K(A)的值為10-2.294 C.混合氣體的平均摩爾質量不變時,可以判斷該反應已達到平衡狀態 D.30℃時,B點對應狀態的v(正)<v(逆) 發布:2024/12/19 1:30:1組卷:134引用:4難度:0.7 -
2.Ⅰ.某溫度下,在一個容積可變的密閉容器中,反應2A(g)+B(g)?2C(g)達到平衡時,A、B、C的物質的量分別為4mol、2mol和4mol,此時容器容積為4L.則此溫度下該反應的平衡常數K=
.保持溫度和壓強不變,將各組分的物質的量都減少1mol,此時,容器的容積為,該反應的濃度商Q=.此時,平衡移動(填“向左”、“向右”或“不”)
Ⅱ.2007年度中國國家科學技術最高獎授予了石油化工催化專家閔恩澤,以表彰他在催化劑研究方面作出的突出貢獻.氯化汞(HgCl2)和氯化鋁(AlCl3)都有有機化工生產中常用的催化劑.
(1)氯化汞是一種能溶于水的白色固體,熔點276℃,是一種弱電解質,在水溶液中分步電離,寫出其第一步電離的方程式.
氯化汞可以被氯化亞鐵在溶液中還原為氯化亞汞(Hg2Cl2,白色沉淀),寫出該反應的離子方程式
若該反應是一個可逆反應,寫出在常溫下該反應的平衡常數表達式.
(2)無水氯化鋁用作石油裂解及催化重整的催化劑.能否直接加熱蒸干氯化鋁水溶液獲得無水氯化鋁?為什么?(用簡要的文字敘述和必要的化學方程式說明).發布:2024/11/18 8:0:1組卷:10引用:1難度:0.3 -
3.已知:NO和O2轉化為NO2的反應機理如下:
①2NO(g)?N2O2(g)(快) ΔH1<0 平衡常數K1
②N2O2(g)+O2(g)?2NO2(g)(僈) ΔH2<0 平衡常數K2
下列說法正確的是( )A.2NO(g)+O2(g)?2NO2(g)的ΔH=-(ΔH1+ΔH2) B.②的速率大小決定2NO(g)+O2(g)?2NO2(g)的反應速率 C. 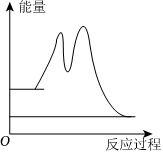
反應過程中的能量變化可用圖表示D.2NO(g)+O2(g)?2NO2(g)的平衡常數K= K1K2發布:2024/10/31 4:30:1組卷:55引用:3難度:0.8


