小明同學在家里的藥箱中發現一瓶用來清洗傷口用的消毒液--“雙氧水”,他聯想到在化學課上曾用過氧化氫溶液制取過氧氣,他高興的將家中的“雙氧水”拿到學校的實驗室,在老師的指導下和同學們一起做了如下實驗。
【第一組實驗】小明欲證明該雙氧水是否失效。
實驗過程
①在試管中加入5mL“雙氧水”,把帶火星的木條伸入試管中,發現木條未復燃;
②用酒精燈給上述試管加熱,液體中有氣泡產生,把帶火星的木條伸入試管中,發現木條仍未復燃;
③如圖1裝置進行操作,帶火星的木條復燃,

(1)水槽中冰水所起的作用是 使水蒸氣冷凝成水,以防干擾實驗使水蒸氣冷凝成水,以防干擾實驗;
(2)實驗結論:雙氧水沒有失效雙氧水沒有失效。
【第二組實驗】小明想探究CuO能否起到類似MnO2的催化作用。
(3)【猜想】ⅠCuO不是催化劑,也不參與反應,反應前后質量和化學性質不變;
ⅡCuO參與反應產生O2,反應前后質量和化學性質發生了改變;
ⅢCuO是反應的催化劑,反應前后 質量和化學性質不變質量和化學性質不變。
【實驗】用天平稱量0.2gCuO,取5ml 5%過氧化氫溶液于試管中,進行實驗(如圖2):
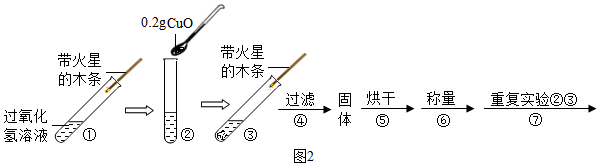
(4)填表:
| 步驟③現象 | 步驟⑥結果 | 步驟⑦現象 | 結論 |
|
劇烈反應,產生大量氣泡 劇烈反應,產生大量氣泡 ;帶火星木條復燃 |
仍為0.2g(或質量不變) 仍為0.2g(或質量不變)
|
溶液中有氣泡產生; 帶火星木條復燃 帶火星木條復燃 |
猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
做對照(或對比或比較)
做對照(或對比或比較)
。(6)利用該方法獲得氧氣的符號表達式為
H2O2H2O+O2
C
u
O
H2O2H2O+O2
C
u
O
(7)步驟④得到的固體是CuO.CuO的相對分子質量是
80
80
,其中銅元素的質量分數是 80%
80%
。【答案】使水蒸氣冷凝成水,以防干擾實驗;雙氧水沒有失效;質量和化學性質不變;劇烈反應,產生大量氣泡;仍為0.2g(或質量不變);帶火星木條復燃;做對照(或對比或比較);H2O2H2O+O2;80;80%
C
u
O
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:63引用:3難度:0.1
相似題
-
1.實驗室有一瓶配制數天的Na2SO3溶液,現在對其成分進行檢測:
【成分猜想】猜想一:只有Na2SO3;
猜想二:;
猜想三:既有Na2SO3,也有Na2SO4。
【查閱資料】①Na2SO3易被空氣中的氧氣氧化生成Na2SO4.②BaSO4
不溶于稀鹽酸和稀硫酸。③Na2SO3和鹽酸、硫酸反應均生成SO2。
【方案設計】
【方案分析】方案 實驗操作 實驗現象 結論 一 
①加入足量的稀鹽酸
②再加入足量的BaCl2溶液
猜想三正確 二
①加入足 量的稀硫酸
量的稀硫酸
②再加入足量的BaCl2溶液有氣體和白色沉淀生成 猜想一或猜想三正確
(1)方案一中的實驗現象為;方案一中加入BaCl2溶液后發生反應的化學方程式為。
(2)方案二的設計是否合理:(填“合理”或“不合理”);若不合理。理由是。
【實驗結論】通過分析比較,方案設計(填“—”或“二”)合理。發布:2024/12/24 10:0:46組卷:350引用:3難度:0.5 -
2.小強在實驗室里做實驗時,拿出一瓶久置的氫氧化鈣粉末,進行如下實驗:
(1)取氫氧化鈣粉末溶于足量水中,有現象出現,小強判斷該藥品已變質。并寫出氫氧化鈣變質的反應方程式。
(2)小強進一步做如下實驗探究,請你參與并完成表:實驗操作步驟 實驗現象 實驗結論 取樣、加適量的水,攪拌,過濾。 ①取少量濾渣于試管中,加入少量的 。粉末變質。 ②取少量濾液于試管中,滴入少量的 溶液。氫氧化鈣粉末部分變質。 發布:2024/11/27 8:0:1組卷:108引用:1難度:0.5 -
3.氫氧化鈉變質的實驗探究:
I:向鈉離子質量分數均為2%的氯化鈉溶液、氫氧化鈉溶液、碳酸鈉溶液中滴加酚酞,氯化鈉溶液不變紅,氫氧化鈉溶液、碳酸鈉溶液變紅。
Ⅱ:一位實驗員在實驗室剛配制一定質量分數的氫氧化鈉溶液后,突然接到緊急任務離開,幾天后回到實驗室才發現沒有蓋上瓶塞。
(1)你認為能使酚酞變紅的微粒為。
A.Na+
B.OH-
C.或由CO2-3引發生成的OH-。CO2-3
(2)氫氧化鈉變質為碳酸鈉,反應的化學方程式為。溶液中的離子數量如何變化?。(填:不變、減少、增大)
(3)欲證明有氫氧化鈉變質為碳酸鈉,同學甲認為可選擇試劑a:稀鹽酸,同學乙認為可選擇試劑b;氯化鋇溶液,你的觀點是。(單項選擇題)
A.過量稀鹽酸
B.過量氯化鋇溶液
C.過量稀鹽酸和氯化鋇溶液均可以
D.過量稀鹽酸和氯化鋇溶液均不可以
(4)同學丙認為氫氧化鈉只有一部分變質為碳酸鈉,溶液中仍然含有氫氧化鈉,他通過設計以下實驗證明其結論是正確的。
第一步:取少量待測液,向其中加入過量的溶液,過濾;
第二步:向以上濾液中加入,出現的現象,則丙同學觀點正確。
(5)100g質量分數為A%的氫氧化鈉溶液有部分變質后,同學丁認為仍然可以通過設計實驗方案計算出A的數值,其具體的實驗方案如下:向變質后的溶液中加入過量的稀鹽酸,蒸發結晶,洗滌,干燥,得到5.85g固體,從而可以計算出A的數值。你認為是否可以?(填“可以”或“不可以”)。若不可以,請簡述理由,若可以,則寫出A的數值。發布:2024/12/25 15:0:2組卷:166引用:3難度:0.5


