研究氮的循環和轉化對生產、生活有重要的價值。
Ⅰ.利用石灰乳和硝酸工業的尾氣(含NO、NO2)反應,既能凈化尾氣,又能獲得應用廣泛的Ca(NO2)2,其部分工藝流程如圖1所示:
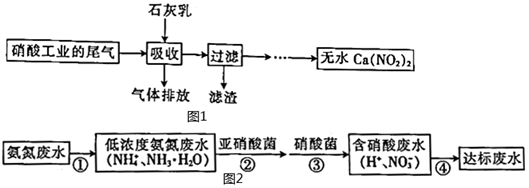
(1)流程中“濾渣”可循環使用,“濾渣”的主要成分是 Ca(OH)2Ca(OH)2(填化學式)。已知0℃時Ca(NO2)2在水中的溶解度仍然很大,實驗室從Ca(NO2)2溶液得到Ca(NO2)2晶體的操作是 蒸發結晶蒸發結晶。
(2)生產中溶液需保持弱堿性。酸性條件下,Ca(NO2)2溶液會發生反應生成Ca(NO3)2、NO和H2O,該反應的離子方程式為 2H++3NO-2=NO-3+2NO↑+H2O2H++3NO-2=NO-3+2NO↑+H2O。
Ⅱ.工業上也可用Na2CO3溶液吸收處理氮的氧化物尾氣(NOx)。一定比例的NO和NO2的混合氣體被Na2CO3溶液吸收只生成一種含氧酸鹽和一種無色無味的氣體。
(3)寫出上述反應的離子方程式:CO2-3+NO+NO2=2NO-2+CO2CO2-3+NO+NO2=2NO-2+CO2。
Ⅲ.氨氮廢水的排放會加速藻類和其他浮游生物的大量繁殖,使水質惡化。利用微生物對氨氮廢水進行處理的流程如圖2。
(4)檢驗某溶液中是否含有NH+4的方法是 取少量待測液于試管中,加入NaOH濃溶液并加熱,若產生使濕潤的紅色石蕊試紙變藍的氣體(或將蘸有濃鹽酸的玻璃棒靠近試管口,有白煙產生),則證明待測液中含有NH+4取少量待測液于試管中,加入NaOH濃溶液并加熱,若產生使濕潤的紅色石蕊試紙變藍的氣體(或將蘸有濃鹽酸的玻璃棒靠近試管口,有白煙產生),則證明待測液中含有NH+4(寫出所需試劑、操作及現象)。
(5)過程②在空氣中進行,在亞硝酸菌的作用下,NH+4轉化為HNO2,寫出該轉化的離子方程式:NH+4+3O2=2HNO2+2H2O+2H+NH+4+3O2=2HNO2+2H2O+2H+。
(6)根據圖3和圖4,判斷使用亞硝酸菌的最佳條件為 pH=8、溫度為32℃時pH=8、溫度為32℃時。
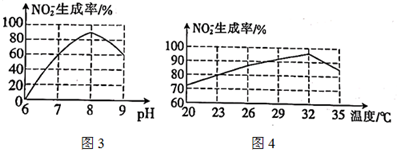
(7)過程②、③:在微生物亞硝酸菌和硝酸菌作用下實現NH+4→NO-2→NO-3的轉化,該過程稱為硝化反應。1molNH+4可被 44.844.8L(標準狀況)O2最終氧化成NO-3。
(8)利用微生物處理氨氮廢水的優點為 反應條件溫和,過程中使用的物質無毒無害,最終產物無污染反應條件溫和,過程中使用的物質無毒無害,最終產物無污染。
NO
-
2
NO
-
3
NO
-
2
NO
-
3
CO
2
-
3
NO
-
2
CO
2
-
3
NO
-
2
NH
+
4
NH
+
4
NH
+
4
NH
+
4
NH
+
4
NH
+
4
NH
+
4
NO
-
2
NO
-
3
mol
NH
+
4
NO
-
3
【答案】Ca(OH)2;蒸發結晶;2H++3=+2NO↑+H2O;+NO+NO2=2+CO2;取少量待測液于試管中,加入NaOH濃溶液并加熱,若產生使濕潤的紅色石蕊試紙變藍的氣體(或將蘸有濃鹽酸的玻璃棒靠近試管口,有白煙產生),則證明待測液中含有;+3O2=2HNO2+2H2O+2H+;pH=8、溫度為32℃時;44.8;反應條件溫和,過程中使用的物質無毒無害,最終產物無污染
NO
-
2
NO
-
3
CO
2
-
3
NO
-
2
NH
+
4
NH
+
4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:20引用:1難度:0.5
相似題
-
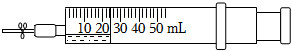 1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
(1)根據操作步驟,完成表格:
(2)如果要將注射器中的NO充分轉化,可以采取什么措施?操作步驟河 實驗現象 解釋原因 Ⅰ.振蕩注射器,觀察現象 無明顯現象 ① Ⅱ.打開彈簧夾,快速吸入10mL空氣后夾上彈簧夾,觀察現象 ② ③ Ⅲ.振蕩注射器,再觀察現象 氣體又變為無色,注射器的活塞向內移動 ④ 。
(3)上述實驗對工業上生產硝酸有什么啟示?。發布:2024/12/30 6:30:2組卷:9引用:3難度:0.6 -
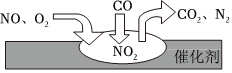 2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )
2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )A.該轉化過程中N元素化合價降低,C元素化合價升高,共兩種元素化合價發生變化 B.汽車尾氣的主要污染成分包括CO、NO和N2 C.NO和O2必須在催化劑表面才能反應 D.催化轉化的總化學方程式為2NO+O2+4CO 4CO2+N2催化劑發布:2024/12/30 6:30:2組卷:9引用:2難度:0.6 -
3.下列有關NO2的敘述正確的是( )
A.閃電時,空氣中的N2和O2可直接化合生成NO2 B.NO2與水反應時,NO2作還原劑,水作氧化劑 C.NO2、NO都是大氣污染氣體,在空氣中都能穩定存在 D.NO2是紅棕色有毒氣體 發布:2024/12/30 6:30:2組卷:7引用:2難度:0.7


