鐵及其化合物在日常生活、生產(chǎn)中應用廣泛.
(1)高鐵酸鈉(Na2FeO4)是水處理過程中的一種新型凈水劑,工業(yè)上利用NaClO 和NaOH的混合溶液將2Fe(OH)3氧化性制備高鐵酸鈉,反應的化學方程式為2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;高鐵酸鈉能用作新型凈水劑的原理是本身具有強氧化性可殺菌消毒,在反應中被還原成三價鐵離子水解生成氫氧化鐵膠體凈水本身具有強氧化性可殺菌消毒,在反應中被還原成三價鐵離子水解生成氫氧化鐵膠體凈水;
(2)氧化鐵紅顏料跟某些油料混合,可以制成防銹油漆.以黃鐵礦為原料制硫酸產(chǎn)生的硫酸渣中含F(xiàn)e2O3、SiO2、Al2O3、MgO等,用硫酸渣制備鐵紅(Fe2O3)的過程如下:
①酸溶過程中發(fā)生反應的化學方程式為Fe2O3+3H2SO4═Fe2(SO4)3+3H2OFe2O3+3H2SO4═Fe2(SO4)3+3H2O,
Al2O3+3H2SO4═Al2(SO4)3+3H2OAl2O3+3H2SO4═Al2(SO4)3+3H2O,MgO+H2SO4═MgSO4+H2OMgO+H2SO4═MgSO4+H2O;“濾渣A”主要成分的化學式為SiO2SiO2.
②還原過程中加入FeS2的目的是將溶液中的Fe3+還原為Fe2+,而本身被氧化為H2SO4,請寫出該反應的離子方程式FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+;
③氧化過程中,O2、NaOH與Fe2+反應的離子方程式為4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④為了確保鐵紅的質量和純度,氧化過程需要調節(jié)溶液的pH的范圍是3.2~3.83.2~3.8,
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 開始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
Al3+、Mg2+形成沉淀,使制得的鐵紅不純
Al3+、Mg2+形成沉淀,使制得的鐵紅不純
.【答案】2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;本身具有強氧化性可殺菌消毒,在反應中被還原成三價鐵離子水解生成氫氧化鐵膠體凈水;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Al2O3+3H2SO4═Al2(SO4)3+3H2O;MgO+H2SO4═MgSO4+H2O;SiO2;FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+;4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓;3.2~3.8;Al3+、Mg2+形成沉淀,使制得的鐵紅不純
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:33引用:5難度:0.5
相似題
-
1.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
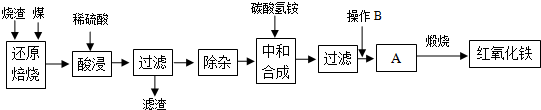
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗
Fe3+已經(jīng)除盡的試劑是.
(4)“中和合成”的目的是將溶液中Fe2+轉變?yōu)樘妓醽嗚F沉淀,則操作B是.
(5)煅燒A的反應方程式是.
(6)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標準規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數(shù)應不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:5引用:1難度:0.5 -
2.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如圖:
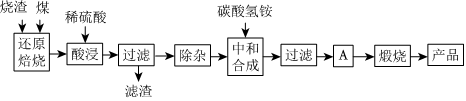
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,檢驗Fe3+已經(jīng)除盡的試劑是;當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變?yōu)樘妓醽嗚F沉淀,則A的操作是.
(5)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標準規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數(shù)應不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:114引用:4難度:0.5 -
3.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
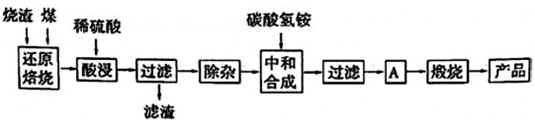
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常溫下,當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變?yōu)樘妓醽嗚F沉淀,則A的操作是.發(fā)布:2025/1/19 8:0:1組卷:12引用:1難度:0.5


