六十九中學化學興趣小組的同學們在上制取氧氣的實驗課時發現一瓶標簽殘缺的無色液體(如圖)(溫馨提示:標簽上的5%表示該混合物中主要成分所占的質量分數)。他們對此瓶無色液體是什么產生了興趣,于是進行了如下探究。

【提出問題】這瓶無色液體是什么?
【猜想與假設】小龍同學猜想這瓶液體是:水
小哈同學猜想這瓶液體是:過氧化氫溶液
(1)小組同學對標簽又進行了仔細的觀察、分析,他們一致認為 小龍小龍同學猜想不合理。理由是 水為純凈物,不會有質量分數水為純凈物,不會有質量分數。
【設計實驗】同學們結合所學知識設計出如下探究方案:
(2)向盛有少量二氧化錳的試管中加入適量的該液體,并將帶火星的木條放在試管口,觀察到 溶液中產生大量氣泡,帶火星的木條復燃溶液中產生大量氣泡,帶火星的木條復燃,得出小哈同學的猜想正確,此反應的符號表達式為 H2O2MnO2H2O+O2H2O2MnO2H2O+O2。

【查閱資料】
1.氧化銅也可以作為過氧化氫溶液分解的催化劑
2.過氧化氫分解能夠放出熱量
3.過濾是將不溶于水的固體和液體分離開的操作,二氧化錳不溶于水
【探究實驗】
(3)興趣小組的同學想要回收二氧化錳,用來比較氧化銅和二氧化錳對過氧化氫分解的催化效果哪一種更好,需要對試管內的固液混合物進行分離得到純凈的二氧化錳。采取的實驗操作是 過濾、洗滌、干燥過濾、洗滌、干燥。
【設計實驗】同學們用如圖所示的裝置進行了兩次實驗,在錐形瓶中分別加入等質量的氧化銅和二氧化錳,分別將3mL5%的過氧化氫溶液注入錐形瓶中,利用注射器收集氧氣,得到的相關曲線如圖所示。


(4)小龍同學通過圖像得出 二氧化錳二氧化錳催化效果好,除此還能得出:催化劑只能改變反應速率,不增加生成物的質量(合理即可)催化劑只能改變反應速率,不增加生成物的質量(合理即可)。
(5)小西同學觀察到燒杯中液面下的導管口有氣泡冒出,分析原因,是由于過氧化氫分解放出熱量,使瓶內①氣體溫度升高氣體溫度升高,②氣壓增大,大于外壓氣壓增大,大于外壓,在壓強差的作用下,瓶內氣體逸出。
M
n
O
2
M
n
O
2
【考點】缺失標簽的藥品成分的探究;催化劑的特點與催化作用.
【答案】小龍;水為純凈物,不會有質量分數;溶液中產生大量氣泡,帶火星的木條復燃;H2O2H2O+O2;過濾、洗滌、干燥;二氧化錳;催化劑只能改變反應速率,不增加生成物的質量(合理即可);氣體溫度升高;氣壓增大,大于外壓
M
n
O
2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:26引用:2難度:0.5
相似題
-
 1.某化學興趣小組的同學在整理化學藥品柜時【提出問題】這瓶無色溶液是什么物質的溶液?
1.某化學興趣小組的同學在整理化學藥品柜時【提出問題】這瓶無色溶液是什么物質的溶液?
【查閱資料】①20℃是碳酸鈉的溶解度是21.8g,碳酸氫鈉的溶解度是9.6g,硫酸鈉的溶解度19.5g,硝酸鈉的溶解度是88g。
②碳酸鋇是不溶于水的白色固體,硫酸鋇是既不溶解于水又不溶解于酸的白色固體;
③Ca(OH)2和Ba(OH)2的不同溫度下的溶解度如表所示:
【猜想與假設】小組同學提出了如下假設:溫度(℃) 10 20 30 40 50 60 Ca(OH)2 0.17g 0.16g 0.15g 0.14g 0.13g 0.12g Ba(OH)2 2.48g 3.89g 5.59g 8.22g 13.12g 20.94g
①碳酸鈉溶液;②硫酸鈉溶液;③碳酸氫鈉溶液;④硝酸鈉溶液
【討論交流】在老師的指導下,小組同學認為假設不合理,理由是。
【進行實驗】小組同學設計并進行了如下實驗,請你完善小組同學的“相互評價”。
【實驗反思】請寫出硫酸鈉和氫氧化鋇反應的化學方程式實驗組別 操作、現象與結論 結論與評價 第一組 取少量的樣品溶液于一試管中,向其中加入稀鹽酸,試管中無明顯現象。猜想②成立。 你認為此結論 (填“正確”或不正確”),理由是。第二組 取少量的樣品溶液于一試管中,向其中加入氫氧化鋇溶液,試管中出現白色沉淀。猜想②成立。 此結論不正確,要想進一步確定猜想②成立,還需進行的實驗是 。。
【注意:若答對下列兩個小題獎勵4分,化學試卷總分不超過60分】
【拓展提升】長期存放的氫氧化鈉溶液會變質生成碳酸鈉,為探究氫氧化鈉變質的程度,實驗室常用先加過量的氯化鈣溶液或氯化鋇溶液充分反應后過濾,再在濾液中滴加酚酞溶液的方案進行實驗。
【實驗反思】實驗發現加氯化鋇溶液比加氯化鈣溶液實驗結果更準確,原因是。如果使用氯化鈣溶液,要達到實驗目的,你認為改進實驗的方法是。發布:2024/12/25 16:30:1組卷:91引用:2難度:0.5 -
2.倉庫中有一包氮肥的包裝標簽模糊不清,有同學進行了以下探究:
(1)操作③用玻璃棒攪拌的目的是.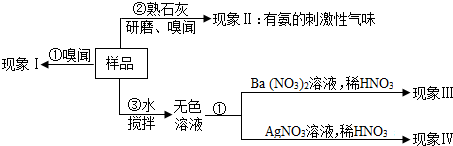
(2)請完成如表(已知AgCl和BaSO4是難溶于水和酸的白色固體):
(3)若現象Ⅲ、Ⅳ都無現象,則該氮肥可能是假設和現象 判斷和化學方程式 a 若現象I為無氨味. 則樣品中不含 (填名稱).b 由操作②現象判斷. 該樣品一定含有 離子.c 若現象Ⅲ為白色沉淀,現象Ⅳ為無沉淀. 則樣品中含有 (寫名稱),該反應的化學方程式為.d 若現象Ⅲ為“無沉淀”,現象Ⅳ為白色沉淀. 則樣品中含有 (寫化學式),該反應的化學方程式為.(寫化學式);若操作②現象為無氣味、現象Ⅲ、Ⅳ無現象,則該氮肥可能是(只寫一種).發布:2024/12/24 11:1:11組卷:356引用:5難度:0.1 -
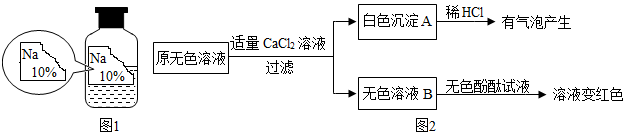
3.實驗室有一瓶標簽殘缺并且瓶蓋沒有完全密封的無色溶液(如圖1),化學小組的同學經過詢問老師后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一種溶液,為確認原瓶中是何種溶質并判斷其是否變質,化學小組的同學進行了如下的探究活動:
【進行猜想】
猜想I:原溶液的溶質是NaCl;
猜想Ⅱ:原溶液的溶質是NaOH;
猜想Ⅲ:原溶液的溶質是Na2CO3;
猜想 IV:原溶液的溶質是NaHCO3。
【查閱資料】常溫下,有關物質的相關信息如表:
從物質的相關信息可知,原溶液的溶質一定不是NaHCO3,因為物質 NaCl NaOH Na2CO3 NaHCO3 常溫下的溶解度/g 36 109 21.5 9.6 常溫下稀溶液的pH 7 13 11 9 。
【進行實驗】
(1)取少量樣品,測得溶液的pH大于7,則原溶液的溶質肯定不是。
(2)同學們另取樣品又進行了如下實驗,實驗過程如圖2:
①生成白色沉淀A的化學方程式。
②通過實驗可以判斷樣品無色溶液中含有的溶質有
【獲得結論】
實驗完成后,最終得到的結論:原瓶中的溶質是,且已變質。發布:2024/12/25 16:0:1組卷:142引用:5難度:0.5


