硫酸是重要的化工原料,某興趣小組對濃硫酸的性質(zhì)進行如下探究。
I.(1)棉布上滴濃H2SO4后破洞。體現(xiàn)了濃H2SO4的 脫水脫水 (填“脫水”“吸水”或“強氧化”、下同)性:在冷的濃H2SO4中放入鐵片無明顯現(xiàn)象,體現(xiàn)了濃H2SO4的 強氧化強氧化性。
II.為了檢驗濃硫酸與木炭在加熱條件下反應(yīng)產(chǎn)生的SO2和CO2氣體,設(shè)計了如圖所示實驗裝置,a、b、c為止水夾,B是用于儲氣的氣囊。(已知淀粉溶液遇I2變藍)
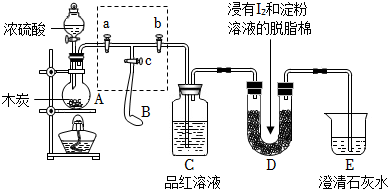
(2)裝置A中發(fā)生反應(yīng)的化學方程式為 2H2SO4(濃)+C △ 2SO2↑+CO2↑+2H2O2H2SO4(濃)+C △ 2SO2↑+CO2↑+2H2O。
(3)實驗時,裝置C中的現(xiàn)象為 酸性KMnO4溶液褪色酸性KMnO4溶液褪色。
(4)此實驗成敗的關(guān)鍵在于控制反應(yīng)產(chǎn)生氣體的速率不能過快,因此設(shè)計了虛框部分的裝置,正確的操作順序是 ③①②③①②(填序號)。
①向A裝置中加入濃硫酸,加熱,使A中產(chǎn)生的氣體進入氣囊B,當氣囊中充入一定量氣體時,停止加熱。
②待裝置A冷卻,且氣囊B的體積不再變化后,關(guān)閉止水夾a,打開止水夾b,慢慢擠壓氣囊,使氣囊B中氣體慢慢進入裝置C中,待達到實驗?zāi)康暮螅P(guān)閉止水夾b。
③打開止水夾a和c,關(guān)閉止水夾b。
(5)若要檢驗濃硫酸與木炭在加熱條件下生成的水蒸氣,可在裝置 A、B或B、C之間A、B或B、C之間 之間加上一個盛有無水CuSO4的硬質(zhì)玻璃管。
(6)當D中產(chǎn)生 進氣口一端脫脂棉藍色變淺,出氣口一端脫脂棉藍色不變進氣口一端脫脂棉藍色變淺,出氣口一端脫脂棉藍色不變現(xiàn)象時,可以說明使E中澄清石灰水變渾濁的是CO2,而不是SO2;寫出D中發(fā)生反應(yīng)的化學方程式 2H2O+SO2+I2=2HI+H2SO42H2O+SO2+I2=2HI+H2SO4。
(7)當D中反應(yīng)轉(zhuǎn)移電子0.3mol時,參加反應(yīng)的氣體體積(標準狀況下)為 3.363.36L。
△
△
【考點】濃硫酸的特性;濃硫酸的性質(zhì)實驗.
【答案】脫水;強氧化;2H2SO4(濃)+C 2SO2↑+CO2↑+2H2O;酸性KMnO4溶液褪色;③①②;A、B或B、C之間;進氣口一端脫脂棉藍色變淺,出氣口一端脫脂棉藍色不變;2H2O+SO2+I2=2HI+H2SO4;3.36
△
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:10引用:1難度:0.5
相似題
-
1.某研究小組成員在討論鑒別濃硫酸和稀硫酸的方案時,收集了如下方案:
(1)其中可行的是方案 操作 結(jié)論 甲 將火柴梗分別放入其中 變黑者為濃硫酸 乙 分別加入金屬鋁片 產(chǎn)生刺激性氣味者為濃硫酸 丙 分別加入盛水的試管中 放熱者為濃硫酸 丁 分別在CuSO4?5H2O晶體上滴加二者 變白者為濃硫酸 (填“甲”“乙”“丙”“丁”)。
(2)對其中一個操作稍做改進就能成為可行方案的是,改進方法是。
(3)請給出另外兩種鑒別方案,完成表格。方案 操作 結(jié)論 A B 發(fā)布:2024/12/30 7:0:1組卷:3引用:3難度:0.6 -
2.下列說法正確的是( )
A.工業(yè)制備硫酸流程中用水吸收三氧化硫生成煙硫酸 B.氨水可以導電,因此氨水是電解質(zhì) C.市售硝酸的質(zhì)量分數(shù)為68%~70%,常因溶有少量NO2而略顯黃色 D.常溫下可以用鐵制容器盛裝濃硫酸,原因是濃硫酸與鐵不反應(yīng) 發(fā)布:2024/12/31 8:0:1組卷:4引用:0難度:0.7 -
3.兩支試管中分別盛有濃硫酸和稀硫酸,某同學使用的下列4種方法中,能鑒別出哪支試管盛濃硫酸的方法有( )
①加入銅片(加熱);②加入鐵片;③加入膽礬; ④加入氯化鋇.A.1 種 B.2種 C.3種 D.4種 發(fā)布:2024/12/30 15:0:1組卷:9引用:2難度:0.9
相關(guān)試卷


