2021-2022學年陜西省西安市閻良區高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題共16小題,每小題3分,計48分。每小題只有一個選項是符合題意的)
-
1.化學與科技、生活緊密相關。下列說法正確的是( )
A.“溫室效應”、“光化學煙霧”的形成都與氮氧化物有關 B.SO2有毒,所以不能用作食品添加劑 C.新型冠狀病毒粒子直徑約60~220nm,介于溶液和膠體之間 D.“奮斗者號”潛水器使用的固體浮力材料由空心玻璃微球填充高強樹脂制成,屬于復合材料 組卷:20引用:2難度:0.7 -
2.向盛有FeCl3溶液的試管中滴入KSCN溶液,溶液呈( )
A.紅色 B.黃色 C.藍色 D.淺綠色 組卷:26引用:1難度:0.8 -
3.古詩詞是古人為我們留下的寶貴精神財富,下列詩句不涉及氧化還原反應的是( )
A.爐火照天地,紅星亂紫煙 B.千淘萬漉雖辛苦,吹盡狂沙始到金 C.熬膽礬鐵釜,久之亦化為銅 D.爆竹聲中一歲除,春風送暖入屠蘇 組卷:28引用:8難度:0.7 -
4.下列各組混合物中,能用分液漏斗進行分離的是( )
A.酒精和水 B.碘和四氯化碳 C.水和四氯化碳 D.汽油和植物油 組卷:364引用:89難度:0.9 -
5.下列有關試劑保存的說法中不正確的是( )
A.濃硝酸不需密封保存 B.液氯貯存在鋼瓶中 C.存放液溴的試劑瓶中應加水封 D.漂白粉要密封存放于干燥陰涼處 組卷:6引用:1難度:0.8 -
6.某溶液中含有大量的下列離子:Fe3+、SO42-、Al3+和M離子,經測定Fe3+、SO42-、Al3+和M離子的物質的量之比為2:4:1:1,則M離子可能是下列中的( )
A.Na+ B.NO3- C.Mg2+ D.OH- 組卷:80引用:11難度:0.9 -
7.配制400mL0.100mol/L的KCl溶液,下列說法正確的是( )

A.上述實驗操作步驟的正確順序為:④①②③ B.容量瓶需要用自來水、蒸餾水洗滌,干燥后才可用 C.實驗中需稱量2.98gKCl固體 D.定容時,若仰視容量瓶的刻度線,使配得的KCl溶液濃度偏低 組卷:59引用:2難度:0.7
二、非選擇題(本大題共5小題,計52分)
-
20.鐵、鋁、鈉是三種重要的金屬。回答下列問題:
I.氯化鐵溶液常用作印刷電路銅板的腐蝕劑。
(1)寫出該反應的離子方程式,從腐蝕廢液中回收金屬銅還需要的試劑是。
II.KAl(SO4)2?12H2O(明礬)是一種復鹽,在造紙等方面應用廣泛。實驗室中,采用廢易拉罐(主要成分為Al,含有少量的Fe、Mg雜質)制備明礬的過程如圖所示:
(2)試劑①應選用(填字母),反應的化學方程式為。
a HCl溶液
b.H2SO4溶液
c.氨水
d.NaOH溶液
(3)向30mL1mol/L的KAl(SO4)2溶液中逐漸加入濃度為4mol/L的NaOH溶液,若產生0.78g白色沉淀,則加入NaOH溶液的體積可能為mL或mL。
III.現有一不純的小蘇打樣品(含雜質NaCl、Na2CO3、10H2O),為測定NaHCO3的質量分數,設計如圖所示的實驗裝置(夾持儀器未畫出)。
實驗步驟如下:
①按圖組裝好實驗裝置并檢查氣密性。
②稱取定質量的樣品,并將其放入硬質玻璃管中;稱量裝濃硫酸的洗氣瓶C的質量和裝堿石灰的U形管D的質量。
③打開活塞K1、K2,關閉K3,緩緩鼓入空氣數分鐘。
④關閉活塞K1、K2打開K3,點燃酒精燈加熱至不再產生氣體。
⑤打開活塞K1,緩緩鼓入空氣數分鐘,然后拆下裝置,再次稱量洗氣瓶C和U形管D的質量。
(4)若無裝置E,則會導致測得NaHCO3的質量分數( 填“偏大”、“偏小”或“無影響”)。
(5)步驟③的目的是。
(6)若實驗中稱取樣品的質量為50.0g,反應后C、D裝置增加的質量分別為12.6g、8.8g,則混合物中NaHCO3的質量分數為。組卷:10引用:1難度:0.5 -
21.硫酸是重要的化工原料,某興趣小組對濃硫酸的性質進行如下探究。
I.(1)棉布上滴濃H2SO4后破洞。體現了濃H2SO4的(填“脫水”“吸水”或“強氧化”、下同)性:在冷的濃H2SO4中放入鐵片無明顯現象,體現了濃H2SO4的性。
II.為了檢驗濃硫酸與木炭在加熱條件下反應產生的SO2和CO2氣體,設計了如圖所示實驗裝置,a、b、c為止水夾,B是用于儲氣的氣囊。(已知淀粉溶液遇I2變藍)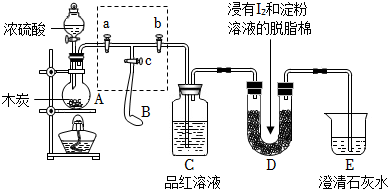
(2)裝置A中發生反應的化學方程式為。
(3)實驗時,裝置C中的現象為。
(4)此實驗成敗的關鍵在于控制反應產生氣體的速率不能過快,因此設計了虛框部分的裝置,正確的操作順序是(填序號)。
①向A裝置中加入濃硫酸,加熱,使A中產生的氣體進入氣囊B,當氣囊中充入一定量氣體時,停止加熱。
②待裝置A冷卻,且氣囊B的體積不再變化后,關閉止水夾a,打開止水夾b,慢慢擠壓氣囊,使氣囊B中氣體慢慢進入裝置C中,待達到實驗目的后,關閉止水夾b。
③打開止水夾a和c,關閉止水夾b。
(5)若要檢驗濃硫酸與木炭在加熱條件下生成的水蒸氣,可在裝置之間加上一個盛有無水CuSO4的硬質玻璃管。
(6)當D中產生現象時,可以說明使E中澄清石灰水變渾濁的是CO2,而不是SO2;寫出D中發生反應的化學方程式。
(7)當D中反應轉移電子0.3mol時,參加反應的氣體體積(標準狀況下)為L。組卷:10引用:1難度:0.5


