 某化學課外活動小組為驗證元素化學性質遞變規律,進行如下實驗探究。
某化學課外活動小組為驗證元素化學性質遞變規律,進行如下實驗探究。
Ⅰ.驗證同周期X、Y、Z三種元素金屬性遞變規律。
| 實驗操作 | 實驗現象 |
| 各取1.0g金屬X和金屬Z(形狀相同),分別加入到5mL水中 | 金屬X與水反應比金屬Z劇烈 |
| 各取1.0g金屬Z和金屬Y(形狀相同),分別加入到5mL(g)1.0mol/L鹽酸中 | 金屬Z與鹽酸反應比金屬Y劇烈 |
X>Z>Y
X>Z>Y
。下列判斷正確的是 a
a
(填字母)。a.原子序數:Y>Z>X
b.原子的最外層電子數:X>Y>Z
c.原子半徑:Y>Z>X
d.Y的最高價氧化物對應水化物的堿性最強
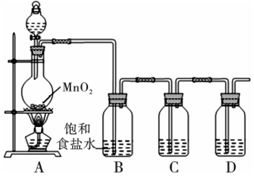
Ⅱ.驗證氯元素的非金屬性比硫元素的非金屬性強,實驗裝置如圖所示:
(1)裝置A的分液漏斗中盛裝的試劑是
濃鹽酸
濃鹽酸
,燒瓶中發生反應的化學方程式為 4HCl(濃)+MnO2 MnCl2+Cl2↑+2H2O
△
4HCl(濃)+MnO2 MnCl2+Cl2↑+2H2O
。 △
(2)裝置C中盛放的試劑是
a
a
(填字母),發生反應的離子方程式為 S2-+Cl2═2Cl-+S↓
S2-+Cl2═2Cl-+S↓
。a.Na2S溶液
b.Na2SO3溶液
c.Na2SO4溶液
(3)為防止污染空氣,裝置D中盛放的試劑可能是
氫氧化鈉溶液
氫氧化鈉溶液
。(4)下列事實不能證明氯元素的非金屬性比硫元素強的是
b
b
(填字母)。a.HCl比H2S穩定
b.稀溶液中,HClO的氧化性比H2SO4強
c.HClO4的酸性比H2SO4強
d.鐵與Cl2反應生成FeCl3,而鐵與硫反應生成FeS
(5)要驗證非金屬性:Cl>I,可在C裝置中加入淀粉-KI溶液,能夠證明氯元素的非金屬性比碘元素強的實驗現象是
淀粉-KI溶液變藍
淀粉-KI溶液變藍
。【答案】X>Z>Y;a;濃鹽酸;4HCl(濃)+MnO2 MnCl2+Cl2↑+2H2O;a;S2-+Cl2═2Cl-+S↓;氫氧化鈉溶液;b;淀粉-KI溶液變藍
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:36引用:1難度:0.5
相似題
-
1.某化學興趣小組的同學學習了同周期元素性質的遞變規律后,設計了一套實驗方案進行實驗探究,并記錄了有關實驗現象,如下表。
請你幫助該同學整理并完成實驗報告。實驗方案 實驗現象 ①用砂紙擦后的鎂帶與沸水反應,再向反應液中滴加酚酞 A.浮于水面,熔成小球,在水面上無定向移動,隨之消失,溶液變成紅色 ②向新制的H2S飽和溶液中滴加新制的氯水 B.產生大量氣體,可在空氣中燃燒,溶液變成淺紅色 ③鈉與滴有酚酞試液的冷水反應 C.反應不十分劇烈,產生的氣體可以在空氣中燃燒 ④鎂帶與2mol?L-1的鹽酸反應 D.劇烈反應,產生的氣體可以在空氣中燃燒 ⑤鋁條與2mol?L-1的鹽酸反應 E.生成白色膠狀沉淀,繼而沉淀消失 ⑥向氯化鋁溶液中滴加氫氧化鈉溶液 F.生成淡黃色沉淀
(1)實驗目的:。
(2)實驗儀器:①;②;③;④試管夾;⑤鑷子;⑥小刀;⑦玻璃片;⑧砂紙;⑨膠頭滴管等。
(3)實驗藥品:鈉、鎂帶、鋁條、2mol?L-1鹽酸、新制的氯水、硫化氫飽和溶液、氯化鋁溶液、氫氧化鈉溶液等。
(4)請你寫出上述的實驗操作對應的現象(用A~F表示):
①;②;③;④;⑤;⑥。
(5)寫出實驗操作②、⑥中有關反應的離子方程式:實驗②,實驗⑥。
(6)實驗結論:。發布:2024/6/27 10:35:59組卷:11引用:1難度:0.4 -
2.某研究性學習小組設計了一組實驗驗證元素周期律。
Ⅰ.甲同學在a、b、c、d四只燒杯中分別加入50mL冷水,再各滴加幾滴酚酞試液,依次加入大小相近的鈉(Na)、鎂(Mg)、鋁(Al)、鉀(K)金屬塊,觀察現象。
(1)反應最劇烈的燒杯中金屬是。(填字母序號)
A.鈉
B.鎂
C.鋁
D.鉀
(2)實驗中發現b、c兩只燒杯中幾乎沒有什么現象,要想達到實驗目的,請你幫助選擇下列合適的方法。(填字母序號)
A.把鎂、鋁的金屬塊換成金屬粉末
B.把燒杯中的冷水換成熱水
C.把燒杯中的冷水換成鹽酸
D.把燒杯中的冷水換成氫氧化鈉溶液
Ⅱ.乙同學設計實驗探究碳、硅元素的非金屬性的相對強弱。根據要求完成下列各題
實驗裝置:(已知酸性強弱:亞硫酸>碳酸)
(3)銅與濃硫酸反應的化學方程式是;裝置E中酸性KMnO4溶液的作用是。
(4)能說明碳元素的非金屬性比硅元素非金屬性強的實驗現象是;試管F中發生反應的離子方程式為。發布:2024/6/27 10:35:59組卷:29引用:1難度:0.6 -
3.某學生做探究同主族元素性質遞變規律的實驗時,自己設計了一套實驗方案,并記錄了有關實驗現象。請你幫助該學生整理并完成實驗報告。
(1)實驗目的:。
(2)實驗用品:
儀器:①;②(請填寫兩種主要玻璃儀器)。
藥品:氯水、溴水、溴化鈉溶液、碘化鉀溶液、四氯化碳。
(3)實驗內容(在下列空格內填寫相關內容)
(4)實驗結論:序號 實驗方案 實驗現象 ① ② 。
(5)問題和討論:
①請用物質結構理論簡單說明得出上述結論的原因:。
②由于F2過于活潑,很難設計一個簡單的實驗驗證其氧化性的強弱。試列舉一個事實說明F的非金屬性比Cl強:。發布:2024/6/27 10:35:59組卷:5引用:1難度:0.6


