某校化學學習小組設計了相關實驗來探究元素周期律。該組同學為驗證鹵素單質氧化性的相對強弱,用如圖1所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。
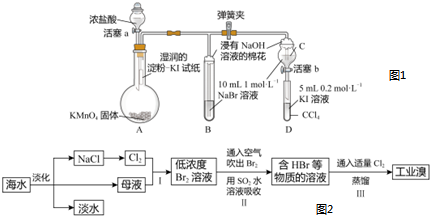
實驗過程及現象:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸;
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾;
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a;
Ⅳ.打開活塞b,將少量C中溶液滴入D中,關閉活塞b,取下D振蕩,靜置后CCl4層溶液變為紫紅色。
請回答下列問題。
(1)B中反應的離子方程式為 2Br-+Cl2=2Cl-+Br22Br-+Cl2=2Cl-+Br2。
(2)驗證氯氣的氧化性強于碘的實驗現象是 A裝置上方淀粉-KI試紙變藍A裝置上方淀粉-KI試紙變藍。
(3)B和C儀器口放置浸有NaOH溶液的棉花的作用是 吸收未反應的氯氣,防止污染空氣吸收未反應的氯氣,防止污染空氣。
(4)由此實驗得出的結論:同主族元素從上到下,單質的得電子能力逐漸 減弱減弱(填“減弱”或“增強”)。
(5)海水是巨大的資源寶庫,從海水中提取食鹽和溴的過程如圖2所示;下列描述錯誤的是 CC。
A.淡化海水水的方法主要有蒸餾法、電滲析法、離子交換法
B.以NaCl為原料可以生產燒堿、純堿、金屬鈉、氯氣、鹽酸等化工產品
C.步驟Ⅱ中鼓入熱空氣吹出溴,是因為溴蒸氣的密度比空氣的密度小
D.用SO2水溶液吸吸收Br2的離子反應方程式為Br2+SO2+2H2O═4H++SO2-4+2Br-
SO
2
-
4
【考點】探究鹵素單質間的置換反應;海水淡化.
【答案】2Br-+Cl2=2Cl-+Br2;A裝置上方淀粉-KI試紙變藍;吸收未反應的氯氣,防止污染空氣;減弱;C
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:13引用:1難度:0.7
相似題
-
1.為驗證鹵素單質氧化性的相對強弱,某小組用如圖所示裝置進行實驗(夾持儀器和加熱裝置已略去,氣密性已檢驗)。
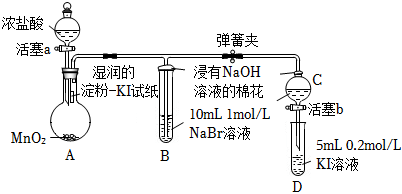
實驗過程:
I.打開彈簧夾,打開活塞a,滴加濃鹽酸。
II.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
III.當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.…
(1)A中利用濃鹽酸和MnO2固體的反應制備氯氣,反應的離子方程式是。
(2)驗證氯氣的氧化性強于碘的實驗現象是。
(3)B中溶液發生反應的離子方程式是。
(4)為驗證溴的氧化性強于碘,過程Ⅳ的操作和現象是。
(5)過程Ⅲ實驗的目的是。
(6)從原子結構角度分析氯、溴、碘單質的氧化性逐漸減弱的原因:。發布:2024/6/27 10:35:59組卷:42引用:1難度:0.7 -
2.為了驗證鹵素單質氧化性的相對強弱,某小組用如圖所示裝置進行實驗。(夾持儀器已略去,氣密性已檢驗)

實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a
Ⅳ.…
(1)A中反應的化學方程式為:KMnO4+HCl(濃)═KCl+MnCl2+Cl2↑+H2O,則氧化性KMnO4Cl2。(填“>”、“<”或“=”)
(2)驗證氯氣的氧化性強于碘的實驗現象是。
(3)過程Ⅲ的實驗目的是。
(4)為驗證溴的氧化性強于碘,過程Ⅳ的操作和現象是。
(5)浸有NaOH溶液的棉花團的作用是。此處發生的化學方程式是。
(6)氰(CN)2、硫氰(SCN)2的化學性質和鹵素很相似,化學上稱為“類鹵素”,它們陰離子的還原性強弱為:Cl-<Br-<CN-<SCN-<I-。試寫出:
a.(CN)2與KOH反應的化學方程式。
b.在NaBr和KSCN的混合溶液中加入(CN)2的離子方程式。發布:2024/7/18 8:0:9組卷:97引用:3難度:0.5 -
3.某小組同學用如圖所示裝置驗證鹵素單質氧化性的相對強弱。請回答:
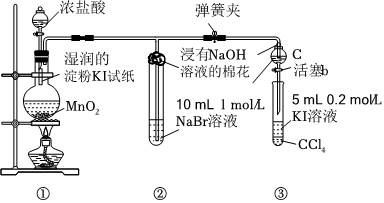
(1)①中產生的是黃綠色氣體,其電子式是,在該反應中濃鹽酸表現了性和性。
(2)反應一段時間后,①中濕潤的淀粉碘化鉀試紙可觀察到的現象是。
(3)B中試管口處浸有NaOH溶液的棉花的作用是。
(4)由②、③中的現象說明鹵素單質的氧化性由強到弱的順序是。
(5)實驗室中所用少量氯氣也可用下列方法制取:K2Cr2O7+14HCl(濃)=2KCl+2CrCl3+3Cl2↑+7H2O,該氧化劑與還原劑的比為;該反應中每有73gHCl被氧化,生成標況下Cl2的體積為L。發布:2024/6/27 10:35:59組卷:87引用:1難度:0.7


