當(dāng)前位置:
2006年第十六屆“天原杯”全國(guó)初中學(xué)生化學(xué)素質(zhì)和實(shí)驗(yàn)?zāi)芰Ω?jìng)賽(江蘇賽區(qū))初賽試卷>
試題詳情
復(fù)分解反應(yīng)是我們學(xué)過(guò)的化學(xué)基本反應(yīng)類(lèi)型之一。學(xué)習(xí)時(shí),應(yīng)注意將知識(shí)進(jìn)行歸納、總結(jié),深刻理解復(fù)分解反應(yīng)發(fā)生的條件,形成完整的知識(shí)體系。(已知BaSO4難溶于水)
(1)寫(xiě)出下列反應(yīng)的化學(xué)方程式:
①氯化鋇溶液與硫酸鈉混合:BaCl2+Na2SO4=BaSO4↓+2NaClBaCl2+Na2SO4=BaSO4↓+2NaCl:
②碳酸鉀溶液與稀鹽酸混合:K2CO3+2HCl=2KCl+CO2↑+H2OK2CO3+2HCl=2KCl+CO2↑+H2O;
③氫氧化鋇溶液與稀硝酸混合:Ba(OH)2+2HNO3=Ba(NO3)2+2H2OBa(OH)2+2HNO3=Ba(NO3)2+2H2O。
(2)你想過(guò)上述復(fù)分解反應(yīng)為什么能夠發(fā)生嗎?這是因?yàn)樵谶@些反應(yīng)物中含有一些“特殊”的陰、陽(yáng)離子,它們能相互結(jié)合。如上述反應(yīng)①中,實(shí)際參加反應(yīng)的離子是Ba2+和SO42-,而Cl-、Na+則是“旁觀者”,并沒(méi)有參加反應(yīng)。請(qǐng)你分析上述反應(yīng)②中實(shí)際參加反應(yīng)的離子是CO32-、H+CO32-、H+;上述反應(yīng)③中實(shí)際參加反應(yīng)的離子是H+、OH-H+、OH-。
(3)請(qǐng)根據(jù)你的想象,在如圖空白的容器中畫(huà)出體現(xiàn)NaOH溶液和稀鹽酸反應(yīng)產(chǎn)物的示意圖。
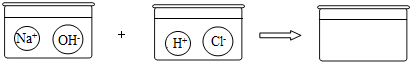
【考點(diǎn)】復(fù)分解反應(yīng)的實(shí)質(zhì)與應(yīng)用;書(shū)寫(xiě)化學(xué)方程式、文字表達(dá)式、電離方程式;微粒觀點(diǎn)及模型圖的應(yīng)用.
【答案】BaCl2+Na2SO4=BaSO4↓+2NaCl;K2CO3+2HCl=2KCl+CO2↑+H2O;Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;CO32-、H+;H+、OH-
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:207引用:32難度:0.7
相似題
-
1.下列各組溶液,相互能發(fā)生反應(yīng)的是( )
A.碳酸鉀和硝酸鋇 B.硝酸鋇和鹽酸 C.氫氧化鈉和碳酸鉀 D.硫酸鈉和碳酸鉀 發(fā)布:2024/12/25 16:0:1組卷:119引用:7難度:0.9 -
2.在宏觀、微觀和符號(hào)之間建立聯(lián)系是化學(xué)學(xué)科的重要思維方式。
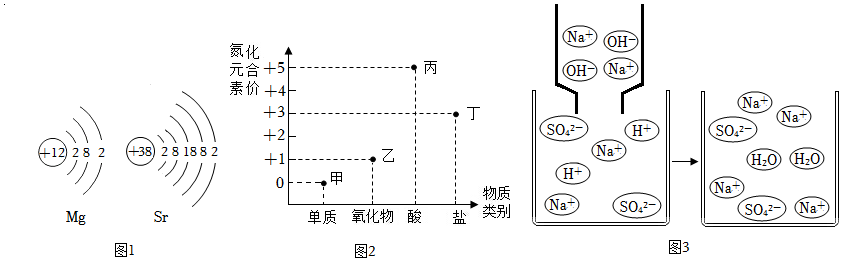
(1)如圖1是鎂原子和鍶原子結(jié)構(gòu)示意圖。
①鎂和鍶兩種元素的最本質(zhì)區(qū)別是。
②鍶與地殼中含量最多的元素形成的化合物為(填化學(xué)式)。
③元素的性質(zhì)與其原子結(jié)構(gòu)有密切關(guān)系。原子的最外層電子數(shù)相同時(shí),電子層數(shù)越多,最外層電子離核越遠(yuǎn),原子核對(duì)最外層電子的吸引力越小。由此推測(cè),鍶(Sr)的金屬的活動(dòng)性比鎂(Mg)的金屬活動(dòng)性(填“強(qiáng)”或“弱”)。
(2)氮及其化合物的“化合價(jià)-物質(zhì)類(lèi)別”關(guān)系圖如圖2。
①甲在空氣中的體積分?jǐn)?shù)為;丙的化學(xué)式為HNO3,該物質(zhì)的名稱(chēng)是。
②若丁是工業(yè)用鹽NaNO2,能區(qū)別NaNO2溶液與食鹽溶液的一種試劑是。(友情提示:NaNO2有毒,有咸味,外形與食鹽相似,其水溶液呈堿性,AgNO2微溶于水。)
(3)圖3描述了NaOH與NaHSO4兩溶液反應(yīng)的微觀示意圖。
①NaHSO4物質(zhì)類(lèi)別屬于(填“酸”、“堿”或“鹽”)。
②寫(xiě)出與該反應(yīng)微觀本質(zhì)相同的另一化學(xué)方程式。發(fā)布:2024/12/24 9:0:1組卷:124引用:2難度:0.7 -
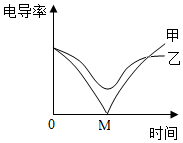 3.電導(dǎo)率傳感器可輔助探究復(fù)分解反應(yīng)的實(shí)質(zhì),相同條件下,離子濃度越大,電導(dǎo)率越大,溶液導(dǎo)電性越強(qiáng).將含有酚酞的Ba(OH)2溶液平均分成兩份置于兩個(gè)燒杯中并插入電導(dǎo)率傳感器,往其中一份滴加稀硫酸,往另一份滴加硫酸鈉溶液,測(cè)得溶液的電導(dǎo)率變化如圖所示.下列說(shuō)法正確的是( )
3.電導(dǎo)率傳感器可輔助探究復(fù)分解反應(yīng)的實(shí)質(zhì),相同條件下,離子濃度越大,電導(dǎo)率越大,溶液導(dǎo)電性越強(qiáng).將含有酚酞的Ba(OH)2溶液平均分成兩份置于兩個(gè)燒杯中并插入電導(dǎo)率傳感器,往其中一份滴加稀硫酸,往另一份滴加硫酸鈉溶液,測(cè)得溶液的電導(dǎo)率變化如圖所示.下列說(shuō)法正確的是( )A.甲曲線對(duì)應(yīng)的是氫氧化鋇與硫酸鈉反應(yīng) B.甲曲線上的M點(diǎn)代表兩種溶液恰好完全反應(yīng) C.乙曲線電導(dǎo)率減小過(guò)程中,溶液由紅色變?yōu)闊o(wú)色 D.乙曲線對(duì)應(yīng)的反應(yīng)中四種離子數(shù)目都減少 發(fā)布:2024/12/25 11:0:2組卷:174引用:4難度:0.5


