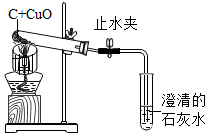
 木炭作為還原劑用于金屬冶煉已有幾千年歷史。科學興趣小組按下列裝置進行木炭與氧化銅反應實驗時,發現很難觀察到紫紅色銅的生成。為觀察到有紫紅色銅的生成,興趣小組同學采取了以下的方法,對實驗進行了改進。
木炭作為還原劑用于金屬冶煉已有幾千年歷史。科學興趣小組按下列裝置進行木炭與氧化銅反應實驗時,發現很難觀察到紫紅色銅的生成。為觀察到有紫紅色銅的生成,興趣小組同學采取了以下的方法,對實驗進行了改進。
(1)采用超細炭粉與氧化銅粉末混合進行實驗。這樣的做法的好處是能夠增大反應物接觸面積,加快反應速率能夠增大反應物接觸面積,加快反應速率。
(2)待反應結束,先將導氣管從石灰水中取出,然后關閉止水夾,讓產物自然冷卻。若不關閉止水夾,可能出現的問題是空氣進入把銅氧化空氣進入把銅氧化。
(3)探究影響實驗的反應物的比例。按下表的比例稱取2克木炭與CuO的混合物,重復實驗3次。實驗記錄如表:總質量相同(2克)但木炭與CuO比例不同的實驗對比表:
| 反應物比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10-1:11 | 1:12 | 1:13 |
| 加熱時間 | 1′51″ | 1′43″ | 1′57″ | 1′51″ | 1′51″ | 1′53″ | 4′ |
| 實驗現象 | 紅熱,產生大量氣泡,石灰水變渾濁 | 偶爾紅熱, 氣泡較少 |
|||||
| 實驗結果 | 表層銅較大:出現未完全反應的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反應較完全,生成亮紅色網狀銅塊 | 部分生成 Cu2O |
主要產物是Cu2O | |||
1:10-1:11
1:10-1:11
時,反應最充分。【考點】碳的化學性質.
【答案】能夠增大反應物接觸面積,加快反應速率;空氣進入把銅氧化;1:10-1:11
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:104引用:2難度:0.5
相似題
-
1.已知碳在一定條件下能夠與氧化銅發生反應,該反應的化學方程式為:C+2CuO
2Cu+CO2↑,其中碳在該反應中作為( )高溫A.還原劑 B.氧化劑 C.助燃劑 D.催化劑 發布:2024/12/25 10:18:46組卷:255引用:4難度:0.6 -
2.關于碳的化學性質不正確的是( )
A.溫度越高,碳的活動性越強 B.碳具有還原性,高溫時碳能使氧化鐵還原成鐵 C.碳在氧氣中充分燃燒是放熱反應,而不充分燃燒時是吸熱反應 D.碳在常溫下能長時間保存不變質 發布:2024/12/25 10:18:46組卷:283引用:3難度:0.6 -
3.下列有關碳和碳的化合物的說法中,不正確的是( )
A.CH4中,碳元素的化合為+4 B.用6B鉛筆芯、電池、小燈泡和導線可驗證石墨的導電性 C.金剛石、石墨、C60在空氣中完全燃燒的產物都是二氧化碳 D.在特定的條件下石墨轉化為金剛石的變化屬于化學變化 發布:2024/12/25 14:30:2組卷:353引用:10難度:0.7


