Ⅰ.能量之間可相互轉化:電解食鹽水制備氯氣是將電能轉化為化學能,而原電池可將化學能轉化為電能。設計兩種類型的原電池,探究其能量轉化效率。
限選材料:ZnSO4(aq),FeSO4 (aq),CuSO4 (aq);銅片,鐵片,鋅片和導線
(1)完成原電池甲的裝置示意圖1,并作相應的標注。要求:在同一燒杯中,電極與溶液含相同的金屬元素。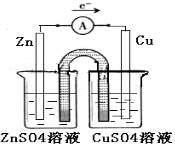

(2)以銅片為電極之一,硫酸銅溶液為電解質溶液,只在一個燒杯中組裝原電池乙,工作一段時間后,可觀察到負極有紅色固體生成,負極被腐蝕有紅色固體生成,負極被腐蝕
(3)甲乙兩種原電池中可更有效地將化學能轉化為電能的是甲甲,其原因是甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能
(4)根據犧牲陽極的陰極保護法原理,為了減緩電解質溶液中鐵片的腐蝕,在上述的材料中應選鋅片鋅片作陽極。
Ⅱ.CO與H2反應還可制備C2H5OH,C2H5OH可作為燃料使用,用C2H5OH和O2組合形成的質子交換膜燃料電池的結構示意圖如圖2:
電池總反應為C2H5OH+3O2═2CO2+3H2O,則d電極是正極正極(填“正極”或“負極”),c電極的反應方程式為CH3OH-6e-+H2O=CO2↑+6H+CH3OH-6e-+H2O=CO2↑+6H+。若線路中轉移2 mol電子,則上述燃料電池消耗的O2在標況下的體積為11.211.2 L。


【考點】設計原電池;原電池與電解池的綜合.
【答案】 ;有紅色固體生成,負極被腐蝕;甲;甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能;鋅片;正極;CH3OH-6e-+H2O=CO2↑+6H+;11.2
;有紅色固體生成,負極被腐蝕;甲;甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能;鋅片;正極;CH3OH-6e-+H2O=CO2↑+6H+;11.2
 ;有紅色固體生成,負極被腐蝕;甲;甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能;鋅片;正極;CH3OH-6e-+H2O=CO2↑+6H+;11.2
;有紅色固體生成,負極被腐蝕;甲;甲可以保持電流穩定,化學能基本都轉化為電能。而乙中的活潑金屬還可以與CuSO4溶液發生置換反應,部分能量轉化為熱能;鋅片;正極;CH3OH-6e-+H2O=CO2↑+6H+;11.2【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:14引用:1難度:0.5
相似題
-
1.某電池總反應為Fe+2Fe3+=3Fe2+,下列與此電池總反應不符的原電池是( )
A.銅片、鐵片、FeCl3溶液組成的原電池 B.石墨、鐵片、Fe(NO3)3溶液組成的原電池 C.鐵片、鋅片、Fe2(SO4)3溶液組成的原電池 D.銀片、鐵片、Fe(NO3)3溶液組成的原電池 發布:2024/12/13 10:30:1組卷:203引用:3難度:0.8 -
 2.某小組在驗證反應“Fe+2Ag+=Fe2++2Ag”,實驗探究過程如下。結合探究過程回答下列問題。
2.某小組在驗證反應“Fe+2Ag+=Fe2++2Ag”,實驗探究過程如下。結合探究過程回答下列問題。
向硝酸酸化的0.05mol?L-1硝酸銀溶液中(忽略Ag+的水解)加入過量鐵粉,攪拌后靜置,一段時間后,將燒杯底部黑色固體過濾,濾液呈黃色。
(1)檢測到濾液中含有Fe3+,可以選用的試劑為(填化學式)溶液。Fe3+產生的原因可能有以下幾種。
假設a:可能是鐵粉表面有氧化層,能產生Fe3+。
假設b:空氣中存在O2,Fe2+被氧化為Fe3+,寫出反應的離子方程式:。
假設c:酸性溶液中的具有氧化性,可產生Fe3+。NO-3
(2)某同學證明上面假設c不成立,向硝酸酸化的硝酸鈉溶液中加入過量鐵粉,攪拌后靜置,一段時間后,上層清液未變黃色,經檢驗無Fe3+。
(3)取過濾后的黑色固體,洗滌后,(填操作和現象),證明黑色固體中含有Ag。
(4)某同學利用原電池證明Ag+可以將Fe2+氧化為Fe3+,設計了如圖所示的原電池裝置。連接裝置后,電流表中有電流通過,一段時間后電流表不再偏轉(所用溶液均已去除O2)。甲溶液中的溶質為。寫出石墨電極上發生的電極反應式:。電流表指針不再偏轉后,向左側燒杯中加入FeCl3固體,發現電流表指針反向偏轉,此時石墨電極為(填“正極”或“負極”),銀電極的電極反應式為。發布:2024/10/12 6:0:3組卷:95引用:4難度:0.5 -
3.(1)某蓄電池的正負極標志難以辨別,請設計實驗方案,將蓄電池的正負極辨別出來
。
(2)解釋下列化學反應的反應速率變化關系曲線
①將除去氧化膜的鎂條投入盛有稀鹽酸的試管中,產生氫氣的速率隨時間的變化關系如圖A所示,試解釋原因:。
②過氧化氫在酶的催化作用下的分解速率隨溫度的變化關系如圖B所示,試解釋原因:。
(3)氫能源是最具應用前景的能源之一,高純氫的制備是目前的研究熱點。可利用太陽能光伏電池電解水制高純氫,工作示意圖如圖。通過控制開關連接K1或K2,可交替得到H2和O2。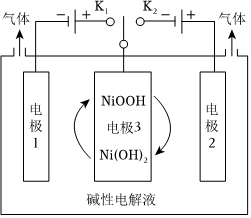
①制H2時,連接。
②改變開關連接方式,可得O2,電極反應式為。
③結合①和②中電極3的電極反應式,說明電極3的作用:。
(4)甲醇燃料電池DMFC可作電腦、汽車的能量來源。在實驗室完成一個實驗,用DMFC電解NaClO3溶液可制取NaClO4溶液,裝置如圖所示(其中DMFC以KOH作電解質)。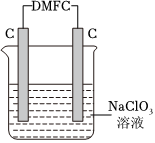
①寫出電源負極電極反應式:。
②寫出電解的總反應化學方程式:。發布:2024/9/14 4:0:8組卷:26引用:1難度:0.5


