 “84消毒液”是家居常用的防疫用品,某小組同學查看包裝說明,得到如下信息:
“84消毒液”是家居常用的防疫用品,某小組同學查看包裝說明,得到如下信息:
| 84消毒液 【有效成分】NaClO 【規格】1000mL 【濃度】4.0mol?L-1 注:①按一定比例稀釋后使用 ②不得與酸性產品(如潔廁靈)同時使用 |
(1)稀釋:將“84消毒液”原液稀釋配制成480mL c(NaClO)=0.0500mol?L-1的溶液。
①稀釋過程中,需要用到的玻璃儀器有燒杯、玻璃棒、量筒、
500mL容量瓶
500mL容量瓶
、膠頭滴管
膠頭滴管
。②稀釋時,需要取用
6.3
6.3
mL“84消毒液”原液。③下列操作會使溶液中NaClO濃度偏高的是
BC
BC
。(填標號)A.取用久置的“84消毒液”原液進行稀釋
B.定容時,俯視刻度線
C.量取“84消毒液”原液時,仰視讀數
D.定容搖勻后,液面低于刻度線,再加水至刻度線
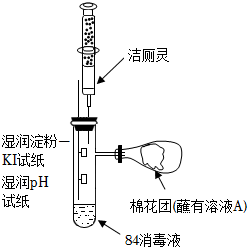
(2)利用如圖所示裝置探究84消毒液與潔廁靈的反應:
①將注射器中的潔廁靈注入試管中,可觀察到試管內產生
黃綠
黃綠
色氣體,pH試紙 先變紅,后褪色
先變紅,后褪色
,淀粉KI試紙上發生的離子反應方程式為 Cl2+2I-=I2+2Cl-
Cl2+2I-=I2+2Cl-
。②棉花團蘸取的溶液A是
NaOH
NaOH
,其作用是 吸收生成的氯氣,防止逸出造成環境污染
吸收生成的氯氣,防止逸出造成環境污染
。③該小組查資料得:“84消毒液”也不能與雙氧水混合,兩者混合會產生一種無色無味氣體,使其消毒能力大大降低,寫出該反應的化學方程式
H2O2+NaClO=NaCl+H2O+O2↑
H2O2+NaClO=NaCl+H2O+O2↑
。【考點】氯及其化合物的綜合應用;配制一定物質的量濃度的溶液.
【答案】500mL容量瓶;膠頭滴管;6.3;BC;黃綠;先變紅,后褪色;Cl2+2I-=I2+2Cl-;NaOH;吸收生成的氯氣,防止逸出造成環境污染;H2O2+NaClO=NaCl+H2O+O2↑
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:160引用:4難度:0.5
相似題
-
1.如圖是一些常見含氯產品,根據情況回答下列問題。

(1)下列有關氯單質和氯水的說法正確的是(填序號)。
①液氯是純凈物,氯水是混合物
②氯氣可使濕潤的紅色布條褪色,所以氯氣具有漂白性
③過量的鐵在少量的氯氣中燃燒生成FeCl2
④新制氯水可使藍色石蕊試紙先變紅后褪色
⑤新制氯水放置數天后酸性將減弱
(2)漂白粉常用于對環境和飲用水進行殺菌、消毒,以抑制大規模傳染病爆發。寫出漂白粉在空氣中殺菌消毒的原理。(用化學方程式表示)
(3)據報道,有人在清洗衛生間時,因混合使用“潔廁靈”(主要成分為稀鹽酸)與“84”消毒液(有效成分NaClO),而發生氯氣中毒事件,請從氧化還原的角度分析原因 (用離子方程式表示)。
(4)某“84”消毒液部分標簽如圖所示:
①計算該“84”消毒液的物質的量濃度凈含量:500mL 密度:1.19gcm-3
主要成分:25% NaClO
注意喜項:密封保存,易吸收空氣中的CO2變質mol?L-1。(保留小數點后一位)
②某實驗需用250mL上述消毒液,現用NaClO固體配制。在配制過程中,除需要燒杯、托盤天平處還必需的儀器有(寫三種),下列操作可能使配制溶液濃度偏低的是。
A.移液時,未洗滌燒杯內壁和玻璃棒
B.溶解后未經冷卻就移液
C.移液時,有少量液體濺出
D.定容時,俯視刻度線
E.容量瓶用蒸餾水洗凈后,沒烘干就直接使用
F.定容時,仰視刻度線發布:2025/1/15 8:0:2組卷:35引用:1難度:0.7 -
2.下列有關鹽酸的說法中正確的是( )
A.純凈的鹽酸是純凈物 B.鹽酸就是液態氯化氫 C.鹽酸中所有陽離子所帶的正電荷數與所有陰離子所帶的負電荷數相等 D.濃鹽酸有腐蝕性,稀鹽酸沒有腐蝕性 發布:2025/1/1 8:0:2組卷:4引用:0難度:0.9 -
3.關于鹽酸的敘述正確的是( )
A.鹽酸是純凈物 B.鹽酸是電解質 C.鹽酸是分散系 D.1L 1mol/L 鹽酸中含有HCl分子數為 1NA 發布:2025/1/1 8:0:2組卷:20引用:7難度:0.9


