當前位置:
試題詳情
學習了溶液的概念后,老師的提問及同學的回答如下圖所示:
(1)以上三位同學中能夠正確描述溶液特征的是李佳、王華李佳、王華同學.老師接著問:“你們還想知道什么?”王華回答:“影響物質在水中溶解能力的因素有哪些?”
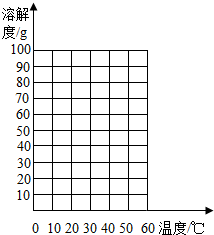
(2)針對王華的問題,老師引導同學們進行了一系列探究,下表列出了從探究實驗中獲取的部分數據,請你根據這些下表中的數據,在右邊的坐標圖中繪制A、B兩物質的溶解度曲線(圖中注明A、B).
| 溫度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | A物質 | 30 | 35 | 41 | 50 |
| B物質 | 25 | 35 | 55 | 90 | |
0℃--20℃
0℃--20℃
.(4)將在20゜C時等量的A、B飽和溶液同時降溫到10゜C,則析出晶體的質量A
小于
小于
B(填“大于”、“等于”或“小于”).(5)在20゜C時,向100g水中加入40gA物質充分溶解后,形成的A物質溶液質量是
135
135
g.【考點】溶液的概念、組成及其特點;溶解度的相關計算.
【答案】李佳、王華;0℃--20℃;小于;135
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/11/11 8:0:1組卷:18引用:3難度:0.7
相似題
-
1.多角度認識溶液,有助于我們更好地了解其在生產生活中的重要作用.
(1)溶液的形成
①將適量調味品加入水中,充分攪拌后不能形成溶液的是(填標號).
A.食鹽 B.蔗糖 C.花生油
②將生石灰和足量的水充分攪拌后靜置,取上層溶液即為澄清石灰水.寫出生石灰與水反應的化學方程式.
(2)溶液的性質
①關于溶液的說法正確的有(填標號).
A.鹽酸是純凈物 B.溶液是均一、穩定的
C.溶液的酸堿度可用石蕊溶液測定 D.飽和溶液不一定是濃溶液
②常溫下,將某固態物質A溶于水,形成飽和溶液(如圖1),進行以下實驗.回答下列問題: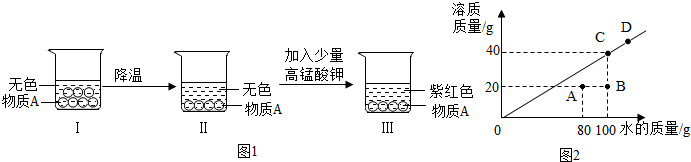
a.該物質的溶解度隨溫度升高而(填“增大”或“減小”)
b.往溶液Ⅱ中加入少量高錳酸鉀完全溶解,溶液呈紫紅色.據此現象,寫出對“飽和溶液”概念的理解.
③常溫下,該物質在不同質量的水中溶解達到飽和狀態,溶質的質量與水的質量關系如圖2所示.
a.常溫時,該物質的溶解度是g.
b.D點時,該溶液的溶質質量分數為(結果精確到0.1%)
c.將A點狀態的溶液變化到C點狀態的操作步驟為.
d.圖中A、B、C三個點表示溶液中溶質質量分數從大到小的關系是.
(3)溶液的用途
生活中溶液由許多用途,例如:碘酒能用于殺菌消毒;請再舉一個生活中溶液應用的實例:.發布:2025/1/1 8:0:2組卷:36引用:1難度:0.7 -
2.多角度認識溶液,有助于我們更好地了解其在生產生活中的重要作用.
(1)溶液的形成
①將適量調味品加入水中,充分攪拌后不能形成溶液的是(填標號).
A.食鹽 B.蔗糖 C.花生油
②將生石灰和足量的水充分攪拌后靜置,取上層清液即為澄清石灰水.寫出生石灰與水反應的化學方程式.
(2)溶液的性質
①關于溶液的說法正確的有(填標號).
A.鹽酸是純凈物 B.溶液是均一、穩定的
C.溶液的酸堿度可用石蕊溶液測定 D.飽和溶液不一定是濃溶液
②常溫下,將某固態物質A溶于水,形成飽和溶液I(如圖1),進行以下實驗.回答下列問題: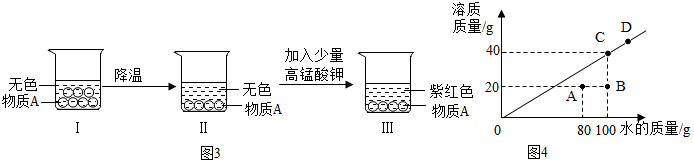
a.該物質的溶解度隨溫度升高而(填“增大”或“減小”).
b.往溶液 Ⅱ中加入少量高錳酸鉀完全溶解,溶液呈紫紅色.
據此現象,寫出對“飽和溶液”概念的理解.
③常溫時,該物質在不同質量的水中溶解達到飽和狀態,
溶質的質量與水的質量關系如圖2所示.
a.常溫時,該物質的溶解度是g.
b.D點時,該溶液的溶質質量分數為(結果精確到0.1%).
c.將A點狀態的溶液變化到C點狀態的操作步驟為.
d.圖中A、B、C三個點表示溶液中溶質質量分數從大到小的關系是.
(3)溶液的用途
生活中溶液有許多用途,例如:碘酒能用于殺菌消毒;請再舉一個生活中溶液應用的實例:.發布:2025/1/1 8:0:2組卷:34引用:1難度:0.5 -
3.多角度認識溶液,有助于我們更好地了解其在生活中的重要作用.
(1)溶液的形成
①將適量調味品加入水中,充分攪拌后不能形成溶液的是(填標號)
A.食鹽 B.蔗糖 C.花生油
②將生石灰和足量的水充分攪拌后靜置,取上層清液即為澄清石灰水,寫出生石灰與水反應的化學方程式.
(2)溶液的性質
①關于溶液的說法正確的有(填標號)
A.鹽酸是純凈物 B.溶液是均一、穩定的 C.溶液的酸堿度可用石蕊溶液測定 D.飽和溶液不一定是濃溶液
②常溫下,將某固態物質A溶于水,形成飽和溶液Ⅰ(如圖1),進行以下實驗,回答下列問題: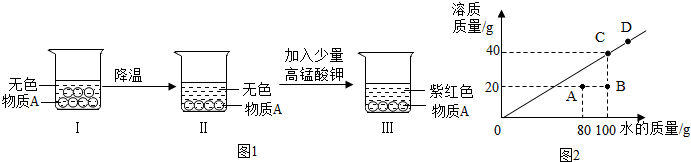
a.該物質的溶解度隨溫度升高而(填“增大”或“減小”);
b.往溶液Ⅱ中加入少量高錳酸鉀完全溶解,溶液呈紅色,據此現象,寫出對“飽和溶液”的理解.
③常溫時,該物質在不同質量的水中,溶解達到飽和狀態,溶質的質量與水的質量關系如圖2所示.
a.常溫時,該物質的溶解度是g.
b.D點時,該溶液的溶質質量分數為(結果精確到0.1%).
c.將A點狀態的溶液變化到C點狀態的操作步驟為.
d.圖中A,B,C三個點表示溶液中溶質質量分數從大到小的關系是.
(3)溶液的用途
生活中溶液有許多用途,例如:碘酒能用于殺菌消毒;請再舉一個生活中溶液應用的實例.發布:2025/1/1 8:0:2組卷:58引用:1難度:0.5


