我國科學家最近發(fā)明了一種Zn-PbO2電池,電解質(zhì)為K2SO4、H2SO4和KOH,由a和b兩種離子交換膜隔開,形成A、B、C三個電解質(zhì)溶液區(qū)域,結(jié)構(gòu)示意圖如圖:

回答下列問題:
(1)電池中,Zn為 負負極,B區(qū)域的電解質(zhì)為 K2SO4K2SO4(填“K2SO4”、“H2SO4”或“KOH”)。
(2)電池正極反應的方程式為 PbO2+2e-+SO2-4+4H+=PbSO4+2H2OPbO2+2e-+SO2-4+4H+=PbSO4+2H2O。
(3)陽離子交換膜為圖中的 aa膜(填“a”或“b”)。
(4)此電池中,消耗6.5gZn,理論上導線中轉(zhuǎn)移 0.20.2mol電子。
(5)已知E為電池電動勢[電池電動勢即電池的理論電壓,是兩個電極電位之差,E=E(+)-E(-)],則該電池與傳統(tǒng)鉛酸蓄電池相比較,EZn-PbO2 >>EPb-PbO2(填“>”、“=”或“<”)。
(6)Zn是一種重要的金屬材料,工業(yè)上一般先將ZnS氧化,再采用熱還原或者電解法制備。利用H2還原ZnS也可得到Zn,其反應式如下:ZnS(s)+H2(g)催化劑高溫Zn(s)+H2S(g)。727℃時,上述反應的平衡常數(shù)Kp=2.24×10-6。此溫度下,在盛有ZnS的剛性容器內(nèi)通入壓強為1.01×105的H2,達平衡時H2S的分壓為 0.200.20Pa(結(jié)果保留兩位小數(shù))。
SO
2
-
4
SO
2
-
4
E
Z
n
-
P
b
O
2
E
P
b
-
P
b
O
2
催化劑
高溫
【考點】原電池與電解池的綜合;化學平衡的計算.
【答案】負;K2SO4;PbO2+2e-++4H+=PbSO4+2H2O;a;0.2;>;0.20
SO
2
-
4
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:25引用:1難度:0.6
相似題
-
1.關(guān)于如圖所示的原電池,下列說法正確的是( )
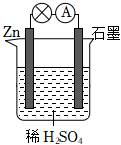
A.石墨電極上發(fā)生氧化反應 B.電子由鋅片通過導線流向石墨棒 C.該裝置將電能轉(zhuǎn)化為化學能 D.將稀硫酸換成乙醇,燈泡亮度不變 發(fā)布:2025/1/6 6:0:5組卷:83引用:5難度:0.8 -
2.某原電池結(jié)構(gòu)如圖所示,下列有關(guān)該原電池的說法正確的是( )
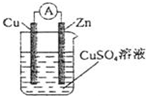
A.銅棒為負極 B.鋅棒發(fā)生還原反應 C.電子從銅棒經(jīng)外電路流向鋅棒 D.鋅棒質(zhì)量減輕 發(fā)布:2025/1/6 6:0:5組卷:417引用:11難度:0.9 -
3.一種新型短路膜電化學電池消除CO2裝置如圖所示。下列說法錯誤的是( )
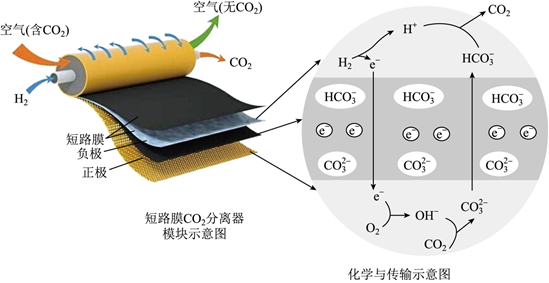
A.負極反應為:H2+2OH--2e-=2H2O B.正極反應消耗標準狀況下22.4LO2,理論上需要轉(zhuǎn)移4mol電子 C.短路膜和常見的離子交換膜不同,它既能傳遞離子,還可以傳遞電子 D.該裝置可用于空氣中CO2的捕獲,緩解溫室效應 發(fā)布:2024/12/30 19:30:2組卷:51引用:5難度:0.5
相關(guān)試卷


