回答下列問題:
Ⅰ.某小組研究Na2S溶液與KMnO4溶液反應,探究過程如圖。
| 實驗序號 | Ⅰ | Ⅱ |
| 實驗過程 |  |
 |
| 實驗現象 | 紫色變淺(pH>1),生成棕褐色沉淀(MnO2) | 溶液呈淡黃色(pH≈8),生成淺粉色沉淀(MnS) |
(1)根據實驗可知,Na2S具有
還原
還原
性。(2)甲同學預測實驗Ⅰ中S2-被氧化成
S
O
2
-
3
①根據實驗現象,乙同學認為甲的預測不合理,理由是
溶液呈淺紫色,說明酸性KMnO4溶液過量,能被其繼續氧化
S
O
2
-
3
溶液呈淺紫色,說明酸性KMnO4溶液過量,能被其繼續氧化
。S
O
2
-
3
②乙同學取實驗Ⅰ中少量溶液進行實驗,檢測到有
S
O
2
-
4
S
O
2
-
4
因為KMnO4溶液是用H2SO4酸化的,溶液中本來就存在
S
O
2
-
4
因為KMnO4溶液是用H2SO4酸化的,溶液中本來就存在
。S
O
2
-
4
③同學們經討論后,設計了如圖實驗,證實該條件下
M
n
O
-
4
S
O
2
-
4
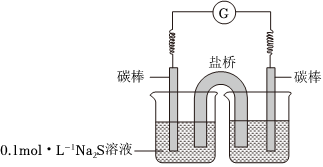
右側燒杯中的溶液是
0.01mol?L-1KMnO4溶液(H2SO4酸化至pH=0)
0.01mol?L-1KMnO4溶液(H2SO4酸化至pH=0)
;連通后電流計指針偏轉,一段時間后,取左側燒杯中的溶液,用鹽酸酸化后,滴加BaCl2溶液,觀察到有白色沉淀生成,證明S2-氧化成了S
O
2
-
4
Ⅱ.甲烷和甲醇的燃料電池具有廣闊的開發和應用前景。
(3)甲醇燃料電池(簡稱DMFC)由于結構簡單、能量轉化率高、對環境無污染,可作為常規能源的替代品而越來越受到關注。DMFC的工作原理如圖所示:
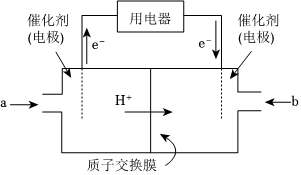
通入a物質的電極是原電池的
負
負
(填“正”或“負”)極,其電極反應式為 CH3OH-6e-+H2O=CO2↑+6H+
CH3OH-6e-+H2O=CO2↑+6H+
。(4)某研究小組將兩個甲烷燃料電池串聯后作為電源,進行飽和氯化鈉溶液電解實驗:如圖所示U形管中氯化鈉溶液的體積為800mL。閉合K后,若每個電池中甲烷通入量為0.224L(標準狀況),且反應完全,則理論上通過電解池的電量為
7.72×103C
7.72×103C
(法拉第常數F=9.65×104C?mol-1),若產生的氣體全部逸出,電解后溶液混合均勻,電解后U形管中溶液的pH為 13
13
(假設反應后溶液體積不變)。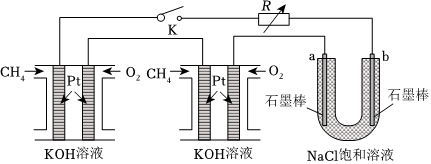
【考點】性質實驗方案的設計;原電池與電解池的綜合.
【答案】還原;溶液呈淺紫色,說明酸性KMnO4溶液過量,能被其繼續氧化;因為KMnO4溶液是用H2SO4酸化的,溶液中本來就存在;0.01mol?L-1KMnO4溶液(H2SO4酸化至pH=0);負;CH3OH-6e-+H2O=CO2↑+6H+;7.72×103C;13
S
O
2
-
3
S
O
2
-
4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/9/20 13:0:8組卷:23引用:5難度:0.5
相似題
-
1.如圖是在實驗室進行二氧化硫制備與性質實驗的組合裝置,部分固定裝置未畫出。
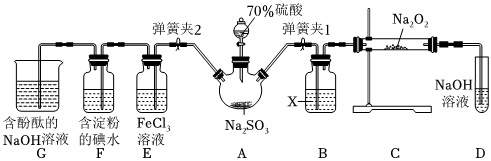
(1)在組裝好裝置后,若要檢驗A~D裝置的氣密性,其操作是首先,然后往D中裝入水,然后微熱A,觀察到D中有氣泡冒出,移開酒精燈或松開雙手,D中導管有水柱形成且高度保持不變,說明裝置氣密性良好。
(2)裝置D中盛放NaOH溶液的作用是。
(3)關閉彈簧夾1后,打開彈簧夾2,殘余氣體進入E、F、G中,能說明I-還原性弱于SO2的現象為;發生反應的離子方程式是。
(4)為了驗證E中SO2與FeCl3發生了氧化還原反應,設計了如下實驗:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,產生白色沉淀,說明SO2與FeCl3發生了氧化還原反應。上述方案是否合理?(填“合理”或“不合理”),原因是。
(5)實驗過程中G中含酚酞的NaOH溶液逐漸褪色,此實驗證明SO2具有漂白性還是其溶于水顯酸性?請設計實驗驗證:。發布:2024/12/30 14:0:1組卷:29引用:2難度:0.5 -
2.某化學興趣小組為探究銅跟濃硫酸的反應,用圖裝置進行有關實驗.請回答下列問題:
(1)裝置A中發生的化學反應的化學方程式為.
(2)裝置B 的作用是貯存多余的氣體,B中廣口瓶內應盛放的液體是(填序號)
①水 ②酸性KMnO4 ③Na2CO3溶液 ④飽和的NaHSO3溶液
(3)裝置C和D 中產生的現象相同,但原因卻不同.用離子方程式和必要的文字解釋C中溶液褪色的原因
(4)裝置D中試管口塞一團棉花,棉花中應浸有一種液體,這種液體是.
(5)實驗完畢,待A中燒瓶內液體冷卻后,過濾,向濾液中加入少量的蒸餾水稀釋,溶液為藍色.為了證明藍色只與Cu2+有關,而與其它離子無關,某同學設計了下列實驗,其中對實驗目的沒有意義的是(填序號)
①觀察稀H2SO4 溶液呈無色 ②觀察CuSO4 粉末呈白色 ③稀釋CuSO4溶液,溶液藍色變淺 ④往CuSO4溶液中加入足量NaOH溶液,生成藍色沉淀,過濾,濾液呈無色⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,過濾,濾液仍顯藍色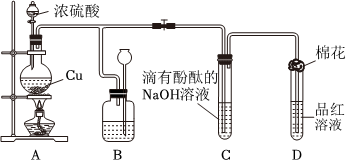 發布:2024/12/30 14:30:1組卷:13引用:2難度:0.7
發布:2024/12/30 14:30:1組卷:13引用:2難度:0.7 -
 3.某同學為探究元素周期表中元素性質的遞變規律,設計了如下系列實驗。
3.某同學為探究元素周期表中元素性質的遞變規律,設計了如下系列實驗。
Ⅰ.(1)將鈉、鉀、鎂、鋁各1mol分別投入到足量的同濃度的鹽酸中,試預測實驗結果:與鹽酸反應最劇烈,與鹽酸反應產生的氣體最多。(填元素符號)
(2)向Na2S溶液中通入氯氣出現黃色渾濁,可證明Cl的非金屬性比S強,反應的離子方程式為:。
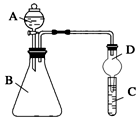
Ⅱ.利用如圖裝置可驗證同主族元素非金屬性的變化規律
(1)儀器A的名稱為。
(2)實驗室中現有藥品:①稀鹽酸 ②稀硝酸 ③Na2SiO3溶液 ④Na2CO3固體,請選擇合適藥品設計實驗驗證 N、C、Si的非金屬性的變化規律;裝置A、B中所裝藥品分別為、。(填序號)但有同學認為該裝置有缺陷,如何改進?。發布:2024/12/30 14:30:1組卷:19引用:2難度:0.5


