2023-2024學年福建省廈門市集美中學高二(上)第一次月考化學試卷(10月份)
發布:2024/9/20 13:0:8
一、單選題(共15小題,每題3分,共45分)
-
1.反應物(X)轉化為產物(Y)時的能量變化與反應進程的關系如圖曲線①所示,在反應中僅改變一種外界條件,可得到如圖曲線②。下列說法正確的是( )
 ?
?A.該反應是吸熱反應 B.X?M為反應所加的催化劑 C.改變該條件后,降低了反應的焓變 D.該條件的改變增大了單位體積內活化分子百分數 組卷:129引用:3難度:0.7 -
2.用下列裝置或操作進行相應實驗,不能達到實驗目的的是( )
選項 A B C D 目的 探究氧化性:KMnO4>Cl2>I2 用鐵絲蘸取碳酸鉀溶液進行焰色試驗 驗證Na和水反應是否為放熱反應 比較Na2CO3與NaHCO3的熱穩定性 裝置或
操作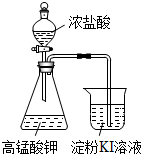
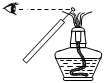
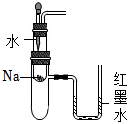
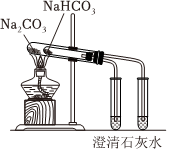
A.A B.B C.C D.D 組卷:9引用:3難度:0.6 -
3.下列有關說法正確的是( )
A.已知2C(s)+O2(g)=2CO(g)ΔH=akJ?mol-1,2C(s)+2O2(g)=2CO2(g)ΔH=bkJ?mol-1,則a<b B.500℃、30MPa下,將0.5molN2和1.5molH2置于密閉容器中反應生成NH3(g),放熱19.3kJ,其熱化學方程式為N2(g)+3H2(g)?2NH3(g)ΔH=-38.6kJ?mol-1 C.等質量的硫固體和硫蒸汽分別完全燃燒,前者放出的熱量少 D.已知P(白磷,s)=P(紅磷,s)ΔH<0,則白磷比紅磷穩定 組卷:47引用:2難度:0.5 -
4.有一合金由X、Y、Z、W四種金屬組成,若將合金放入鹽酸中,只有Z、Y能溶解;若將合金置于潮濕空氣中,表面只出現Z的化合物;若將該合金做陽極,用X鹽溶液作電解液,通電時四種金屬都以離子形式進入溶液中,但在陰極上只析出X.這四種金屬的活動性順序是( )
A.Y>Z>W>X B.Z>Y>W>X C.W>Z>Y>X D.X>Y>Z>W 組卷:265引用:43難度:0.7 -
5.鐵觸媒催化合成氨的反應歷程如圖所示,其中吸附在催化劑表面的物質用“ad”表示,下列說法正確的是( )

A.“吸附”過程吸熱,“脫附”過程放熱 B.合成氨反應N2(g)+3H2(g)?2NH3(g)的ΔH=-92kJ?mol-1 C.降溫或加壓可以增大反應速率 D.該歷程中反應速率最慢的過程為 N2ad+12H2=N2ad+3Had32組卷:11引用:4難度:0.5 -
6.以太陽能為熱源,硫碘循環分解水是一種高效、環保的制氫方法,其流程如圖所示。

相關反應的熱化學方程式為:
反應 I:SO2(g)+I2(g)+2H2O(l)═2HI(aq)+H2SO4(aq)ΔH1=-213kJ?mol-1
反應Ⅱ:H2SO4(aq)═SO2(g)+H2O(l)+O2(g)ΔH2=+327kJ?mol-112
反應Ⅲ:2HI(aq)═H2(g)+I2(g)ΔH3=+172kJ?mol-1
下列說法不正確的是( )A.該過程實現了太陽能到化學能的轉化 B.SO2和I2對總反應起到了催化作用 C.總反應的熱化學方程式為2H2O(l)═2H2(g)+O2(g)ΔH=+286kJ?mol-1 D.該過程降低了水分解制氫的活化能,但總反應的ΔH不變 組卷:82引用:4難度:0.7
二、填空題(本題包括4小題,共55分)
-
18.碲(Te)為第ⅥA元素,其單質憑借優良的性能成為制作合金添加劑、半導體、光電元件的主體材料,并被廣泛應用于冶金、航空航天、電子等領域。可從精煉銅的陽極泥(主要成分為Cu2Te)中回收碲。工藝流程圖如下:
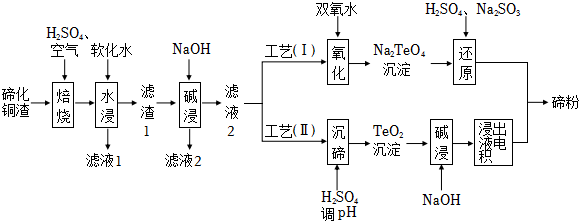
(1)“焙燒”后,碲主要以TeO2形式存在,寫出相應反應的化學方程式:。
(2)為了選擇最佳的焙燒工藝,進行了溫度和硫酸加入量的條件試驗,結果如下表所示:
則焙燒工藝中應選擇的適宜條件為溫度/℃ 硫酸加入量(理論量倍數) 浸出率/% Cu Te 450 1.25 77.3 2.63 460 1.00 80.29 2.81 1.25 89.86 2.87 1.50 92.31 7.70 500 1.25 59.83 5.48 550 1.25 11.65 10.63 。
(3)濾渣1在堿浸時發生的化學方程式為。
(4)工藝(Ⅰ)中,“還原”時發生的總的離子方程式為。
(5)由于工藝(Ⅰ)中“氧化”對溶液和物料條件要求高,有研究者采用工藝(Ⅱ)獲得碲,則“電積”過程中,陰極的電極反應式為。
(6)工業生產中,濾渣2經硫酸酸浸后得濾液3和濾渣3。
①濾液3與濾液1合并。進入銅電積系統。該處理措施的優點為。
②濾渣3中若含Au和Ag,可用將二者分離。(填字母)
A.王水
B.濃氫氧化鈉溶液
C.稀硝酸
D.濃鹽酸組卷:13引用:1難度:0.5 -
19.回答下列問題:
Ⅰ.某小組研究Na2S溶液與KMnO4溶液反應,探究過程如圖。
資料:單質硫可溶于過量硫化鈉溶液形成淡黃色的Na2S2溶液。實驗序號 Ⅰ Ⅱ 實驗過程 

實驗現象 紫色變淺(pH>1),生成棕褐色沉淀(MnO2) 溶液呈淡黃色(pH≈8),生成淺粉色沉淀(MnS)
(1)根據實驗可知,Na2S具有性。
(2)甲同學預測實驗Ⅰ中S2-被氧化成。SO2-3
①根據實驗現象,乙同學認為甲的預測不合理,理由是。
②乙同學取實驗Ⅰ中少量溶液進行實驗,檢測到有,得出S2-被氧化成SO2-4的結論,丙同學否定了該結論,理由是SO2-4。
③同學們經討論后,設計了如圖實驗,證實該條件下的確可以將S2-氧化成MnO-4。SO2-4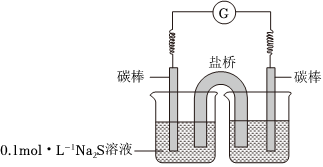
右側燒杯中的溶液是;連通后電流計指針偏轉,一段時間后,取左側燒杯中的溶液,用鹽酸酸化后,滴加BaCl2溶液,觀察到有白色沉淀生成,證明S2-氧化成了。SO2-4
Ⅱ.甲烷和甲醇的燃料電池具有廣闊的開發和應用前景。
(3)甲醇燃料電池(簡稱DMFC)由于結構簡單、能量轉化率高、對環境無污染,可作為常規能源的替代品而越來越受到關注。DMFC的工作原理如圖所示: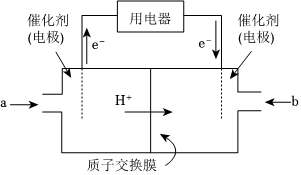
通入a物質的電極是原電池的(填“正”或“負”)極,其電極反應式為。
(4)某研究小組將兩個甲烷燃料電池串聯后作為電源,進行飽和氯化鈉溶液電解實驗:如圖所示U形管中氯化鈉溶液的體積為800mL。閉合K后,若每個電池中甲烷通入量為0.224L(標準狀況),且反應完全,則理論上通過電解池的電量為(法拉第常數F=9.65×104C?mol-1),若產生的氣體全部逸出,電解后溶液混合均勻,電解后U形管中溶液的pH為(假設反應后溶液體積不變)。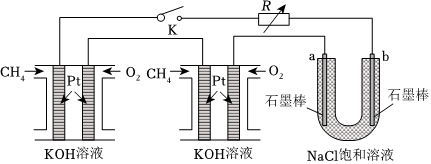 組卷:23引用:5難度:0.5
組卷:23引用:5難度:0.5


