制堿的簡(jiǎn)要流程如圖:

信息提示:下表是四種物質(zhì)在100g水中不同溫度的溶解度,其中NH4HCO3水溶液呈堿性,性質(zhì)不穩(wěn)定,36℃時(shí)開始分解為二氧化碳、氨和水,60℃可以分解完。
某學(xué)生用如圖裝置進(jìn)行模擬制堿:

試回答下列問題:
(1)若將操作Ⅰ和Ⅱ的順序調(diào)換對(duì)NaHCO3的產(chǎn)率 有有(填“有”或“沒有”)影響,原因可能是 由于CO2在水中溶解度很小,再通NH3也不能產(chǎn)生大量的碳酸氫根離子,故不可能析出NaHCO3晶體由于CO2在水中溶解度很小,再通NH3也不能產(chǎn)生大量的碳酸氫根離子,故不可能析出NaHCO3晶體。
(2)①工業(yè)制堿反應(yīng)控制在30-35℃,是因?yàn)?若高于35℃,碳酸氫銨會(huì)發(fā)生分解,若低于30℃,則反應(yīng)速率減慢若高于35℃,碳酸氫銨會(huì)發(fā)生分解,若低于30℃,則反應(yīng)速率減慢。
②加料完畢,保溫30分鐘,目的 使反應(yīng)充分進(jìn)行使反應(yīng)充分進(jìn)行;而實(shí)驗(yàn)室模擬常采用如圖丙裝置用冷水浴的原因是 冷水浴有利于碳酸氫鈉晶體析出冷水浴有利于碳酸氫鈉晶體析出。
③操作Ⅲ靜置后只析出NaHCO3晶體的原因 相同溫度下碳酸氫鈉溶解度最小相同溫度下碳酸氫鈉溶解度最小。
| 溫度/物質(zhì) | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 45.8 | 50.4 | 55.2 | 60.2 |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 |
| NH4HCO3 | 11.9 | 16.1 | 21.6 | 27.1 | 36.6 | / | / |
蒸發(fā)濃縮、冷卻結(jié)晶、過濾
蒸發(fā)濃縮、冷卻結(jié)晶、過濾
。【考點(diǎn)】純堿的制取;結(jié)晶的原理、方法及其應(yīng)用.
【答案】有;由于CO2在水中溶解度很小,再通NH3也不能產(chǎn)生大量的碳酸氫根離子,故不可能析出NaHCO3晶體;若高于35℃,碳酸氫銨會(huì)發(fā)生分解,若低于30℃,則反應(yīng)速率減慢;使反應(yīng)充分進(jìn)行;冷水浴有利于碳酸氫鈉晶體析出;相同溫度下碳酸氫鈉溶解度最小;蒸發(fā)濃縮、冷卻結(jié)晶、過濾
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:123引用:1難度:0.3
相似題
-
1.侯德榜是我國著名的化學(xué)家,為純堿和氮肥工業(yè)技術(shù)的發(fā)展做出了杰出的貢獻(xiàn),他發(fā)明的侯氏制堿法大大提高了原料的利用率,其工藝流程大致如下圖所示:
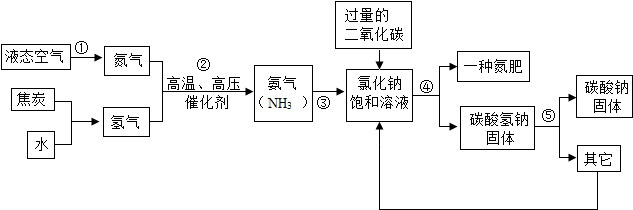
(1)上述流程中,用到的原料有空氣、焦炭、水、二氧化碳、等;
(2)上述流程中,可循環(huán)利用的物質(zhì)是;
(3)上述流程中,“一種氮肥”的化學(xué)式是。發(fā)布:2024/11/15 8:0:2組卷:22引用:1難度:0.5 -
2.侯德榜是我國著名的化學(xué)家,為純堿和氮肥工業(yè)技術(shù)的發(fā)展作出了杰出的貢獻(xiàn),他發(fā)明的侯氏制堿法大大提高了原料的利用率,其工業(yè)流程大致如圖:

(1)上述流程中,用到的原料有空氣、焦炭、水、二氧化碳以及。
(2)若上述流程中,“一種氮肥”指的是一種銨態(tài)氮肥,則其化學(xué)式是。
(3)上述流程中,為了節(jié)約成本,可循環(huán)利用的物質(zhì)是。發(fā)布:2024/11/15 8:0:2組卷:147引用:2難度:0.5 -
3.海洋是人類寶貴的自然資源,海水“曬鹽”和海水“制堿”體現(xiàn)了人類利用和改造自然的智慧,請(qǐng)根據(jù)粗鹽“制堿”的流程圖(如圖)回答問題:

(1)步驟Ⅰ除雜中,常見的方法有兩種:一是物理方法,即用NaCl溶液浸洗粗鹽,溶解除去其中的可溶性雜質(zhì),則浸洗溶液應(yīng)選用NaCl的(填“飽和”或“不飽和”)溶液;二是化學(xué)方法,操作步驟依次為:加水溶解→加過量試劑①→加過量試劑②→過濾→加適量鹽酸,以下試劑①②組合選用合理的是。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步驟Ⅲ先向飽和食鹽水中通入氨氣,再通入二氧化碳,這樣做的目的是,寫出步驟Ⅲ反應(yīng)的化學(xué)方程式。
(3)步驟Ⅳ發(fā)生的反應(yīng)屬于反應(yīng)(填基本反應(yīng)類型)。
(4)我國化學(xué)家侯德榜創(chuàng)立的聯(lián)合制堿法的優(yōu)點(diǎn)有。
A.無“索爾維氨堿法”中的廢棄物CaCl2生成,有利于保護(hù)環(huán)境
B.大大提高了食鹽的利用率,節(jié)約了成本
C.將“制堿”與制氨生產(chǎn)聯(lián)合起來,同時(shí)析出的NH4Cl晶體可用作復(fù)合肥發(fā)布:2024/12/24 10:30:2組卷:548引用:9難度:0.5
相關(guān)試卷


