 為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的焓變,并采取相應措施.化學反應的焓變通常用實驗進行測定,也可進行理論推算.
為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的焓變,并采取相應措施.化學反應的焓變通常用實驗進行測定,也可進行理論推算.
(1)實驗測得,5g甲醇在氧氣中充分燃燒生成二氧化碳氣體和液態水時釋放出113.5kJ的熱量,試寫出甲醇燃燒的熱化學方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
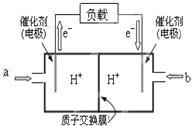
(2)如圖是某筆記本電腦用甲醇燃料電池的結構示意圖.放電時甲醇應從aa處通入(填“a”或“b”),電池內部H+向右右(填“左”或“右”)移動.寫出電池負極的電極反應式:CH3OH-6e-+H2O=CO2+6H+CH3OH-6e-+H2O=CO2+6H+.
(3)由氣態基態原子形成1mol化學鍵釋放的最低能量叫鍵能.從化學鍵的角度分析,化學反應的過程就是反應物的化學鍵的破壞和生成物的化學鍵的形成過程.在化學反應過程中,拆開化學鍵需要消耗能量,形成化學鍵又會釋放能量.
| 化學鍵 | H-H | N-H | N≡N |
| 鍵能/kJ?mol-1 | 436 | a | 945 |
+391 kJ?mol-1
+391 kJ?mol-1
.(4)依據蓋斯定律可以對某些難以通過實驗直接測定的化學反應的焓變進行推算.
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ?mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ?mol-1
根據蓋斯定律,計算2C(s,石墨)+H2(g)=C2H2(g)反應的焓變△H=
+226.7kJ?mol-1
+226.7kJ?mol-1
.【答案】2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol;a;右;CH3OH-6e-+H2O=CO2+6H+;+391 kJ?mol-1;+226.7kJ?mol-1
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:45引用:3難度:0.1
相似題
-
1.氫在地球上主要以化合態的形式存在,是宇宙中分布最廣泛的物質,它構成了宇宙質量的75%,屬于二次能源.工業上生產氫的方式很多,常見的有水電解制氫,煤炭氣化制氫,重油及天然氣水蒸氣催化制氫等.氫氣是一種理想的綠色能源,如圖1為氫能產生和利用的途徑:
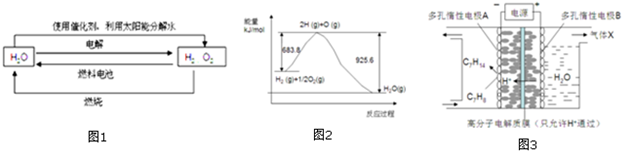
(1)圖1的四個過程中能量轉化形式有
A.2種 B.3種 C.4種 D.4種以上
(2)電解過程要消耗大量的電能,而使用微生物作催化劑在陽光下也能分解水.
2H2O(1)2H2(g)+O2(g)△H 1 2H2O(1)通電2H2(g)+O2(g)△H2光照催化劑
以上反應的△H1△H2(選填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依據圖2能量變化寫出氫氣燃燒生產液態水的熱化學方程式
(4)氫能利用需要選擇合適的儲氫材料.
①NaBH4是一種重要的儲氫載體,能與水反應生成NaBO2,且反應前后B的化合價不變,該反應的化學方程式為
②鑭鎳合金在一定條件下可吸收氫氣生產氫化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)釋放出氣態氫,根據平衡移動的原理,可改變的條件之一是
③一定條件下,如圖3所示裝置可實現有機物的電化學儲氫,使C7H8轉化為C7H14,則電解過程中產生的氣體X 為,電極A上發生的電極反應式為.發布:2024/12/17 8:0:2組卷:38引用:1難度:0.5 -
2.肼(N2H4)可作為發射火箭的燃料。已知1g液態肼(N2H4)氣體在空氣中燃燒生成氮氣和水蒸氣,放出16.7kJ的熱量,該反應的熱化學方程式是( )
A.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-16.7kJ?mol-1 B.N2H4(l)+O2(g)═2H2O(l)+N2(g),△H=-534.4kJ?mol-1 C.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-534.4kJ?mol-1 D.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=+534.4kJ?mol-1 發布:2024/12/30 3:0:4組卷:121引用:9難度:0.6 -
3.在298K、1.01×105Pa下,將0.5mol CO2通入750mL 1mol?L-1NaOH溶液中充分反應,測得反應放出xkJ的熱量。已知在該條件下,1mol CO2通入1L 2mol?L-1NaOH溶液中充分反應放出ykJ的熱量,則CO2與NaOH溶液反應生成NaHCO3的熱化學方程式正確的是( )
A.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2y-x)kJ?mol-1 B.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2x-y)kJ?mol-1 C.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(4x-y)kJ?mol-1 D.2CO2(g)+2NaOH(l)═2NaHCO3(l)ΔH=-(8x-2y)kJ?mol-1 發布:2024/12/30 4:0:1組卷:142引用:5難度:0.7


