甲醇的合成是現代化工領域研究的重點。合成甲醇時,合成氣成分主要包括CO、CO2、H2、H2O等凈化氣體和CH4、N2、Ar等惰性氣體以及H2S等有害氣體。這些氣體成分將對甲醇產品質量以及產量造成不同程度的影響。合成過程中的部分反應如下:
(ⅰ)CO(g)+2H2(g)═CH3OH(g)△H1=-90.1kJ?mol-1
(ⅱ)CO(g)+H2O(g)═CO2(g)+H2(g)△H2=-41.1kJ?mol-1
(ⅲ)CO(g)+3H2(g)═CH4(g)+H2O(g)△H3=-206kJ?mol-1
(ⅳ)2CH3OH(g)═CH3OCH3(g)+H2O(g)△H4=-24.5kJ?mol-1
(1)反應CO2(g)+3H2(g)═CH3OH(g)+H2O(g)的△H5=-49kJ?mol-1-49kJ?mol-1。該反應的化學平衡常數表達式為c(CH3OH)×c(H2O)c(CO2)×c3(H2)c(CH3OH)×c(H2O)c(CO2)×c3(H2)。下列關于CO2在合成甲醇反應中的主要作用描述,錯誤的是ACDACD。
A.可以抑制反應(ⅳ)的發生
B.可以提高碳元素的利用率
C.可以提高甲醇蒸氣的純度
D.有利于合成塔冷卻降溫過程的進行
(2)尋找合適的催化劑,一直是甲醇合成研究領域的重點。Saussey和Lavalley認為ZnO催化CO、H2合成CH3OH的機理如圖1所示。這種理論解釋了合成氣中少量的水提高了甲醇生成活性的事實,其理由為水是反應過程的催化劑(或水參與了甲醇生成的反應)水是反應過程的催化劑(或水參與了甲醇生成的反應)。
Cu作催化劑合成甲醇時,雜質氣體會發生反應H2S+Cu═CuS+H2,因為該反應是不可逆不可逆(填“可逆”或“不可逆”)的,所以會導致催化劑永久性中毒。
(3)2020年我國科學家在甲醇合成方面,進行了大量有價值的研究。
①某研究報告中指出,由于甲烷的生成,導致合成塔內溫度極難控制,使合成成本增加,其原因為生成甲烷的反應是熱效應最大的放熱反應生成甲烷的反應是熱效應最大的放熱反應。
②提高合成塔內反應溫度,合成反應速率雖然會增大,但其平衡常數會減小減小(填“增大”或“減小”),故不同階段會有不同的最佳溫度。
從理論上講,反應初期和隨著塔內甲醇濃度上升(中后期),合成塔內的最佳溫度應有何不同:前期的最佳溫度應高于中后期前期的最佳溫度應高于中后期。
實際生產中,在氣壓值為5.0MPa,用銅催化劑進行催化時,隨著反應進行合成塔內的最佳溫度范圍控制如圖2所示,這主要是為了保證催化劑有較高的活性活性。該合成粗甲醇的實際情況下,CO、CO2、H2三種氣體的氫碳比值(氣體的體積比)f應控制在5左右。已知f=(H2-CO2)(CO+CO2),CO的體積分數應在12%以下,CO2的體積分數應在3%左右,則H2的體積分數應控制在78%78%左右。
c
(
C
H
3
OH
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
3
(
H
2
)
c
(
C
H
3
OH
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
3
(
H
2
)
(
H
2
-
C
O
2
)
(
CO
+
C
O
2
)
【考點】反應熱和焓變.
【答案】-49kJ?mol-1;;ACD;水是反應過程的催化劑(或水參與了甲醇生成的反應);不可逆;生成甲烷的反應是熱效應最大的放熱反應;減小;前期的最佳溫度應高于中后期;活性;78%
c
(
C
H
3
OH
)
×
c
(
H
2
O
)
c
(
C
O
2
)
×
c
3
(
H
2
)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:38引用:2難度:0.5
相似題
-
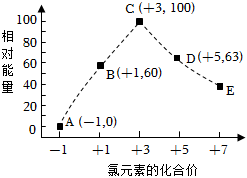 1.一定條件下,在水溶液中物質的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩定的點為( )
1.一定條件下,在水溶液中物質的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩定的點為( )A.A B.B C.C D.D 發布:2025/1/6 6:0:5組卷:0引用:1難度:0.9 -
2.下列與化學反應的能量變化有關的敘述正確的是( )
A.由石墨比金剛石穩定可知,C(金剛石)═C(石墨)△H<0 B.一個反應的反應物的總能量可能等于其生成物的總能量 C.有熱量變化的反應一定是化學反應 D.強酸與強堿的中和反應的熱化學方程式均可表示為H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1 發布:2025/1/6 6:0:5組卷:1引用:3難度:0.6 -
3.下列說法不正確的是( )
A.CH3COOH 溶液加水稀釋后,溶液中 的值減小c(CH3COOH)c(CH3COO-)B.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為α,Ka= .若加入少量醋酸鈉固體,則CH3COOH?CH3COO-+H+向左移動,α減小,Ka變小(cα)2c(1-α)C.實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵 D.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol.
CO(g)+O2(g)═CO2(g),△H=-283.0 kJ/mol.12
C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol.
則4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol發布:2025/1/1 8:0:2組卷:11引用:1難度:0.7
相關試卷


