二氧化碳是主要的溫室氣體,也是一種工業(yè)原料。將其固定及利用,有利于緩解溫室效應(yīng)帶來的環(huán)境問題。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)═2H2O(g)ΔH=-484kJ/mol
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g)ΔH=-1348kJ/mol
在催化劑作用下,CO2(g)和H2(g)反應(yīng)生成CH3OH(g)和H2O(g),該反應(yīng)的熱化學(xué)方程式是 CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH=-52 kJ/molCO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH=-52 kJ/mol。
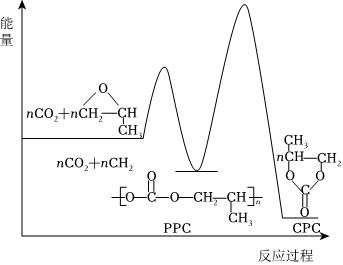
(2)用二氧化碳與環(huán)氧丙烷(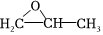 )反應(yīng)合成可降解塑料PPC,同時(shí)也能生成副產(chǎn)物CPC,其化學(xué)反應(yīng)過程中的能量變化如圖所示:在不同溫度和壓強(qiáng)下,PPC的選擇性(產(chǎn)物中PPC的質(zhì)量與產(chǎn)物總質(zhì)量的比值)和總產(chǎn)率(產(chǎn)物總質(zhì)量與反應(yīng)物投料總質(zhì)量的比值)如下表所示。
)反應(yīng)合成可降解塑料PPC,同時(shí)也能生成副產(chǎn)物CPC,其化學(xué)反應(yīng)過程中的能量變化如圖所示:在不同溫度和壓強(qiáng)下,PPC的選擇性(產(chǎn)物中PPC的質(zhì)量與產(chǎn)物總質(zhì)量的比值)和總產(chǎn)率(產(chǎn)物總質(zhì)量與反應(yīng)物投料總質(zhì)量的比值)如下表所示。
| 序號 | 溫度/℃ | 壓強(qiáng)/MPa | 總產(chǎn)率/% | PPC的選擇性/% |
| ⅰ | 25 | 0.5 | 90 | 92.1 |
| ⅱ | 25 | 1.5 | 94.9 | >99 |
| ⅲ | 25 | 2.0 | 95.4 | >99 |
| ⅳ | 40 | 1.5 | 95.6 | 96.2 |
| ⅴ | 60 | 1.5 | 99 | 76 |
其他條件相同,壓強(qiáng)越大,總產(chǎn)率和PPC的選擇性均越高
其他條件相同,壓強(qiáng)越大,總產(chǎn)率和PPC的選擇性均越高
。在25℃時(shí),實(shí)際生產(chǎn)中反應(yīng)壓強(qiáng)為1.5Mpa,而不是2.0Mpa,理由是
壓強(qiáng)為1.5 MPa時(shí),總產(chǎn)率和PPC的選擇性已經(jīng)很高了,增加到2.0 MPa,兩者增幅不大,但是對設(shè)備和能源要求提高了,不經(jīng)濟(jì)
壓強(qiáng)為1.5 MPa時(shí),總產(chǎn)率和PPC的選擇性已經(jīng)很高了,增加到2.0 MPa,兩者增幅不大,但是對設(shè)備和能源要求提高了,不經(jīng)濟(jì)
。②通過表中數(shù)據(jù)ⅱ、ⅳ、ⅴ可知溫度升高會使PPC的選擇性下降,結(jié)合如圖說明其原因可能是
溫度升高,速率的增幅副反應(yīng)大于主反應(yīng),或溫度升高,有利于PPC反應(yīng)生成CPC
溫度升高,速率的增幅副反應(yīng)大于主反應(yīng),或溫度升高,有利于PPC反應(yīng)生成CPC
。
【考點(diǎn)】熱化學(xué)方程式;化學(xué)平衡的影響因素.
【答案】CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH=-52 kJ/mol;其他條件相同,壓強(qiáng)越大,總產(chǎn)率和PPC的選擇性均越高;壓強(qiáng)為1.5 MPa時(shí),總產(chǎn)率和PPC的選擇性已經(jīng)很高了,增加到2.0 MPa,兩者增幅不大,但是對設(shè)備和能源要求提高了,不經(jīng)濟(jì);溫度升高,速率的增幅副反應(yīng)大于主反應(yīng),或溫度升高,有利于PPC反應(yīng)生成CPC
【解答】
【點(diǎn)評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/10/18 1:0:1組卷:2引用:1難度:0.6
相似題
-
1.肼(N2H4)可作為發(fā)射火箭的燃料。已知1g液態(tài)肼(N2H4)氣體在空氣中燃燒生成氮?dú)夂退魵猓懦?6.7kJ的熱量,該反應(yīng)的熱化學(xué)方程式是( )
A.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-16.7kJ?mol-1 B.N2H4(l)+O2(g)═2H2O(l)+N2(g),△H=-534.4kJ?mol-1 C.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-534.4kJ?mol-1 D.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=+534.4kJ?mol-1 發(fā)布:2024/12/30 3:0:4組卷:121引用:9難度:0.6 -
2.氫在地球上主要以化合態(tài)的形式存在,是宇宙中分布最廣泛的物質(zhì),它構(gòu)成了宇宙質(zhì)量的75%,屬于二次能源.工業(yè)上生產(chǎn)氫的方式很多,常見的有水電解制氫,煤炭氣化制氫,重油及天然氣水蒸氣催化制氫等.氫氣是一種理想的綠色能源,如圖1為氫能產(chǎn)生和利用的途徑:
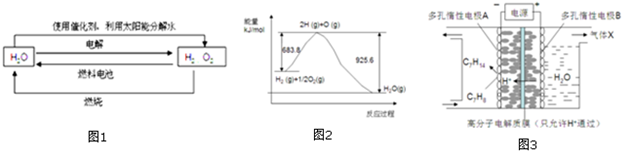
(1)圖1的四個(gè)過程中能量轉(zhuǎn)化形式有
A.2種 B.3種 C.4種 D.4種以上
(2)電解過程要消耗大量的電能,而使用微生物作催化劑在陽光下也能分解水.
2H2O(1)2H2(g)+O2(g)△H 1 2H2O(1)通電2H2(g)+O2(g)△H2光照催化劑
以上反應(yīng)的△H1△H2(選填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依據(jù)圖2能量變化寫出氫氣燃燒生產(chǎn)液態(tài)水的熱化學(xué)方程式
(4)氫能利用需要選擇合適的儲氫材料.
①NaBH4是一種重要的儲氫載體,能與水反應(yīng)生成NaBO2,且反應(yīng)前后B的化合價(jià)不變,該反應(yīng)的化學(xué)方程式為
②鑭鎳合金在一定條件下可吸收氫氣生產(chǎn)氫化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)釋放出氣態(tài)氫,根據(jù)平衡移動(dòng)的原理,可改變的條件之一是
③一定條件下,如圖3所示裝置可實(shí)現(xiàn)有機(jī)物的電化學(xué)儲氫,使C7H8轉(zhuǎn)化為C7H14,則電解過程中產(chǎn)生的氣體X 為,電極A上發(fā)生的電極反應(yīng)式為.發(fā)布:2024/12/17 8:0:2組卷:38引用:1難度:0.5 -
3.在298K、1.01×105Pa下,將0.5mol CO2通入750mL 1mol?L-1NaOH溶液中充分反應(yīng),測得反應(yīng)放出xkJ的熱量。已知在該條件下,1mol CO2通入1L 2mol?L-1NaOH溶液中充分反應(yīng)放出ykJ的熱量,則CO2與NaOH溶液反應(yīng)生成NaHCO3的熱化學(xué)方程式正確的是( )
A.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2y-x)kJ?mol-1 B.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2x-y)kJ?mol-1 C.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(4x-y)kJ?mol-1 D.2CO2(g)+2NaOH(l)═2NaHCO3(l)ΔH=-(8x-2y)kJ?mol-1 發(fā)布:2024/12/30 4:0:1組卷:142引用:5難度:0.7
相關(guān)試卷


