2022-2023學(xué)年北京二十二中高二(上)期中化學(xué)試卷
發(fā)布:2024/10/18 1:0:1
一、(選擇題,共40分)在每題列出的四個(gè)選項(xiàng)中,選出最符合題目要求的一項(xiàng)。
-
1.下列物質(zhì)中,既能導(dǎo)電又是電解質(zhì)的是( )
A.稀H2SO4 B.熔融態(tài)NaOH C.NH3 D.NaCl固體 組卷:1引用:1難度:0.8 -
2.下列電離方程式正確的是( )
A.NaHSO4═Na++HSO4- B.NaHCO3?Na++H++CO23- C.H3PO4?3H++PO43- D.HF?H++F- 組卷:43引用:5難度:0.9 -
3.下列敘述正確的是( )
A.化學(xué)反應(yīng)除了生成新的物質(zhì)外,還伴隨著能量的變化 B.物質(zhì)燃燒不一定是放熱反應(yīng) C.放熱的化學(xué)反應(yīng)不需要加熱就能發(fā)生 D.吸熱反應(yīng)不加熱就不會發(fā)生 組卷:20引用:8難度:0.9 -
4.在25℃、1.01×105 Pa下,反應(yīng)2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ?mol-1能自發(fā)進(jìn)行的合理解釋是( )
A.該反應(yīng)是分解反應(yīng) B.該反應(yīng)的熵增效應(yīng)大于焓變效應(yīng) C.該反應(yīng)是熵減反應(yīng) D.該反應(yīng)是放熱反應(yīng) 組卷:606引用:6難度:0.9 -
5.下列不能表明醋酸是弱電解質(zhì)的是( )
A.0.1mol/L的醋酸水溶液中,c(H+)約為10-3mol/L B.常溫下同濃度醋酸水溶液的導(dǎo)電性比鹽酸弱 C.醋酸水溶液能使紫色石蕊試液變紅 D.醋酸稀溶液中同時(shí)存在CH3COOH和CH3COO- 組卷:16引用:6難度:0.7 -
6.下列說法正確的是( )
A.可逆反應(yīng)的特征是正反應(yīng)速率和逆反應(yīng)速率相等 B.在其他條件不變時(shí),使用催化劑只能改變反應(yīng)速率,而不能改變化學(xué)平衡狀態(tài) C.在其他條件不變時(shí),升高溫度可以使平衡向放熱反應(yīng)方向移動 D.在其他條件不變時(shí),增大壓強(qiáng)一定會破壞氣體反應(yīng)的平衡狀態(tài) 組卷:61引用:31難度:0.9 -
7.已知299K時(shí),合成氨反應(yīng) N2(g)+3H2(g)?2NH3(g)△H=-92.0kJ/mol,將此溫度下的1mol N2和3mol H2放在一密閉容器中,在催化劑存在時(shí)進(jìn)行反應(yīng),測得反應(yīng)放出的熱量為(忽略能量損失)( )
A.一定大于92.0kJ B.一定等于92.0kJ C.一定小于92.0kJ D.不能確定 組卷:275引用:52難度:0.7 -
8.一定量的鹽酸跟過量的鐵粉反應(yīng)時(shí),為了減緩反應(yīng)速率,且不影響生成氫氣的總量,可向鹽酸中加入適量的( )
①NaOH固體 ②KNO3溶液 ③水 ④CH3COONa固體A.①③ B.②④ C.②③ D.③④ 組卷:73引用:4難度:0.8
二、(非選擇題,共60分)本部分共8題,共60分。
-
 25.氨氣是生產(chǎn)化肥、硝酸等的重要原料,圍繞合成氨人們進(jìn)行了一系列的研究
25.氨氣是生產(chǎn)化肥、硝酸等的重要原料,圍繞合成氨人們進(jìn)行了一系列的研究
(1)氫氣既能與氮?dú)庥帜芘c氧氣發(fā)生反應(yīng),但是反應(yīng)的條件卻不相同。
已知:2H2(g)+O2(g)═2H2O(g)ΔH=-483.6kJ/mol
N2(g)+3H2(g)?2NH3(g)ΔH=-92.4kJ/mol
計(jì)算斷裂1molN≡N鍵需要能量kJ,氮?dú)夥肿又谢瘜W(xué)鍵比氧氣分子中的化學(xué)鍵(填“強(qiáng)”或“弱”),因此氫氣與二者反應(yīng)的條件不同。
(2)在恒溫恒容密閉容器中按照甲、乙、丙三種方式分別投料,發(fā)生反應(yīng):
N2(g)+3H2(g)?2NH3(g)測得甲容器中H2的轉(zhuǎn)化率為40%。
①判斷乙容器中反應(yīng)進(jìn)行的方向N2(mol) H2(mol) NH3(mol) 甲 1 3 0 乙 0.5 1.5 1 丙 0 0 4 。(填“正向”或“逆向”)
②達(dá)平衡時(shí),甲、乙、丙三容器中NH3的體積分?jǐn)?shù)大小順序?yàn)?。組卷:0引用:1難度:0.5 -
26.二氧化碳是主要的溫室氣體,也是一種工業(yè)原料。將其固定及利用,有利于緩解溫室效應(yīng)帶來的環(huán)境問題。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)═2H2O(g)ΔH=-484kJ/mol
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g)ΔH=-1348kJ/mol
在催化劑作用下,CO2(g)和H2(g)反應(yīng)生成CH3OH(g)和H2O(g),該反應(yīng)的熱化學(xué)方程式是。
(2)用二氧化碳與環(huán)氧丙烷(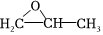 )反應(yīng)合成可降解塑料PPC,同時(shí)也能生成副產(chǎn)物CPC,其化學(xué)反應(yīng)過程中的能量變化如圖所示:在不同溫度和壓強(qiáng)下,PPC的選擇性(產(chǎn)物中PPC的質(zhì)量與產(chǎn)物總質(zhì)量的比值)和總產(chǎn)率(產(chǎn)物總質(zhì)量與反應(yīng)物投料總質(zhì)量的比值)如下表所示。
)反應(yīng)合成可降解塑料PPC,同時(shí)也能生成副產(chǎn)物CPC,其化學(xué)反應(yīng)過程中的能量變化如圖所示:在不同溫度和壓強(qiáng)下,PPC的選擇性(產(chǎn)物中PPC的質(zhì)量與產(chǎn)物總質(zhì)量的比值)和總產(chǎn)率(產(chǎn)物總質(zhì)量與反應(yīng)物投料總質(zhì)量的比值)如下表所示。
①通過表中數(shù)據(jù)ⅰ、ⅱ、ⅲ可以得出的結(jié)論是序號 溫度/℃ 壓強(qiáng)/MPa 總產(chǎn)率/% PPC的選擇性/% ⅰ 25 0.5 90 92.1 ⅱ 25 1.5 94.9 >99 ⅲ 25 2.0 95.4 >99 ⅳ 40 1.5 95.6 96.2 ⅴ 60 1.5 99 76 。
在25℃時(shí),實(shí)際生產(chǎn)中反應(yīng)壓強(qiáng)為1.5Mpa,而不是2.0Mpa,理由是。
②通過表中數(shù)據(jù)ⅱ、ⅳ、ⅴ可知溫度升高會使PPC的選擇性下降,結(jié)合如圖說明其原因可能是。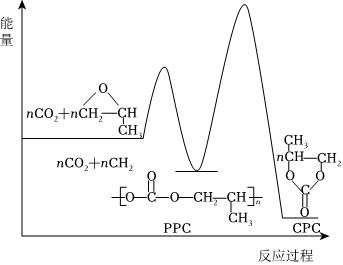 組卷:2引用:1難度:0.6
組卷:2引用:1難度:0.6


