合成氨的反應對人類解決糧食問題貢獻巨大,德國化學家F.Haber因合成氨而獲得諾貝爾獎。合成氨反應熱化學方程式如下:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol。
(1)已知N2(g)+3H2(g)?2NH3(g)不加入催化劑時正反應的活化能為326kJ/mol,則該反應逆反應的活化能為 418.4418.4kJ/mol。
(2)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol,H2的燃燒熱△H=-285.8kJ/mol。則NH3(g)+54O2(g)=NO(g)+32H2O(1)△H=-292.5-292.5kJ/mol
(3)一定溫度下,向恒容的密閉容器中充入一定量的N2和H2發生反應,測得各組分濃度隨時間變化如圖所示。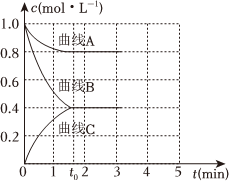
①表示c(H2)變化的曲線是 曲線B曲線B(填“曲線A”“曲線B”或“曲線C”)。
②0~t0時用NH3表示的化學反應速率為v(NH3)=0.4t00.4t0mol?L-1?min-1
③下列能說明該反應達到平衡狀態的是 BCBC(填標號)。
A.容器中混合氣體的密度不隨時間變化
B.容器中的n(N2)與n(H2)的比值不隨時間變化
C.斷裂3molH-H的同時斷裂6molN-H鍵
D.3v正(H2)=2v逆(NH3)
(4)合成氨反應在某催化劑條件下的相對能量一反應歷程如圖所示(ad為吸附態):
①該過程中含氮的中間產物有 22種(填數字)。
②活化能最大的那一步基元反應方程式為 N2(ad)+3H2(ad)=N2H2(ad)+2H2(ad)N2(ad)+3H2(ad)=N2H2(ad)+2H2(ad)。
③下列說法正確的是 ABAB(填標號)。
A.最后一步NH3(ad)變為NH3(g)為吸熱過程.
B.催化劑參與反應,但不改變合成氨反應的△H
C.催化劑和升溫都能降低反應的活化能,加快合成氨的反應速率
D.使用催化劑和壓縮容器體積加壓都能增大活化分子百分數,加快合成氨反應速率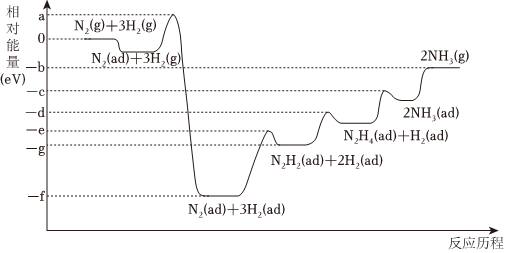
5
4
3
2
0
.
4
t
0
0
.
4
t
0
【答案】418.4;-292.5;曲線B;;BC;2;N2(ad)+3H2(ad)=N2H2(ad)+2H2(ad);AB
0
.
4
t
0
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:32引用:1難度:0.6
相似題
-
1.氨既是一種重要的化工產品,又是一種重要的化工原料。如圖為合成氨以及氨催化制硝酸的流程示意圖。下列說法不正確的是( )
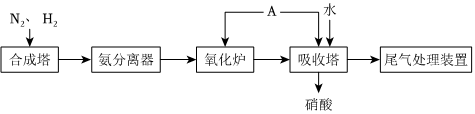
A.可以利用NH3易液化的性質分離出NH3 B.吸收塔中通入A是為了提高原料的利用率 C.可以用NH3進行氮氧化物的尾氣處理 D.合成氨以及氨催化制硝酸的流程中氮元素均被氧化 發布:2024/12/30 7:30:1組卷:117引用:7難度:0.7 -
2.2007年諾貝爾化學獎授予埃特爾以表彰其對于合成氨反應機理的研究,氮氣和氫氣分子在催化劑表面的部分變化過程如圖所示。下列說法不正確的是( )
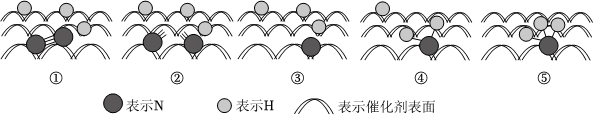
A.圖①→②過程吸熱,圖②→③過程放熱 B.溫度、壓強、催化劑都能改變反應的ΔH C.N2在反應過程中三鍵均發生斷裂 D.反應過程中存在-NH-、-NH2等中間產物 發布:2024/11/19 16:0:1組卷:78引用:5難度:0.7 -
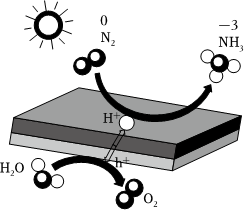 3.光催化固氮合成氨的機理如圖所示,下列說法不正確的是( )
3.光催化固氮合成氨的機理如圖所示,下列說法不正確的是( )A.NH3分子是極性分子 B.此反應中氮氣作氧化劑 C.無論使用哪種催化劑,同一個反應的活化能是不變的 D.此反應的化學反應方程式是:2N2+6H2O 4NH3+3O2催化劑光發布:2024/12/3 18:0:1組卷:74引用:1難度:0.7


