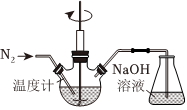
 利用Zn和KNO3溶液反應模擬地下水的脫硝過程,并探究脫硝原理及相關因素對脫硝速率的影響。模擬過程的實驗裝置如圖所示。
利用Zn和KNO3溶液反應模擬地下水的脫硝過程,并探究脫硝原理及相關因素對脫硝速率的影響。模擬過程的實驗裝置如圖所示。
(1)實驗室用稀H2SO4洗滌Zn粒,再用蒸餾水洗滌至接近中性;將KNO3溶液的pH調至2.5。
①用稀H2SO4洗滌Zn粒的目的是 除去鋅粒表面的氧化膜除去鋅粒表面的氧化膜。
②向上述KNO3溶液中加入足量洗滌后的Zn粒,寫出Zn與KNO3溶液反應生成NH+4的離子方程式 4Zn+NO-3+10H+=4Zn2++NH+4+3H2O4Zn+NO-3+10H+=4Zn2++NH+4+3H2O。
③錐形瓶中NaOH溶液的作用是 吸收副反應可能產生的氮氧化物吸收副反應可能產生的氮氧化物。
(2)某興趣小組進行了如下實驗:取兩套如圖所示裝置,分別加入等體積、等濃度的KNO3溶液;將溶液的pH值調節為2.5,并通入氮氣;將其中一套實驗裝置浸入熱水浴中(或浸入冰水浴中);向三頸瓶中分別加入足量且等質量的同種Zn粒,用離子色譜儀測定相同反應時間時三頸瓶中NO-3的濃度。(已知:溶液中的NO-3的物質的量濃度可用離子色譜儀測定)
①該實驗的目的是 探究溫度對脫氮速率的影響探究溫度對脫氮速率的影響。
②該實驗過程中采用了科學探究中一種重要的思想方法是 控制變量法控制變量法。
(3)反應過程中有NO-2生成。為測定反應液中NO-2的含量,取過濾后的濾液100mL,用0.005mol?L-1KMnO4酸性溶液滴定,消耗KMnO4溶液的體積為16.00mL(已知2MnO-4+5NO-2+6H+=2Mn2++5NO-3+3H2O,且在此條件下NH+4不與KMnO4酸性溶液反應)。計算過濾后的濾液中NO-2的物質量濃度 反應的關系式為:2MnO-4~5NO-2,則c(NO-2)=0.005×16×10-3×52100×10-3mol/L=0.002mol/L反應的關系式為:2MnO-4~5NO-2,則c(NO-2)=0.005×16×10-3×52100×10-3mol/L=0.002mol/L。(寫出計算過程)
NH
+
4
NO
-
3
NH
+
4
NO
-
3
NH
+
4
NO
-
3
NO
-
3
NO
-
2
NO
-
2
M
n
O
-
4
NO
-
2
NO
-
3
NH
+
4
NO
-
2
M
n
O
-
4
NO
-
2
N
O
-
2
0
.
005
×
16
×
1
0
-
3
×
5
2
100
×
1
0
-
3
M
n
O
-
4
NO
-
2
N
O
-
2
0
.
005
×
16
×
1
0
-
3
×
5
2
100
×
1
0
-
3
【考點】探究影響化學反應速率的因素.
【答案】除去鋅粒表面的氧化膜;4Zn++10H+=4Zn2+++3H2O;吸收副反應可能產生的氮氧化物;探究溫度對脫氮速率的影響;控制變量法;反應的關系式為:2~5,則c()=mol/L=0.002mol/L
NO
-
3
NH
+
4
M
n
O
-
4
NO
-
2
N
O
-
2
0
.
005
×
16
×
1
0
-
3
×
5
2
100
×
1
0
-
3
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/8/1 8:0:9組卷:28引用:2難度:0.6
相似題
-
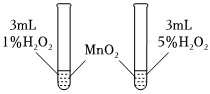 1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )
1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )A.催化劑 B.溫度 C.濃度 D.壓強 發布:2024/12/30 14:0:1組卷:44引用:3難度:0.6 -
2.為探究影響化學反應速率的因素,某研究小組設計了如下五個實驗。按要求回答下列問題(已知:Cu2+、Fe3+對H2O2的分解起催化作用)。
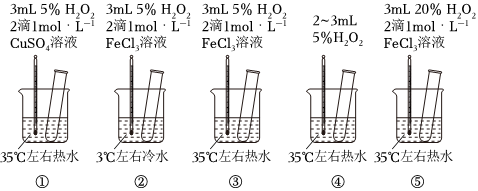
(1)為探究溫度對化學反應速率的影響,應選擇實驗(填序號,下同),選擇的依據是。
(2)為探究催化劑對化學反應速率的影響,同時探究催化劑不同催化效果不同,應選擇實驗。
(3)通過觀察發現實驗⑤比實驗③現象明顯,其原因是。
(4)根據上述實驗,用H2O2快速制取少量O2,可采取的三條措施為。發布:2024/12/30 14:30:1組卷:8引用:5難度:0.5 -
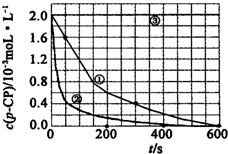 3.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
3.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
(1)編號③的實驗目的是實驗序號 實驗目的 T/K pH c/10-3mol?L-1 H2O2 Fe2+ ① 為以下實驗作參照物 298 3 6.0 0.30 ② 探究溫度對降解反應速率的影響 313 3 6.0 0.30 ③ 298 10 6.0 0.30 .
(2)實驗測得不同實驗編號中p-CP的濃度隨時間變化的關系如圖所示.請根據實驗①曲線,計算降解反應在50-300s內的平均反應速率v(p-CP)=.
(3)實驗①②表明,溫度與該降解反應速率的關系是.
(二)已知Fe3+和I-在水溶液中的反應為2I-+2Fe3+=2Fe2++I2.正向反應速率和I-、Fe3+的濃度關系為v=kcm(I-)cn(Fe3+)(k為常數)
(4)請分析下表提供的數據回答以下問題:
①在v=kcm(I-)cn(Fe3+)中,m、n的值為c(I-)/(mol?L-1) c(Fe3+)/(mol?L-1) v/(mol?L-1?s-1) (1) 0.20 0.80 0.032k (2) 0.60 0.40 0.144k (3) 0.80 0.20 0.128k .(選填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
②I-濃度對反應速率的影響Fe3+濃度對反應速率的影響(填“<”、“>”或“=”).
(三)一定溫度下,反應FeO(s)+CO(g)?Fe(s)+CO2(g)的化學平衡常數為3.0,該溫度下將2mol FeO、4mol CO、5mol Fe、6mol CO2加入容積為2L的密閉容器中反應.請通過計算回答:
(5)v(正)v(逆)(填“>”、“<”或“=”);若將5mol FeO、4mol CO加入同樣的容器中,在相同溫度下達到平衡,則CO的平衡轉化率為.發布:2024/12/30 14:30:1組卷:19引用:2難度:0.5


