氮化鈉(Na3N)是一種實施管制的化學品,它是科學家制備的一種重要的化合物,與水作用可產生NH3。請回答下列問題:
(1)Na3N的電子式是 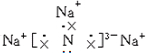
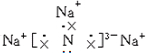 。
。
(2)Na3N與鹽酸反應生成鹽的電子式分別是 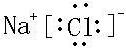 、
、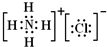
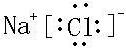 、
、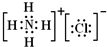 。
。
(3)Na3N與水的反應屬于 復分解復分解(填基本反應類型)反應。
(4)比較Na3N中兩種微粒的半徑:r(Na+) <<r(N3-)(填“>”、“=”或“<”)。
(5)將某主族元素的最高價氧化物R2O的4.7g溶于95.3g水中,所得溶液的質量分數為5.6%,R的原子核中含有20個中子;主族元素Q的單質能和水劇烈反應放出O2,并能和R形成典型的離子化合物RQ。試通過計算寫出R和Q在元素周期表中的位置。
R 第4周期第ⅠA族第4周期第ⅠA族;
Q 第2周期第ⅦA族第2周期第ⅦA族。
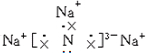
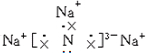
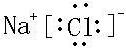 、
、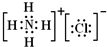
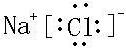 、
、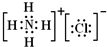
【答案】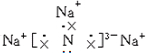 ;
;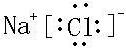 、
、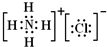 ;復分解;<;第4周期第ⅠA族;第2周期第ⅦA族
;復分解;<;第4周期第ⅠA族;第2周期第ⅦA族
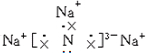 ;
;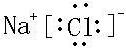 、
、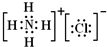 ;復分解;<;第4周期第ⅠA族;第2周期第ⅦA族
;復分解;<;第4周期第ⅠA族;第2周期第ⅦA族【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:10引用:1難度:0.6
相似題
-
1.寫出下列化合物的電子式:
水:二氧化碳:過氧化鈉:.發布:2024/12/30 19:0:1組卷:68引用:2難度:0.5 -
2.下列有關化學用語表示正確的是( )
A.硫離子:S-2 B.用電子式表示氯化氫分子的形成過程: 
C.氫氧根的電子式: 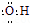
D.HClO的結構式:H-O-Cl 發布:2025/1/4 8:0:1組卷:22引用:1難度:0.9 -
3.下列關于化學用語的表述正確的是( )
A.原子核內有10個中子的氧原子為816O B.HClO的結構式為H-O-Cl C.乙烷的分子式為CH3CH3 D.NH4Cl的電子式為 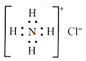 發布:2025/1/4 8:0:1組卷:11引用:1難度:0.9
發布:2025/1/4 8:0:1組卷:11引用:1難度:0.9


