某學習小組利用銹蝕嚴重的廢銅屑(銅銹的主要成分是堿式碳酸銅[Cu2(OH)2CO3])為原料回收銅,分別采用圖1的兩種方案。請回答下列問題。
資料1:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O
資料2:回收銅的兩種實驗方案。
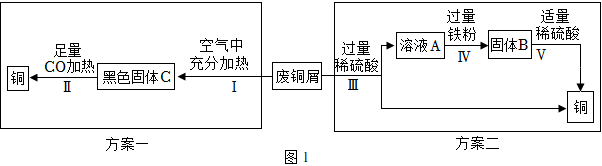
(1)方案一中步驟Ⅱ生成的二氧化碳不能直接排放到空氣中,需要將其回收后再與碳粉作用,又可以生成CO,寫出該過程的化學反應方程式:C+CO2 高溫 2COC+CO2 高溫 2CO。
(2)方案二中步驟Ⅲ、Ⅳ、Ⅴ都涉及到的操作名稱是 過濾過濾,該操作所需的玻璃儀器有:玻璃棒、燒杯和 漏斗漏斗。
(3)方案二中步驟Ⅳ加入過量鐵粉的目的是 將硫酸銅中的銅完全置換出來將硫酸銅中的銅完全置換出來,該反應是利用鐵的金屬活動性比銅的 強強(填“強”或“弱”)。
(4)理論上等質量的廢銅屑通過兩種方案獲得銅的質量比較:方案一 ==方案二(選填“>、=、<”)。
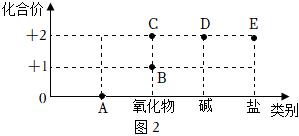
(5)如圖2為銅元素的價類轉化二維圖,寫出D點對應物質的化學式 Cu(OH)2Cu(OH)2。步驟Ⅳ實現的是E→AA點(填字母)的轉化。
(6)堿式碳酸銅和碳酸銅混合物11.8g,與100g9.8%的稀硫酸剛好完全反應,得到的溶液通過方案二中的步驟Ⅳ和步驟Ⅴ,最終能夠得到銅 6.46.4g(不需要寫出計算過程)。
高溫
高溫
【答案】C+CO2 2CO;過濾;漏斗;將硫酸銅中的銅完全置換出來;強;=;Cu(OH)2;A;6.4
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:23引用:3難度:0.5
相似題
-
1.新冠肺炎疫情防控期間,西安市各學校開展全域噴灑低濃度、有效成分是次氯酸鈉的“84”消毒液進行消毒。如圖所示是模擬制備“84”消毒液的流程(Cl2是一種黃綠色的有毒氣體)。請回答下列問題:
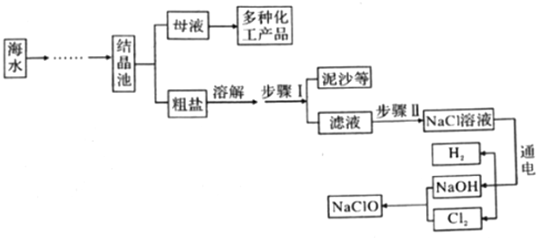
(1)NaOH的俗稱為(寫一種)。
(2)步驟Ⅱ中,通常用碳酸鈉溶液除去濾液中的氯化鈣雜質,請寫出有關反應的化學方程式。
(3)電解水時,一般在水中加入少量NaOH以增強水的導電性,不能加入NaCl的原因是。發布:2025/1/3 8:0:1組卷:6引用:1難度:0.5 -
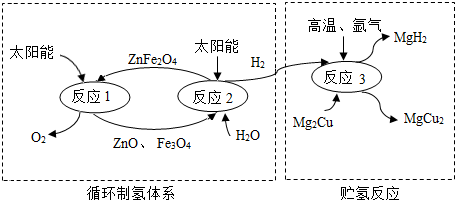 2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )
2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )A.ZnFe2O4中Fe的化合價為+3價 B.循環制氫反應中無需加入ZnFe2O4 C.反應1和反應2的總方程式為:2H2O 2H2↑+O2↑通電D.M與足量稀鹽酸反應生成的H2質量大于反應2產生的H2質量 發布:2024/12/31 8:0:1組卷:48引用:2難度:0.5 -
3.某種家用的消毒液的主要成分是次氯酸鈉(NaClO),制取NaClO的化學方程式為:Cl2+2NaOH=NaClO+NaCl+H2O,下列說法錯誤的是( )
A.NaClO中氯元素的化合價為-1 B.反應中用到的NaOH俗稱燒堿 C.該化學方程式中涉及到兩種鹽 D.反應前后氯元素化合價既升高又降低 發布:2025/1/3 8:0:1組卷:71引用:1難度:0.7


