中科院官微曾給出灰霾中細顆粒物的成因,部分分析如圖1所示。

(1)根據如圖1信息可以看出,所列的氣體污染物并非由機動車行駛造成的是SO2SO2。
汽車發動機廢氣稀燃控制系統主要工作原理如圖2所示;寫出稀燃過程中NO發生的主要反應的方程式2NO+O2=2NO22NO+O2=2NO2。
(2)農業活動排出的氨可能是施用的化肥分解,也可能是施用不當導致的。比如某些氮肥與堿性肥料混合施用會釋出氨,用離子方程式解釋NH4++OH-═NH3↑+H2ONH4++OH-═NH3↑+H2O
(3)經過研究發現我國的霾呈中性,其主要原因如圖3所示,A的化學式是SO42-SO42-。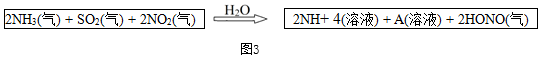
(4)煤燃燒排放的煙氣含有SO2和NOx,采用NaClO2溶液作為吸收劑可同時對煙氣進行脫硫、脫硝。將含有SO2和NOx的煙氣通入盛有NaClO2溶液的反應器中,反應一段時間后,測得溶液中離子濃度的有關數據如下(其他極微量離子忽略不計):
| 離子 | Na+ | SO42- | NO3- | H+ | Cl- |
| 濃度/(mol?L-1) | 5.5×10-3 | 8.5×10-4 | y | 2.8×10-4 | 3.5×10-3 |
4NO+3ClO2-+2H2O=4NO3-+3Cl-+4H+
4NO+3ClO2-+2H2O=4NO3-+3Cl-+4H+
。②表中y=
5.8×10-4
5.8×10-4
。(5)工業生產硝酸也有可能產生NOx污染。請寫出硝酸生產中的第一步:氨的催化氧化的化學方程式
4NH3+5O2 4NO+6H2O
P
t
△
4NH3+5O2 4NO+6H2O
。若用氮氣制氨的產率為90%,用氨生產硝酸時氨的催化氧化和氮氧化物轉化為硝酸的損耗依次為5%、3%,1000mol氮氣可制P
t
△
1659
1659
mol硝酸。【答案】SO2;2NO+O2=2NO2;NH4++OH-═NH3↑+H2O;SO42-;4NO+3ClO2-+2H2O=4NO3-+3Cl-+4H+;5.8×10-4;4NH3+5O2 4NO+6H2O;1659
P
t
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:76引用:2難度:0.6
相似題
-
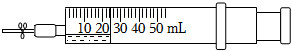 1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
(1)根據操作步驟,完成表格:
(2)如果要將注射器中的NO充分轉化,可以采取什么措施?操作步驟河 實驗現象 解釋原因 Ⅰ.振蕩注射器,觀察現象 無明顯現象 ① Ⅱ.打開彈簧夾,快速吸入10mL空氣后夾上彈簧夾,觀察現象 ② ③ Ⅲ.振蕩注射器,再觀察現象 氣體又變為無色,注射器的活塞向內移動 ④ 。
(3)上述實驗對工業上生產硝酸有什么啟示?。發布:2024/12/30 6:30:2組卷:9引用:3難度:0.6 -
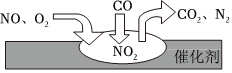 2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )
2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )A.該轉化過程中N元素化合價降低,C元素化合價升高,共兩種元素化合價發生變化 B.汽車尾氣的主要污染成分包括CO、NO和N2 C.NO和O2必須在催化劑表面才能反應 D.催化轉化的總化學方程式為2NO+O2+4CO 4CO2+N2催化劑發布:2024/12/30 6:30:2組卷:9引用:2難度:0.6 -
3.下列有關NO2的敘述正確的是( )
A.閃電時,空氣中的N2和O2可直接化合生成NO2 B.NO2與水反應時,NO2作還原劑,水作氧化劑 C.NO2、NO都是大氣污染氣體,在空氣中都能穩定存在 D.NO2是紅棕色有毒氣體 發布:2024/12/30 6:30:2組卷:7引用:2難度:0.7


