2019-2020學年湖南師大附中高二(上)入學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括11個小題,每小題4分,共44分。每小題只有一個選項符合題意)
-
1.下列有關化學用語表示正確的是( )
A.甲烷的比例模型: 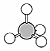
B.過氧化氫的電子式為 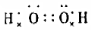
C.中子數為8的碳原子: C146D.Na+的結構示意圖為  組卷:9引用:2難度:0.8
組卷:9引用:2難度:0.8 -
2.設NA表示阿伏加德羅常數的值,下列說法正確的是( )
A.14g C2H4和C3H6的混合物中,所含原子的總數為3NA B.足量的Fe與2.24L Cl2反應轉移的電子數為0.2NA C.0.1mol/L的MgCl2溶液中含Cl-的數目為0.2NA D.1.8g H218O中所含中子數為NA 組卷:5引用:2難度:0.7 -
3.生產液晶顯示器的過程中使用的化學清洗劑NF3是一種溫室氣體,其儲存能量的能力是CO2的12000~20000倍,在大氣中的壽命可長達740年之久,已知鍵能是指斷開1 mol化學鍵變為氣態原子時所需要的能量,或形成1 mol化學鍵時所釋放的能量。以下是幾種化學鍵的鍵能:下列說法中正確的是( )
化學鍵 N≡N F-F N-F 鍵能/kJ?mol-1 941.7 154.8 283.0 A.過程N2(g)→2N(g)放出能量 B.過程N(g)+3F(g)→NF3(g)放出能量 C.反應N2(g)+3F2(g)=2NF3(g)是吸熱反應 D.NF3吸收能量后如果沒有化學鍵的斷裂與形成,仍可能發生化學反應 組卷:116引用:7難度:0.7 -
4.2019年是元素周期表發表150周年,期間科學家為完善周期表做出了不懈努力。中國科學院院士張青蓮教授曾主持測定了銦(49In)等9種元素相對原子質量的新值,被采用為國際新標準。銦與銣(37Rb)同周期。下列說法不正確的是( )
A.In是第五周期第ⅢA族元素 B. In的中子數與電子數的差值為1711549C.原子半徑:In>Al D.堿性:In(OH)3>RbOH 組卷:1125引用:46難度:0.8 -
5.能正確表示下列反應的離子反應方程式為( )
A.氯氣溶于水:Cl2+H2O═2H++Cl-+ClO- B.鈉投入足量水中:2Na+2H2O═2Na++2OH-+H2↑ C.向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O D.向明礬溶液中滴加過量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ 組卷:2引用:1難度:0.7
二、非選擇題(本題包括3個小題,共56分)
-
15.中科院官微曾給出灰霾中細顆粒物的成因,部分分析如圖1所示。

(1)根據如圖1信息可以看出,所列的氣體污染物并非由機動車行駛造成的是。
汽車發動機廢氣稀燃控制系統主要工作原理如圖2所示;寫出稀燃過程中NO發生的主要反應的方程式。
(2)農業活動排出的氨可能是施用的化肥分解,也可能是施用不當導致的。比如某些氮肥與堿性肥料混合施用會釋出氨,用離子方程式解釋
(3)經過研究發現我國的霾呈中性,其主要原因如圖3所示,A的化學式是。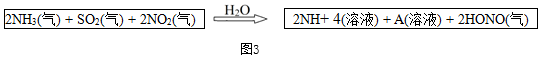
(4)煤燃燒排放的煙氣含有SO2和NOx,采用NaClO2溶液作為吸收劑可同時對煙氣進行脫硫、脫硝。將含有SO2和NOx的煙氣通入盛有NaClO2溶液的反應器中,反應一段時間后,測得溶液中離子濃度的有關數據如下(其他極微量離子忽略不計):
①NO和NaClO2溶液反應的離子方程式是離子 Na+ SO42- NO3- H+ Cl- 濃度/(mol?L-1) 5.5×10-3 8.5×10-4 y 2.8×10-4 3.5×10-3 。
②表中y=。
(5)工業生產硝酸也有可能產生NOx污染。請寫出硝酸生產中的第一步:氨的催化氧化的化學方程式。若用氮氣制氨的產率為90%,用氨生產硝酸時氨的催化氧化和氮氧化物轉化為硝酸的損耗依次為5%、3%,1000mol氮氣可制mol硝酸。組卷:76引用:2難度:0.6 -
16.乙烯是來自石油的重要有機化工原料,其產量通常用來衡量一個國家的石油化工發展水平.結合圖路線回答:
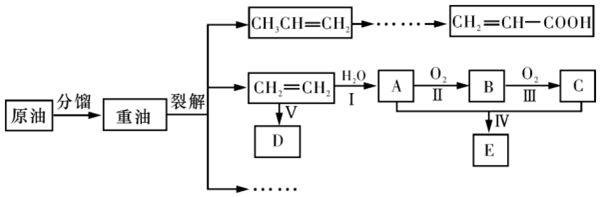
已知:2CH3CHO+O22CH3COOH催化劑△
(1)寫出A的電子式.
(2)反應Ⅱ的化學方程式是.
(3)D為高分子化合物,可以用來制造多種包裝材料,其結構簡式是.
(4)E是有香味的物質,在實驗室用圖裝置制取.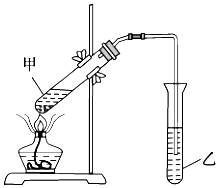
①反應IV的化學方程式是,該反應類型為.
②該裝置圖中有一個明顯的錯誤是.
(5)為了證明濃硫酸在反應IV中起到了催化劑和吸水劑的作用,某同學利用上圖改進后裝置進行了以下4個實驗.實驗開始先用酒精燈微熱3min,再加熱使之微微沸騰3min.實驗結束后充分振蕩小試管乙再測有機層的厚度,實驗記錄如下:
①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用.實驗D中應加入鹽酸的體積和濃度分別是3mL和實驗編號 試管甲中試劑 試管乙中
試劑有機層的
厚度/cmA 2mL乙醇、1mL乙酸、
1mL 18mol?L-1 濃硫酸飽和Na2CO3
溶液3.0 B 2mL乙醇、1mL乙酸 0.1 C 2mL乙醇、1mL乙酸、
3mL 2mol?L-1 H2SO40.6 D 2mL乙醇、1mL乙酸、鹽酸 0.6 mol?L-1.
②分析實驗(填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率.組卷:11引用:2難度:0.3


