鋼鐵是重要的金屬材料,在工農業生產和生活中應用非常廣泛。
Ⅰ.鐵的應用
(1)下列鐵制品的利用與金屬導熱性有關的是 BB(填字母);
A.鐵鏟 B.鐵鍋 C.刀具
(2)“納米a-Fe粉”可以用于食品保鮮,稱之為“雙吸劑”,因為它能吸收空氣中的 氧氣和水氧氣和水;
Ⅱ.鐵的冶煉
工業煉鐵的原理是高溫下用CO作還原劑,將鐵從其氧化物中還原出來。請回答下列問題:
(1)寫出以赤鐵礦為原料,在高溫下煉鐵的化學方程式:3CO+Fe2O3 高溫 2Fe+3CO23CO+Fe2O3 高溫 2Fe+3CO2;
(2)高爐煉鐵中,焦炭的作用除了可以提供熱量外,還能 反應生成還原劑一氧化碳反應生成還原劑一氧化碳;
Ⅲ.實驗探究煉鐵原理:
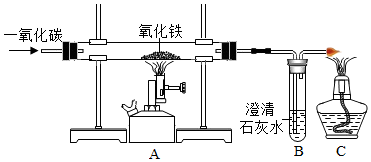
某化學興趣小組的同學利用如圖裝置模擬工業煉鐵的過程,請按要求填空:
(1)實驗時裝置A中的現象是 紅棕色粉末逐漸變成黑色紅棕色粉末逐漸變成黑色;
(2)B中發生反應的化學方程式:CO2+Ca(OH)2=CaCO3↓+H2OCO2+Ca(OH)2=CaCO3↓+H2O;
(3)實驗過程中,CO的作用有 ①②③④①②③④(填序號);
①CO氣體作為反應物;②實驗開始時,排盡裝置中的空氣,防止加熱時發生爆炸;③停止加熱后,防止A中生成物被氧化;④停止加熱后防止B中的溶液倒吸入A中。
Ⅳ.拓展延伸
利用上面的裝置測定某鐵的氧化物中鐵元素和氧元素的質量比。實驗記錄數據如下:①裝鐵的氧化物的硬質玻璃管的質量為20g;②硬質玻璃管與鐵的氧化物的質量共為26.4g;③通入一氧化碳并加熱至鐵的氧化物全部轉化為鐵后,生成的二氧化碳全部被澄清石灰水吸收,且B中生成沉淀的質量為12g。
根據以上實驗記錄,計算此鐵的氧化物中鐵元素和氧元素的質量比 7:37:3。
高溫
高溫
【答案】B;氧氣和水;3CO+Fe2O3 2Fe+3CO2;反應生成還原劑一氧化碳;紅棕色粉末逐漸變成黑色;CO2+Ca(OH)2=CaCO3↓+H2O;①②③④;7:3
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/8/11 2:0:1組卷:78引用:2難度:0.6
相似題
-
1.某化學興趣小組用以下裝置探究煉鐵的原理.
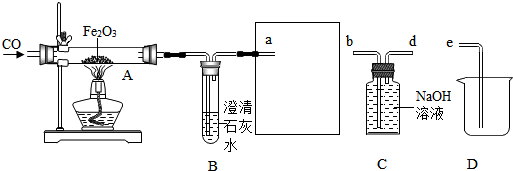
(1)加熱Fe2O3之前要先通一會兒CO,目的是.
(2)方框中連接的是C和D,導管接口的連接順序為a→()→()→(),如果導管連接錯誤,后果是.
(3)玻璃管A中發生反應的化學方程式為,用這種方法“煉”得的鐵與工業上煉出的生鐵在組成上的最大區別是.發布:2024/12/25 16:0:1組卷:202引用:5難度:0.3 -
2.甲圖是一氧化碳還原氧化鐵的裝置,乙圖是煉鐵高爐示意圖。下列敘述中正確的是( )

A.煉鐵的主要原理是:3CO+Fe2O3 2Fe+3CO2高溫B.乙圖煉鐵中原料石灰石的作用是分解制備一氧化碳 C.甲圖中實驗開始時一定要先通一段時間一氧化碳 D.乙圖中分離出爐渣后得到的生鐵是純凈物 發布:2024/12/31 8:0:1組卷:56引用:1難度:0.6 -
3.甲圖是一氧化碳還原氧化鐵的裝置,乙圖是煉鐵高爐示意圖。下列敘述中正確的是( )

A.煉鐵的主要原理是:3CO+Fe2O3═2Fe+3CO2 B.乙圖煉鐵中原料石灰石的作用是分解制備一氧化碳 C.甲圖中實驗開始時一定要先通一段時間一氧化碳 D.乙圖中分離出爐渣后得到的生鐵是純凈物 發布:2024/12/31 8:0:1組卷:231引用:2難度:0.5


