2021-2022學(xué)年廣西欽州四中九年級(jí)(下)月考化學(xué)試卷(2月份)
發(fā)布:2024/8/11 2:0:1
一、單選題
-
1.銅能被加工成厚度僅為7微米的超薄銅箔,說(shuō)明銅具有良好的( )
A.抗腐蝕性 B.導(dǎo)電性 C.導(dǎo)熱性 D.延展性 組卷:120引用:50難度:0.9 -
2.下列物質(zhì)可通過(guò)金屬與稀鹽酸反應(yīng)直接得到的是( )
A.CuCl2 B.AgCl C.ZnCl2 D.FeCl3 組卷:1141引用:26難度:0.8 -
3.某學(xué)習(xí)小組同學(xué)做完鐵與稀硫酸反應(yīng)實(shí)驗(yàn)后,將反應(yīng)后的混合物M全部倒入盛有一小塊銅鋅合金的燒杯中,發(fā)現(xiàn)有大量氣泡產(chǎn)生。待充分反應(yīng)后過(guò)濾,得到濾液和濾渣。他們得出的現(xiàn)象或結(jié)論如下:①M(fèi)中一定不含鐵單質(zhì);②燒杯中溶液由淺綠色變成藍(lán)色;③濾液中一定含有ZnSO4;④濾渣中可能含有三種金屬單質(zhì);⑤濾液中可能含有兩種金屬離子。其中正確的個(gè)數(shù)有( )
A.4個(gè) B.3個(gè) C.2個(gè) D.1個(gè) 組卷:25引用:1難度:0.6 -
4.現(xiàn)有一包由2.4g鎂、6.5g鋅、1.6g碳混合而成的粉末,把它加入到一定量的硝酸銀溶液中,反應(yīng)結(jié)束后,經(jīng)過(guò)濾、洗滌、干燥,測(cè)得濾渣含有三種物質(zhì)。則濾渣的質(zhì)量可能是( )
A.10.5g B.35.6g C.44.8g D.45.8g 組卷:629引用:6難度:0.7 -
5.下列有關(guān)金屬材料的說(shuō)法錯(cuò)誤的是( )
A.在潮濕的空氣中鐵易生銹 B.金屬的回收利用是保護(hù)金屬資源的有效途徑之一 C.鋁和金都有很好的抗腐蝕性,是因?yàn)槎叩幕瘜W(xué)性質(zhì)都很穩(wěn)定 D.高爐煉鐵的原理是在高溫條件下,用一氧化碳把鐵從鐵礦石里還原出來(lái) 組卷:480引用:24難度:0.6 -
6.港珠澳大橋的橋、島、隧以及“雪龍2號(hào)”的船身等主要由金屬材料制成。下列金屬防護(hù)措施不正確的是( )
A.在金屬制品表面鍍保護(hù)層 B.改變金屬結(jié)構(gòu)制成合金使用 C.在金屬制品表面涂油漆 D.用稀鹽酸定期清洗金屬制品 組卷:462引用:19難度:0.6 -
7.下列反應(yīng)屬于置換反應(yīng)的是( )
A.Fe2O3+3CO 2Fe+3CO2高溫B.CH4+2O2 CO2+2H2O點(diǎn)燃C.2Na+2H2O═2NaOH+H2↑ D.Na2CO3+CaCl2═CaCO3↓+2NaCl 組卷:449引用:10難度:0.5
三、計(jì)算題
-
20.為測(cè)定生鐵中鐵的含量,現(xiàn)將一定質(zhì)量的生鐵樣品放入一定質(zhì)量的稀硫酸中,恰好完全反應(yīng)生成0.2g氣體,生鐵中的雜質(zhì)不溶于水,也不與稀硫酸反應(yīng),反應(yīng)后過(guò)濾,將所得的固體洗滌、干燥后稱量為1.4g。請(qǐng)回答下列問(wèn)題:
(1)寫(xiě)出上述反應(yīng)的化學(xué)方程式。
(2)求解生鐵樣品中鐵的質(zhì)量(x)的比例式。
(3)該生鐵中鐵的含量為。
(4)某煉鋼廠每天需消耗5000t含F(xiàn)e2O376%的赤鐵礦,該廠理論上可日產(chǎn)含F(xiàn)e98%的生鐵的質(zhì)量是多少?組卷:1引用:1難度:0.5
四、綜合應(yīng)用題
-
21.鋼鐵是重要的金屬材料,在工農(nóng)業(yè)生產(chǎn)和生活中應(yīng)用非常廣泛。
Ⅰ.鐵的應(yīng)用
(1)下列鐵制品的利用與金屬導(dǎo)熱性有關(guān)的是(填字母);
A.鐵鏟 B.鐵鍋 C.刀具
(2)“納米a-Fe粉”可以用于食品保鮮,稱之為“雙吸劑”,因?yàn)樗芪湛諝庵械?;
Ⅱ.鐵的冶煉
工業(yè)煉鐵的原理是高溫下用CO作還原劑,將鐵從其氧化物中還原出來(lái)。請(qǐng)回答下列問(wèn)題:
(1)寫(xiě)出以赤鐵礦為原料,在高溫下煉鐵的化學(xué)方程式:;
(2)高爐煉鐵中,焦炭的作用除了可以提供熱量外,還能;
Ⅲ.實(shí)驗(yàn)探究煉鐵原理: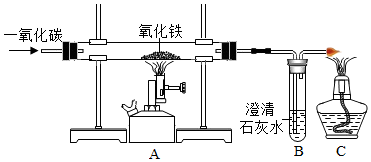
某化學(xué)興趣小組的同學(xué)利用如圖裝置模擬工業(yè)煉鐵的過(guò)程,請(qǐng)按要求填空:
(1)實(shí)驗(yàn)時(shí)裝置A中的現(xiàn)象是;
(2)B中發(fā)生反應(yīng)的化學(xué)方程式:;
(3)實(shí)驗(yàn)過(guò)程中,CO的作用有(填序號(hào));
①CO氣體作為反應(yīng)物;②實(shí)驗(yàn)開(kāi)始時(shí),排盡裝置中的空氣,防止加熱時(shí)發(fā)生爆炸;③停止加熱后,防止A中生成物被氧化;④停止加熱后防止B中的溶液倒吸入A中。
Ⅳ.拓展延伸
利用上面的裝置測(cè)定某鐵的氧化物中鐵元素和氧元素的質(zhì)量比。實(shí)驗(yàn)記錄數(shù)據(jù)如下:①裝鐵的氧化物的硬質(zhì)玻璃管的質(zhì)量為20g;②硬質(zhì)玻璃管與鐵的氧化物的質(zhì)量共為26.4g;③通入一氧化碳并加熱至鐵的氧化物全部轉(zhuǎn)化為鐵后,生成的二氧化碳全部被澄清石灰水吸收,且B中生成沉淀的質(zhì)量為12g。
根據(jù)以上實(shí)驗(yàn)記錄,計(jì)算此鐵的氧化物中鐵元素和氧元素的質(zhì)量比。組卷:78引用:2難度:0.6


