 已知CH3COOH是常見的弱酸,現有常溫下0.1mol?L-1的CH3COOH溶液。
已知CH3COOH是常見的弱酸,現有常溫下0.1mol?L-1的CH3COOH溶液。
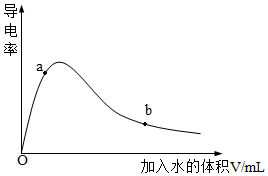
(1)取0.10molCH3COOH作導電性實驗,測得其導電率隨加入的水量變化如圖所示。
①n(H+):a <<b(填“>”、“<”或“=”,下同);
②c(CH3COO-):a >>b;
③完全中和時消耗NaOH的物質的量:a ==b。
(2)溫度不變,加水稀釋過程中,下列表達式的數據一定變小的是 ABAB(填字母,下同);若該溶液升高溫度,下列表達式的數據增大的是 ABCDABCD。
A.c(H+)
B.c(CH3COOH)
C.c(H+)c(CH3COOH)
D.c(CH3COO-)?c(H+)c(CH3COOH)
(3)25℃時,部分物質的電離平衡常數如下表所示:
c
(
H
+
)
c
(
C
H
3
COOH
)
c
(
C
H
3
CO
O
-
)
?
c
(
H
+
)
c
(
C
H
3
COOH
)
| CH3COOH | H2CO3 | HCN |
| 1.7×10-5 | K1=4.3×10-7、K2=5.6×10-11 | 4.9×10-10 |
CH3COOH>H2CO3>HCN
CH3COOH>H2CO3>HCN
。②焦爐煤氣中一般含有H2S和HCN氣體,有的工廠在真空條件下,使用K2CO3溶液吸收煤氣中的H2S和HCN氣體,實現脫硫脫氰。根據上述數據,從理論上推測同為0.1mol?L-1的K2CO3溶液和HCN混合后,最可能發生反應的離子方程式為
CO32-+HCN=HCO3-+CN-
CO32-+HCN=HCO3-+CN-
。【考點】弱電解質的電離平衡.
【答案】<;>;=;AB;ABCD;CH3COOH>H2CO3>HCN;CO32-+HCN=HCO3-+CN-
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:19引用:2難度:0.5
相似題
-
1.用水稀釋0.1mol/L的醋酸溶液,其中隨加水量的增加而增大的有( )
A.C(CH3COOH) B.C(H+) C.C(H+)/C(CH3COOH) D.C(CH3COOH)/C(H+) 發布:2025/1/1 8:0:2組卷:3引用:1難度:0.9 -
2.25℃時,用蒸餾水稀釋0.10mol?L-1的醋酸,若用KW表示水的離子積常數,則下列各式表 示的數值隨水量的增加而增大的是( )
A. [CH3COOH][H+]B. [CH3COO-][CH3COOH]C. [H+]kWD. [H+][OH-]發布:2025/1/1 8:0:2組卷:1引用:1難度:0.7 -
3.將0.1mol?L-1的醋酸溶液加水稀釋,則( )
A.中和此溶液所需的0.1 mol?L-1 NaOH溶液的體積增加 B.c(CH3COOH)減小,平衡向電離方向移動,c(CH3COO-)增大 C.平衡向電離方向移動,c(CH3COOH)、c(H+)、c(OH-)、c(CH3COO-)均減小 D.電離程度增大,由CH3COOH電離出的n(H+)變大 發布:2025/1/1 8:0:2組卷:6引用:1難度:0.7


