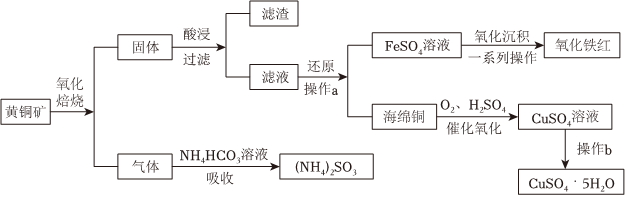
黃銅礦是一種銅鐵硫化物礦物(主要成分為CuFeS2,含少量雜質SiO2等),工業(yè)上利用黃銅礦可生產硫酸銅、氧化鐵紅及亞硫酸銨,主要流程如圖:
(1)黃銅礦在氧化焙燒前磨成精粉目的是 增大接觸面積,增大反應速率,使反應更充分增大接觸面積,增大反應速率,使反應更充分;濾渣的主要成分 SiO2SiO2。
(2)操作b流程依次為蒸發(fā)濃縮、冷卻結晶冷卻結晶、過濾、洗滌干燥。
(3)氧化焙燒反應為:4CuFeS2+13O2 高溫 4CuO+2Fe2O3+8SO2,則反應中生成1molSO2轉移電子物質的量為 132132mol。
(4)寫出濾液“還原”工藝中產生FeSO4的離子方程式 2Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu2Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu。
(5)濕法催化氧化制備硫酸銅相比傳統(tǒng)法有很多優(yōu)點,請寫出海綿銅“催化氧化”中化學反應方程式 2H2SO4+2Cu+O2 △ 2CuSO4+2H2O2H2SO4+2Cu+O2 △ 2CuSO4+2H2O。
(6)上述工藝生產的(NH4)2SO3暴露在空氣中易變質,請設計實驗驗證(NH4)2SO3是否變質 為取少量樣品與試管中,加入適量水溶解,加入足量的稀鹽酸酸化,再加入氯化鋇溶液,若生成白色沉淀,則樣品已氧化變質為取少量樣品與試管中,加入適量水溶解,加入足量的稀鹽酸酸化,再加入氯化鋇溶液,若生成白色沉淀,則樣品已氧化變質。
高溫
13
2
13
2
△
△
【答案】增大接觸面積,增大反應速率,使反應更充分;SiO2;冷卻結晶;;2Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu;2H2SO4+2Cu+O2 2CuSO4+2H2O;為取少量樣品與試管中,加入適量水溶解,加入足量的稀鹽酸酸化,再加入氯化鋇溶液,若生成白色沉淀,則樣品已氧化變質
13
2
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:53引用:1難度:0.6
相似題
-
1.某化學課外小組利用廢銅制取硫酸銅,設計了如下制取方案,其中從理論、操作、經濟、環(huán)保等方面考慮,你認為最合理的是( )
A.Cu CuSO4稀硫酸△B.Cu CuSO4濃硫酸△C.Cu CuOO2△CuSO4稀硫酸D.Cu Cu(NO3)2AgNO3溶液Cu( OH)2NaOH溶液CuSO4稀硫酸發(fā)布:2024/12/30 14:30:1組卷:29引用:3難度:0.7 -
2.(1)H、B、N、Cl四種元素中不屬于p區(qū)的為
(填元素名稱),未成對電子數(shù)目最多的基態(tài)原子的電子排布式為,同周期第一電離能介于B和N之間的元素有種。
(2)最重要的含鈹?shù)V物是綠柱石,含2%鉻(Cr)的綠柱石即為祖母綠。基態(tài)Cr原子的價層電子軌道表示式為。
(3)鈹與相鄰主族的鋁元素性質相似。下列有關鈹和鋁的敘述正確的有(填字母)。
A.都屬于p區(qū)主族元素
B.電負性都比鎂大
C.第一電離能都比鎂大
D.氯化物的水溶液pH均小于7
(4)Mn、Fe兩元素的部分電離能數(shù)據(jù)列于表:
比較Mn、Fe兩元素的I2、I3可知,氣態(tài)Mn2+再失去一個電子比氣態(tài)Fe2+再失去一個電子難。對此,你的解釋是元素 Mn Fe 電離能/(kJ?mol-1) I1 717 759 I2 1509 1561 I3 3248 2957 。
(5)高溫下CuO容易轉化為Cu2O的原因是。發(fā)布:2024/12/30 13:0:2組卷:5引用:3難度:0.5 -
3.把質量為m g的銅絲灼燒變黑后,立即放入下列物質中,銅絲變紅且質量仍為m g的是( )
A.稀硝酸 B.醋酸溶液 C.乙醇 D.CH3CHO 發(fā)布:2024/12/30 19:30:2組卷:51引用:3難度:0.9


