2020-2021學年廣東省佛山市順德區高一(下)期末化學試卷
發布:2024/12/9 0:0:2
一、選擇題共50分本部分包括20小題,1-10題每小題2分,11-20題每小題2分,只有一個選項符合題意。
-
1.下列過程屬于物理變化的是( )
A.裂解 B.煤的氣化 C.減壓蒸餾 D.蛋白質變性 組卷:6引用:2難度:0.8 -
2.化學與人類的生產、生活密切相關,下列有關敘述正確的是( )
A.小米全自動掃拖一體機“T7PrO”搭載驍龍八核芯片的主要成分是二氧化硅 B.我國新一代運載火箭長征八號使用的碳化硅陶瓷是新型無機非金屬材料 C.石墨烯是一種具有優異性能的烯烴 D.水玻璃可用作制備木材防火劑的原料,是一種純凈物 組卷:36引用:3難度:0.6 -
3.下列各項中,官能團的名稱和結構簡式都正確的是( )
A.羥基:OH- B.酯基:-COOH C.醛基:-COH D.碳鹵鍵:-C-X 組卷:39引用:2難度:0.8 -
4.只用溴水不能鑒別的一組物質是( )
A.乙醇和乙酸 B.乙酸乙酯和乙醇 C.苯和四氯化碳 D.己烯和苯 組卷:31引用:2難度:0.7 -
5.氮在生命進程中扮演了至關重要的角色,如圖是有關氮固定的幾種途徑,下列有關敘述不正確的是( )

A.液氮可用于醫學和高科技領域,制造低溫環境 B.雷電固氮過程中氮氣與氧氣直接轉化成紅棕色的二氧化氮 C.光催化固氮和電催化固氮過程中水作還原劑 D.工業固氮采用高溫高壓的目的是提高合成效率 組卷:13引用:1難度:0.7 -
6.下面有關說法正確的有( )
A.聚氯乙烯能使溴水褪色 B.常見烷烴沸點:正戊烷>異丁烷>正丁烷 C.可用酸性高錳酸鉀溶液除去甲烷中混有的乙烯 D.工業上可以利用乙烯與水的反應制取乙醇 組卷:16引用:1難度:0.7 -
7.工業上用洗凈的廢銅屑作原料來制備硝酸銅。為了節約原料和防止污染環境,宜采取的方法是( )
A.Cu+HNO3(濃)→Cu(NO3)2 B.Cu+HNO3(稀)→Cu(NO3)2 C.Cu CuO空氣△Cu(NO3)2HNO3D.Cu CuSO4濃硫酸△Cu(NO3)2Ba(NO3)2組卷:54引用:8難度:0.7 -
8.下列敘述Ⅰ和Ⅱ均正確且有因果關系的是( )
選項 敘述Ⅰ 敘述Ⅱ A 鐵片插入稀硝酸中,無明顯現象 鐵片表面被HNO3鈍化 B 濕潤的藍色石蕊試紙遇到氨氣變紅 氨氣溶于水呈堿性 C 氫氟酸溶液可以刻蝕玻璃 二氧化硅是一種兩性氧化物 D 蔗糖遇濃硫酸變黑,同時產生有刺激性氣味的氣體 濃硫酸具有脫水性和強氧化性 A.A B.B C.C D.D 組卷:39引用:2難度:0.7
二、非選擇題共50分
-
25.二氯化二硫(S2Cl2)是橡膠工業的硫化劑,在冶金工業也可用作金、銀等貴稀金屬的萃取劑。實驗室可用以下兩種原理制備S2Cl2:
①CS2+3Cl2CCl4+S2Cl295~100℃
②2S+Cl2S2Cl2111~140℃
已知:S2Cl2+Cl22SCl2;S2Cl2在300℃以上完全分解產生兩種單質。△
下表是幾種物質的熔沸點:
某實驗小組利用如圖裝置制備S2Cl2,回答下列問題:物質 S CS2 CCl4 S2Cl2 SCl2 熔點/℃ 1128 -109 -23 -77 -121 沸點/℃ 444.6 47 77 137 59.6 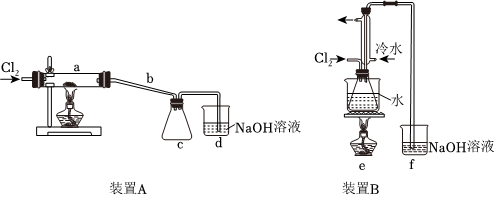
(1)實驗小組欲采用原理②制備S2Cl2,則實驗裝置應選擇(填A或B)。
(2)儀器c的名稱為,儀器b的作用是。
(3)如果在加熱a時溫度過高,對實驗結果的影響是,在b中可能出現的現象是。
(4)上述方案得到的S2Cl2粗品中可能混有的雜質是。
(5)實驗中加入固體硫質量為6.40 g硫,反應后得到產物淺黃色S2Cl2液體4.60mL,則S2Cl2的產率為。(S2Cl2密度1.68g/mL,保留三位有效數字)組卷:32引用:1難度:0.6 -
26.黃銅礦是一種銅鐵硫化物礦物(主要成分為CuFeS2,含少量雜質SiO2等),工業上利用黃銅礦可生產硫酸銅、氧化鐵紅及亞硫酸銨,主要流程如圖:
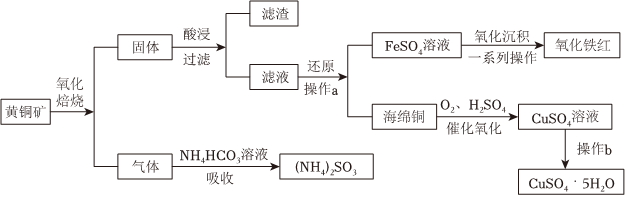
(1)黃銅礦在氧化焙燒前磨成精粉目的是;濾渣的主要成分。
(2)操作b流程依次為蒸發濃縮、、過濾、洗滌干燥。
(3)氧化焙燒反應為:4CuFeS2+13O24CuO+2Fe2O3+8SO2,則反應中生成1molSO2轉移電子物質的量為高溫mol。
(4)寫出濾液“還原”工藝中產生FeSO4的離子方程式。
(5)濕法催化氧化制備硫酸銅相比傳統法有很多優點,請寫出海綿銅“催化氧化”中化學反應方程式。
(6)上述工藝生產的(NH4)2SO3暴露在空氣中易變質,請設計實驗驗證(NH4)2SO3是否變質。組卷:53引用:1難度:0.6


