學習了MnO2對過氧化氫分解有催化作用的知識后,某同學想:CuO能否起到類似MnO2的催化劑作用呢?于是進行了以下探究。
【猜想】Ⅰ、CuO不是催化劑、也不參與反應,反應前后質量和化學性質不變;
Ⅱ、CuO參與反應產生O2,反應前后質量和化學性質發生了改變;
Ⅲ、CuO是反應的催化劑,反應前后質量和化學性質不變質量和化學性質不變。
【實驗】用天平稱量0.2gCuO,取5mL5%的過氧化氫溶液于試管中,進行如下實驗:
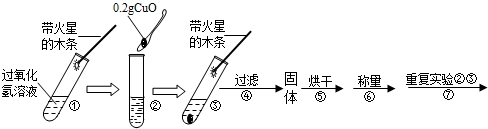
(1)填寫下表:
| 步驟③現象 | 步驟⑥結果 | 步驟⑦現象 | 結論 |
有氣泡 有氣泡 帶火星的木條復燃。 | 氧化銅的質量仍為0.2g 氧化銅的質量仍為0.2g | 溶液中有氣泡放出, 帶火星的木條復燃 帶火星的木條復燃 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
與步驟③對比,檢驗加入氧化銅后雙氧水的分解速率是否發生了變化
與步驟③對比,檢驗加入氧化銅后雙氧水的分解速率是否發生了變化
。(3)步驟④需用到的實驗儀器有:鐵架臺(帶鐵圈)、漏斗、燒杯、
玻璃棒
玻璃棒
。(4)過氧化氫能被CuO催化分解放出O2的化學方程式為
2H2O2 2H2O+O2↑
氧化銅
2H2O2 2H2O+O2↑
。氧化銅
【拓展】要探究步驟⑤做過催化劑的CuO其它化學性質,還應補做的實驗是
用氫氣(或一氧化碳或炭)還原固體,觀察固體是否變成紅色;或用加熱的稀硫酸溶解固體,觀察是否能生成藍色溶液。
用氫氣(或一氧化碳或炭)還原固體,觀察固體是否變成紅色;或用加熱的稀硫酸溶解固體,觀察是否能生成藍色溶液。
。(寫一種)【答案】質量和化學性質不變;有氣泡;氧化銅的質量仍為0.2g;帶火星的木條復燃;與步驟③對比,檢驗加入氧化銅后雙氧水的分解速率是否發生了變化;玻璃棒;2H2O2 2H2O+O2↑;用氫氣(或一氧化碳或炭)還原固體,觀察固體是否變成紅色;或用加熱的稀硫酸溶解固體,觀察是否能生成藍色溶液。
氧化銅
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:441引用:26難度:0.1
相似題
-
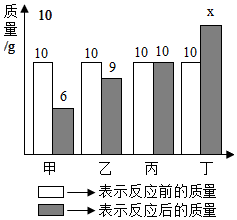 1.甲、乙、丙、丁四種物質在反應前后的質量關系如圖所示,下列有關說法錯誤的是( )
1.甲、乙、丙、丁四種物質在反應前后的質量關系如圖所示,下列有關說法錯誤的是( )A.x的值是15 B.丙可能是該反應的催化劑 C.丁是反應物 D.參加反應的甲和乙的質量比為4:1 發布:2024/8/9 8:0:9組卷:54引用:4難度:0.7 -
2.在密閉容器中加入甲、乙、丙、丁四種物質,使之充分反應,反應前后測得有關數據如表:
下列說法中,不正確的是( )物質 甲 乙 丙 丁 反應前質量/g 18 1 2 32 反應后質量/g X 26 2 12 A.反應后物質甲的質量為13g B.該反應的類型是分解反應 C.反應中乙、丁的質量比為5:4 D.丙可能是該反應的催化劑 發布:2024/8/31 3:0:11組卷:45引用:4難度:0.4 -
3.一定條件下,甲、乙、丙、丁、戊五種物質在密閉容器中發生反應,反應一段時間后,測得反應前后各種物質的質量(單位:g)如圖所示,下列說法不正確的是( )
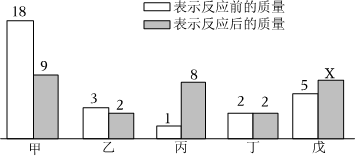 ?
?A.x的數值為8 B.丁可能是該反應的催化劑 C.反應前后乙、丙變化的質量之比為1:7 D.該反應一定是復分解反應 發布:2024/8/3 8:0:9組卷:12引用:1難度:0.5


