高氯酸銨NH4ClO4是復合火箭推進劑的重要成分,實驗室可通過下列反應制取。
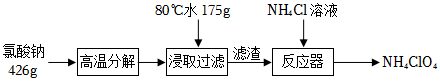
(1)氯酸鈉受熱分解生成高氯酸鈉和氯化鈉的化學方程式為 4NaClO3 高溫 NaCl+3NaClO44NaClO3 高溫 NaCl+3NaClO4。
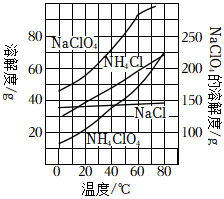
(2)反應得到的混合溶液中NH4ClO4和NaCl的質量分數分別為0.30和0.15,從混合溶液中獲得較多NH4ClO4晶體的實驗操作依次為(填操作名稱) 蒸發濃縮蒸發濃縮、冷卻結晶冷卻結晶、過濾過濾、冰水洗滌、干燥,用冰水洗滌的目的是 減少洗滌過中NH4ClO4晶體的損失減少洗滌過中NH4ClO4晶體的損失。若氯化銨溶液用氨氣和濃鹽酸代替,則該反應不需要加熱就能進行,其原因是 氨氣與濃鹽酸反應放出熱量氨氣與濃鹽酸反應放出熱量。
高溫
高溫
【考點】溶液中溶質的質量分數及相關計算;化學方程式的書寫.
【答案】4NaClO3 NaCl+3NaClO4;蒸發濃縮;冷卻結晶;過濾;減少洗滌過中NH4ClO4晶體的損失;氨氣與濃鹽酸反應放出熱量
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:29引用:1難度:0.6
相似題
-
1.某種酒精與水的混合物中,酒精分子與水分子的個數比為5:6,則該混合物中酒精(化學式C2H6O)的質量分數為( )
A.45.5% B.68.0% C.75.4% D.無法計算 發布:2024/12/21 8:0:2組卷:33引用:3難度:0.7 -
2.若以W1和W2分別表示不同濃度氨水的質量分數,若將二者等體積混合,且混合時體積變化忽略不計.則混合后氨水的質量分數為( )(已知氨水的密度小于純水的密度)
A. W1+W22B.< W1+W22C.> W1+W22D.無法確定 發布:2024/11/2 8:0:1組卷:17引用:1難度:0.7 -
3.下列敘述中正確的是( )
A.溶質質量分數為23%和10%的氨水等質量混合,混合液的溶質質量分數小于16.5% B.同種溶質不同濃度的兩種溶液混合,計算時可將體積直接加和 C.若溶質質量分數為2x%的乙醇溶液的物質的量濃度為2ymol/L,則將其加水稀釋至溶質質量分數為x%,所得稀溶液物質的量濃度大于ymol/L D.某溶液密度為ρg/cm3,溶質摩爾質量為Mg/mol,若物質的量濃度為cmol/L,則該溶液的溶質質量分數為 %cM1000ρ發布:2024/11/15 8:0:2組卷:53引用:1難度:0.5


