(1)利用傳感器實將化學(xué)實驗的實驗過程中某些因素(酸堿性、氣壓等)的變化以數(shù)據(jù)、圖象的形式呈現(xiàn)出來,這種方法極大豐富了實驗研究的方法,被稱為“數(shù)字化實驗”。某校化學(xué)研究小組同學(xué)利用數(shù)字化實驗室,對初中化學(xué)常見的實驗進(jìn)行了探究活動,請回答:
探究蠟燭燃燒的產(chǎn)物
| 方案一 | 方案二數(shù)字化實驗 |
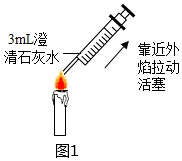
|
 |
石灰水變渾濁
石灰水變渾濁
,證明反應(yīng)生成了二氧化碳,該反應(yīng)的化學(xué)方程式Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
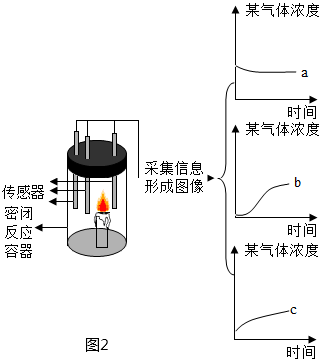
。②如圖2方案二蠟燭在密閉容器內(nèi)燃燒,同時監(jiān)測容器內(nèi)氧氣、二氧化碳和水蒸氣含量的變化,形成三條曲線如坐標(biāo)圖所示,曲線
bc
bc
(選填“a”、“b”、“c”)能夠說明蠟燭燃燒生成了二氧化碳和水。(2)黃石八中劉德蘋老師在今年十一月和實驗中學(xué)901班的學(xué)生一起探究實驗室制取二氧化碳藥品的研究,請你幫忙完成以下探究內(nèi)容
| 藥品組合 | 現(xiàn)象(是否有氣泡、速率快還是慢) | 結(jié)論(是否適合實驗室制CO2) |
| 碳酸鈉粉末和稀鹽酸 | 產(chǎn)生大量氣泡,由于速率太快 產(chǎn)生大量氣泡,由于速率太快
|
否 否
|
| 石灰石和稀硫酸 | 產(chǎn)生氣泡速率緩慢并逐漸停止 產(chǎn)生氣泡速率緩慢并逐漸停止
|
否 |
| 石灰石和稀鹽酸 | 冒氣泡,速率適中 冒氣泡,速率適中
|
是 是
|
CaCO3+H2SO4=CaSO4+H2O+CO2↑
CaCO3+H2SO4=CaSO4+H2O+CO2↑
。(3)該班課代表伍俊杰等同學(xué)還想進(jìn)一步探究,通過查閱資料知道鹽酸的濃度(鹽酸中氯化氫的質(zhì)量與鹽酸的質(zhì)量比)也能影響反應(yīng)的速度,碳酸鈣顆粒的大小也能影響反應(yīng)的速度。以下實驗探究是利用傳感器將塊狀碳酸鈣、粉末狀碳酸鈣與稀鹽酸反應(yīng)的速度過程中氣壓隨時間變化關(guān)系以圖象的形式呈現(xiàn),請你幫忙完成探究內(nèi)容。
| 方案一 | 方案二數(shù)字化實驗 |
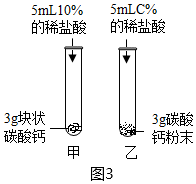
|
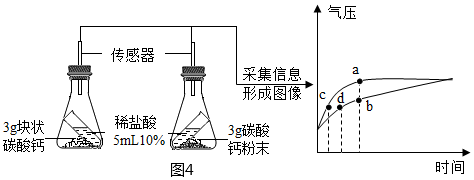
|
10%
10%
。②按如圖4方案二所示進(jìn)行實驗,傾斜錐形瓶使小試管內(nèi)的稀鹽酸流入瓶中與固體接觸發(fā)生反應(yīng),瓶內(nèi)氣壓的變化如坐標(biāo)圖所示。對比分析坐標(biāo)圖中的點(diǎn)
cd
cd
選填(“a”、“b”、“c”、“d)可知:兩個錐形瓶內(nèi)達(dá)到相同的壓強(qiáng)時,碳酸鈣粉末與稀鹽酸反應(yīng)所需時間更短。③如果欲探究鹽酸的濃度對反應(yīng)速度的影響,可將方案二的設(shè)計進(jìn)行改進(jìn),請你寫出你的改進(jìn)方案:
兩錐形瓶中都放入3g塊狀碳酸鈣,一支放5mL10%的稀鹽酸,另一支放5mL5%的稀鹽酸
兩錐形瓶中都放入3g塊狀碳酸鈣,一支放5mL10%的稀鹽酸,另一支放5mL5%的稀鹽酸
。【答案】石灰水變渾濁;Ca(OH)2+CO2═CaCO3↓+H2O;bc;產(chǎn)生大量氣泡,由于速率太快;否;產(chǎn)生氣泡速率緩慢并逐漸停止;冒氣泡,速率適中;是;CaCO3+H2SO4=CaSO4+H2O+CO2↑;10%;cd;兩錐形瓶中都放入3g塊狀碳酸鈣,一支放5mL10%的稀鹽酸,另一支放5mL5%的稀鹽酸
【解答】
【點(diǎn)評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:70引用:2難度:0.3
相似題
-
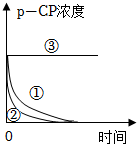 1.Fenton法常用于處理含難降解有機(jī)物的工業(yè)廢水。其原理是利用Fe2+和H2O2的反應(yīng)產(chǎn)生能降解污染物的活性成分。現(xiàn)運(yùn)用該方法降解有機(jī)污染物p-CP,探究有關(guān)因素對降解反應(yīng)速率的影響。實驗探究:控制p-CP的初始濃度相同,實驗溫度恒定在25℃或40℃(其余實驗條件見下表)。
1.Fenton法常用于處理含難降解有機(jī)物的工業(yè)廢水。其原理是利用Fe2+和H2O2的反應(yīng)產(chǎn)生能降解污染物的活性成分。現(xiàn)運(yùn)用該方法降解有機(jī)污染物p-CP,探究有關(guān)因素對降解反應(yīng)速率的影響。實驗探究:控制p-CP的初始濃度相同,實驗溫度恒定在25℃或40℃(其余實驗條件見下表)。
(1)請結(jié)合上述介紹將表中空格補(bǔ)充完整。
(2)實驗測得p-CP的濃度隨時間變化的關(guān)系如圖所示,根據(jù)實驗①、②圖像可得出結(jié)論:實驗編號 實驗?zāi)康?/td> 溫度/℃
pH濃度/(mg?L﹣1) H2O2 Fe2+ ① 為②③提供參照 25 3 204 16.8 ② 探究溫度對降解反應(yīng)速率的影響
3 204 16.8 ③ 探究溶液pH對降解反應(yīng)速率的影響 25 10 204 16.8 。
(3)為測定不同時間內(nèi)有機(jī)物降解的濃度,需在不同時間從反應(yīng)器中取樣,并使所取樣品中的降解反應(yīng)立即停止下來。根據(jù)本題信息,將樣品從反應(yīng)器中取出后應(yīng)立即將其放入某藥品中,反應(yīng)會迅速停止,該藥品可能是。
A鹽酸溶液 B氫氧化鈉溶液 C稀硫酸溶液 D碳酸鈉溶液發(fā)布:2024/11/25 8:0:2組卷:4引用:0難度:0.3 -
2.據(jù)圖1裝置圖回答問題
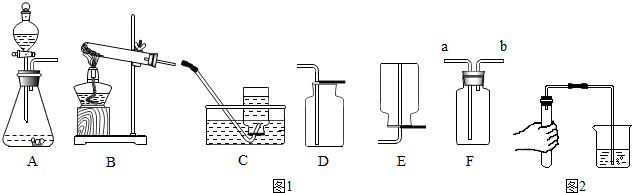
(1)甲同學(xué)用氯酸鉀和二氧化錳共熱制備和收集氧氣,他應(yīng)選用的氣體發(fā)生裝置是(填序號).他用裝置C來收集的原因是,當(dāng)看到導(dǎo)管口的時他才開始收集氧氣.
(2)該同學(xué)用如圖2所示的方法進(jìn)行氣密性檢查,如果裝置不漏氣,可以看到,將手松開一段時間后(導(dǎo)管仍插入水中),可以看到導(dǎo)管中會形成一段水柱.
(3)因為氧氣的密度比空氣的稍大,所以還可以選用(填序號)來收集氧氣,其驗滿的方法是.
(4)老師提醒可以用F(萬能瓶)來收集氣體,則甲同學(xué)應(yīng)將發(fā)生裝置的導(dǎo)管與F的導(dǎo)管(選填a或b)相連接.
(5)乙同學(xué)稱取一定質(zhì)量的KMnO4固體放入大試管中,將溫度控制在250℃加熱制取O2.實驗結(jié)束時,這位同學(xué)發(fā)現(xiàn)用排水法收集到的O2大于理論產(chǎn)量.針對這一現(xiàn)象,同學(xué)們進(jìn)行了如下探究:
【提出猜想】猜想Ⅰ:反應(yīng)生成的二氧化錳(MnO2)分解放出O2;
猜想Ⅱ:反應(yīng)生成的錳酸鉀(K2MnO4)分解放出O2;
【實驗驗證】同學(xué)們分成兩組,分別進(jìn)行下列實驗:
第一組同學(xué)取一定質(zhì)量的MnO2,在250℃條件下加熱一段時間,冷卻后測得MnO2的質(zhì)量不變,則猜想(選填Ⅰ或Ⅱ)錯誤;
第二組同學(xué)取K2MnO4在250℃條件下加熱,沒有用測定質(zhì)量的方法得出了猜想Ⅱ正確的結(jié)論.該組同學(xué)選擇的實驗方法是.
【拓展延伸】實驗發(fā)現(xiàn),KClO3固體加熱制取O2的反應(yīng)速率很慢,但如果將KMnO4固體與KClO3固體混合加熱,則KClO3的分解速率大大加快,請說明KMnO4在KClO3的分解反應(yīng)中是否作催化劑,為什么?.
(6)丙同學(xué)選擇用雙氧水和二氧化錳混合來制氧氣,則他應(yīng)選用的氣體發(fā)生裝置是(填序號).以下是他探究影響該反應(yīng)速率因素的相關(guān)實驗數(shù)據(jù).
通過以上實驗數(shù)據(jù)的分析,可知,過氧化氫分解制氧氣的化學(xué)反應(yīng)速率與實驗
序號H2O2溶液濃度% H2O2溶液體積/mL 溫度℃ MnO2用量/g 收集到的
氧氣體積/mL反應(yīng)所需的
時間/s① 5 1 20 1 30.29 ② 5 1 20 0.1 4 16.75 ③ 15 1 20 0.1 4 6.04 ④ 30 1 55 2 10.76 、、等因素有關(guān);發(fā)生裝置中的(填儀器名稱)也可以幫助控制反應(yīng)的速率.發(fā)布:2024/12/18 8:0:1組卷:12引用:2難度:0.5 -
3.下列探究影響化學(xué)反應(yīng)速率因素的實驗中,實驗方案正確的是( )
選項 影響因素 實驗方案 A 接觸面積 將1g塊狀石灰石和20mL10%的稀鹽酸、1g粉末狀石灰石與20mL10%的稀硫酸混合,比較產(chǎn)生氣泡的快慢 B 催化劑的種類 將0.5g二氧化錳、1g氧化鐵分別與10mL6%的過氧化氫溶液混合,比較產(chǎn)生氣泡的快慢 C 反應(yīng)物的種類 分別將木炭在空氣中、氧氣中燃燒,比較反應(yīng)的劇烈程度 D 反應(yīng)物的性質(zhì) 分別用酒精燈加熱表面積相同的鎂片和鐵片,比較在空氣中能否被點(diǎn)燃 A.A B.B C.C D.D 發(fā)布:2024/12/25 13:0:1組卷:114引用:4難度:0.7
相關(guān)試卷


