 某實驗小組對中學(xué)課本中可生成氫氣的反應(yīng)進(jìn)行了研究,總結(jié)出兩個可以生成H2的反應(yīng):①Zn+鹽酸,②Na+水。為點燃上述兩個反應(yīng)生成的H2,他們設(shè)計了如圖所示裝置。請回答下列問題:
某實驗小組對中學(xué)課本中可生成氫氣的反應(yīng)進(jìn)行了研究,總結(jié)出兩個可以生成H2的反應(yīng):①Zn+鹽酸,②Na+水。為點燃上述兩個反應(yīng)生成的H2,他們設(shè)計了如圖所示裝置。請回答下列問題:
(1)寫出Na與H2O反應(yīng)的化學(xué)方程式:2Na+2H2O=2NaOH+H2↑2Na+2H2O=2NaOH+H2↑。
(2)實驗小組在點燃用上述裝置制得的H2時,①實驗獲得成功,②卻失敗了。他們分析認(rèn)為失敗的原因是Na的用量太少,Na與H2O的反應(yīng)太快。于是他們準(zhǔn)備增加鈉的用量,可老師說太危險,你認(rèn)為產(chǎn)生危險的原因是 大塊的鈉與水反應(yīng)劇烈,放出大量的熱,可能使試管內(nèi)H2和O2的混合氣點燃而爆炸大塊的鈉與水反應(yīng)劇烈,放出大量的熱,可能使試管內(nèi)H2和O2的混合氣點燃而爆炸。
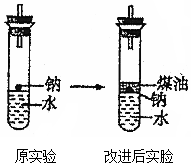
(3)實驗小組查閱鈉、煤油、水的密度分別為0.97g?cm-3、0.80g?cm-3、1.00g?cm-3,并據(jù)此對實驗進(jìn)行改進(jìn)。在改進(jìn)后的實驗中H2的生成速率減小,原因是 鈉處于煤油和水的交界處,鈉與水反應(yīng)產(chǎn)生的H2使鈉浮起,脫離水面,反應(yīng)停止;當(dāng)鈉表面的H2逸出,鈉又回落水層,如此反復(fù),減小了Na與H2O的反應(yīng)速率鈉處于煤油和水的交界處,鈉與水反應(yīng)產(chǎn)生的H2使鈉浮起,脫離水面,反應(yīng)停止;當(dāng)鈉表面的H2逸出,鈉又回落水層,如此反復(fù),減小了Na與H2O的反應(yīng)速率。
【考點】鈉的化學(xué)性質(zhì).
【答案】2Na+2H2O=2NaOH+H2↑;大塊的鈉與水反應(yīng)劇烈,放出大量的熱,可能使試管內(nèi)H2和O2的混合氣點燃而爆炸;鈉處于煤油和水的交界處,鈉與水反應(yīng)產(chǎn)生的H2使鈉浮起,脫離水面,反應(yīng)停止;當(dāng)鈉表面的H2逸出,鈉又回落水層,如此反復(fù),減小了Na與H2O的反應(yīng)速率
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:22引用:1難度:0.6
相似題
-
1.在下列物質(zhì)中,分別加入金屬鈉,不能產(chǎn)生氫氣的是( )
A.蒸餾水 B.乙酸 C.無水乙醇 D.苯 發(fā)布:2024/12/30 9:30:2組卷:15引用:2難度:0.9 -
2.正丙醇(CH3CH2CH2OH)和鈉反應(yīng)要比水和鈉反應(yīng)劇烈。
(判斷對錯)發(fā)布:2024/12/30 15:0:1組卷:7引用:2難度:0.6 -
3.表述I與表述II中,兩者之間因果關(guān)系錯誤的是( )
選項 表述Ⅰ 表述Ⅱ A 金屬鈉保存在煤油中,以隔絕空氣 常溫下,金屬鈉在空氣中會發(fā)生反應(yīng) B 用FeCl3溶液腐蝕印刷電路板 FeCl3溶液能與Cu反應(yīng) C 將干燥的氯氣通入盛有紅色鮮花的集氣瓶中,鮮花褪色 干燥的氯氣具有漂白性 D 氫氧化鋁可用于治療胃酸過多 氫氧化鋁可與鹽酸反應(yīng) A.A B.B C.C D.D 發(fā)布:2025/1/15 8:0:2組卷:23引用:2難度:0.7


