鎳(Ni)元素存在于我們生活用品中,例如保溫杯的不銹鋼就含有。為了了解鎳金屬活動性的強弱,某興趣小組的同學將等量的鎳和鎂與等質量等濃度的稀硫酸進行實驗。將金屬與稀硫酸同時加入反應裝置中,當稀硫酸過量時記錄反應時間和生成氫氣質量,得到如圖甲所示的圖像;當金屬過量時記錄反應時間和生成氫氣的質量,得到如圖乙所示的圖像。若將鎂置于反應裝置中,然后向反應裝置中逐漸滴加稀硫酸,每加一滴完全反應后再加下一滴,以此形式滴加至過量,記錄鎂完全反應時生成氫氣的質量和消耗稀硫酸的質量,得到如圖所示的圖像。(反應的化學方程式:Mg+H2SO4=MgSO4+H2↑;Ni+H2SO4=NiSO4+H2↑)
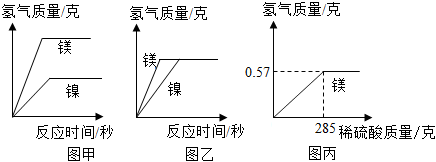
(1)查閱資料得知,與等質量等濃度的同種酸反應,當同種金屬的相同質量時,粉末狀的要比塊狀的反應快。則以上實驗中,鎂和鎳還需要控制 與酸的接觸面積與酸的接觸面積相同。
(2)下列對于甲、乙兩圖理解的說法正確的是 ACDACD(可多選)。
A.甲圖中反應結束后兩種金屬一定沒有剩余 B.乙圖中反應結束后稀硫酸可能有剩余
C.甲圖中反應結束后消耗稀硫酸的質量不相等 D.乙圖中反應結束后消耗稀硫酸的質量相等
(3)取與鎂等質量的鎳置于反應裝置中,然后采用與鎂相同的方式向反應裝置中滴加稀硫酸。請在丙圖上畫出鎳與稀硫酸反應產生氫氣質量與稀硫酸質量的關系圖,標出鎳完全反應時生成氫氣質量和消耗稀硫酸的質量。 



【考點】根據化學反應方程式的計算.
【答案】與酸的接觸面積;ACD;

【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:18引用:1難度:0.5
相似題
-
 1.紹興盛產一種四角菱,稱“馱背白”。其菱肉富含淀粉等多種營養物質,此外菱角的莖和根富含纖維素(C6H10O5)n,也是一種很不錯的食物和藥材。
1.紹興盛產一種四角菱,稱“馱背白”。其菱肉富含淀粉等多種營養物質,此外菱角的莖和根富含纖維素(C6H10O5)n,也是一種很不錯的食物和藥材。
(1)菱肉中的鈣、磷、鐵等元素是以(填“單質”或“化合物”)的形態存在;
(2)該纖維素中C、H、O元素的質量比(最簡比);
(3)查閱資料獲悉菱肉制成的菱粉質細爽滑,為淀粉中之佳品。求菱葉產生3.6千克淀粉[有機物(CH2O)n]的同時,光合作用產生氧氣多少千克?(已知光合作用的化學方程式為:nCO2+nH2O═(CH2O)n+nO2,條件忽略)發布:2025/1/6 8:0:1組卷:4引用:1難度:0.5 -
2.小金為測定某樣品中氧化銅的質量分數,稱量固體樣品20.0克,用如圖所示的裝置進行實驗(雜質不參與反應且生成水完全被吸收),實驗中共消耗0.6克氫氣,測得B裝置反應前后的質量增加了3.6克。
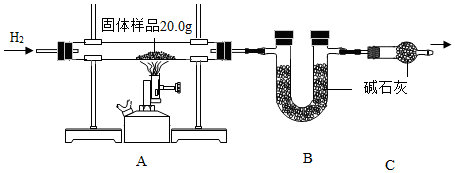
(1)C裝置的作用是;
(2)計算固體樣品中氧化銅的質量分數(根據化學方程式列式計算)。發布:2024/12/28 15:30:1組卷:12引用:2難度:0.5 -
3.侯德榜是我國著名的化學家,發明了侯氏制堿法,其反應原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,請回答:
(1)反應產物中NH4C1可以用于農業生產,它屬于化肥中的肥。
(2)生產16.8t碳酸氫鈉,理論上需要氯化鈉的質量是多少?發布:2024/12/28 15:30:1組卷:12引用:2難度:0.5


