 25℃時,部分物質的電離平衡常數如表所示:
25℃時,部分物質的電離平衡常數如表所示:
| 化學式 | CH3COOH | H2CO3 | HClO | HCN |
|
電離平衡常數(Ka) |
1.8×10-5 |
Ka1=4.3×10-7 Ka2=5.6×10-11 |
3.0×10-8 |
5.0×10-10 |
(1)CH3COOH、H2CO3、HClO、HCN 的酸性由強到弱的順序為
CH3COOH>H2CO3>HClO>HCN
CH3COOH>H2CO3>HClO>HCN
。(2)寫出 H2CO3 溶液中含 C 元素的微粒有:
H2CO3、HCO3-、CO32-
H2CO3、HCO3-、CO32-
。(3)向 NaCN 中通入少量的 CO2,發生的離子方程式為
CN-+CO2+H2O═HCN+HCO3-
CN-+CO2+H2O═HCN+HCO3-
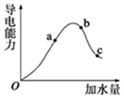
。(4)取 0.10mol CH3COOH (冰醋酸)作導電性實驗,測得其平衡時的導電率隨加入的水量 變化如圖所示:比較 a、b、c 點的相關性質(填“>”“<”或“=”):
①常溫下,b 點醋酸溶液的濃度約為 0.02mol?L-1;該溶液中的 CH3COOH 的電離度為
3%
3%
,若使此溶液中 CH3COOH 的電離程度增大且 c(H+)也增大的方法是 升高溫度
升高溫度
。②從圖象可知,在一定濃度的醋酸溶液中加水 c(CH3COO-)
不確定
不確定
(填增大,減小,或不確定)③若實驗測得 c 點處溶液中 c(CH3COOH)=amol?L-1,c(CH3COO-)=b mol?L-1,則該條件下 CH3COOH 的電離常數 Ka=
b
2
a
b
2
a
④H+濃度相同等體積的兩份溶液 A(鹽酸)和 B(CH3COOH)分別與不同質量的鋅粉反應,若最后僅有一份溶液中存在鋅,放出氫氣的質量相同,則下列說法正確的是
c、d
c、d
(填寫序號)a.反應所需要的時間 B>A
b.開始反應時的速率 A>B
c.參加反應的鋅物質的量 A=B
d.A 中有鋅剩余
【考點】弱電解質的電離平衡.
【答案】CH3COOH>H2CO3>HClO>HCN;H2CO3、HCO3-、CO32-;CN-+CO2+H2O═HCN+HCO3-;3%;升高溫度;不確定;;c、d
b
2
a
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:25引用:2難度:0.7
相似題
-
1.25℃時,用蒸餾水稀釋0.10mol?L-1的醋酸,若用KW表示水的離子積常數,則下列各式表 示的數值隨水量的增加而增大的是( )
A. [CH3COOH][H+]B. [CH3COO-][CH3COOH]C. [H+]kWD. [H+][OH-]發布:2025/1/1 8:0:2組卷:1引用:1難度:0.7 -
2.用水稀釋0.1mol/L的醋酸溶液,其中隨加水量的增加而增大的有( )
A.C(CH3COOH) B.C(H+) C.C(H+)/C(CH3COOH) D.C(CH3COOH)/C(H+) 發布:2025/1/1 8:0:2組卷:3引用:1難度:0.9 -
3.將0.1mol?L-1的醋酸溶液加水稀釋,則( )
A.中和此溶液所需的0.1 mol?L-1 NaOH溶液的體積增加 B.c(CH3COOH)減小,平衡向電離方向移動,c(CH3COO-)增大 C.平衡向電離方向移動,c(CH3COOH)、c(H+)、c(OH-)、c(CH3COO-)均減小 D.電離程度增大,由CH3COOH電離出的n(H+)變大 發布:2025/1/1 8:0:2組卷:6引用:1難度:0.7


