過氧化鈣(CaO2)為白色粉末,是一種用途廣泛的優良供氧劑。工業上可用碳酸鈣作原料制備過氧化鈣,某校活動小組同學模擬工業制備過氧化鈣樣品并測定其純度。
[實驗一]提純碳酸鈣
已知:“轉化”步驟中的反應方程式為:CaCl2+2NH3+CO2+H2O═CaCO3↓+2NH4Cl。
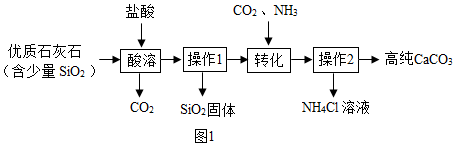
(1)酸溶過程中發生反應的化學方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑CaCO3+2HCl═CaCl2+H2O+CO2↑。
(2)該流程(如圖1)中可循環利用的物質為二氧化碳二氧化碳。
[實驗二]過氧化鈣的制備:
已知:①CaCl2+H2O2+2NH3?H2O+6H2═CaO2?8H2O↓+2NH4Cl。
②CaO2?8H2O在0℃時穩定,加熱至130℃會完全脫水變為CaO2。
③CaO2在350℃開始時分解,生成氧化鈣及氧氣。完全分解的溫度為425℃。

(3)沉淀流程(如圖2)中為控制溫度為0℃左右,在實驗室宜采取的方法為把反應容器浸在冰水混合物中把反應容器浸在冰水混合物中。
(4)操作A在實驗室常用的步驟有加熱濃縮加熱濃縮、降溫結晶、過濾、洗滌、干燥,此操作中洗滌晶體時不可選用的洗滌劑為BB(填字母)。
A.冰水
B.40℃熱水
C.飽和NH4Cl溶液
(5)最后烘干得到過氧化鈣時,適宜的溫度范圍為130℃≤t<350℃130℃≤t<350℃。
[實驗三]過氧化鈣含量的測定
已知:①過氧化鈣在濕空氣、遇水反應緩慢地釋放出氧氣。
②過氧化鈣易和酸反應生成H2O2,CaO2+2HCl═CaCl2+H2O2(放熱)。
③過氧化鈣樣品中其他雜質不與鹽酸反應生成氣體。
該小組取樣品1.5g,設計如圖3裝置,通過測O2體積,計算樣品中CaO2的質量分數。

(6)實驗中MnO2的作用是做過氧化氫分解的催化劑做過氧化氫分解的催化劑。
(7)相同條件下,裝置A裝置A能使測定結果更準確(填“裝置A”或“裝置B”)。
實驗步驟如下:a.連接裝置并檢查裝置氣密性檢查裝置氣密性;
b.稱量樣品的質量1.5g;
c.裝藥品,調節量氣裝置兩邊液面相平,讀取量氣管刻度為10mL;
d.向廣口瓶內加入稀鹽酸,充分反應;
e.冷卻至室溫冷卻至室溫;
f.再次調節量氣裝置兩邊液面相平,讀取量氣管刻度為234mL。
(8)請將上述實驗步驟a、e補充完整;
(9)若標準狀況下,每32g氧氣的體積為22.4L。根據實驗數據計算樣品中CaO2的質量分數96.0%96.0%(寫出計算過程,結果保留到0.1%)。
反思:若其他操作均正確,僅因下列因素可使測定結果偏小的是BCDBCD(填字母)。
A.廣口瓶中殘留少量O2
B.烘干時溫度過高,生成了部分CaO
C.稀鹽酸的用量不足
D.步驟f中沒有調節量氣裝置兩邊液面相平,直接讀數
【答案】CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳;把反應容器浸在冰水混合物中;加熱濃縮;B;130℃≤t<350℃;做過氧化氫分解的催化劑;裝置A;檢查裝置氣密性;冷卻至室溫;96.0%;BCD
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:143引用:2難度:0.5
相似題
-
1.新冠肺炎疫情防控期間,西安市各學校開展全域噴灑低濃度、有效成分是次氯酸鈉的“84”消毒液進行消毒。如圖所示是模擬制備“84”消毒液的流程(Cl2是一種黃綠色的有毒氣體)。請回答下列問題:
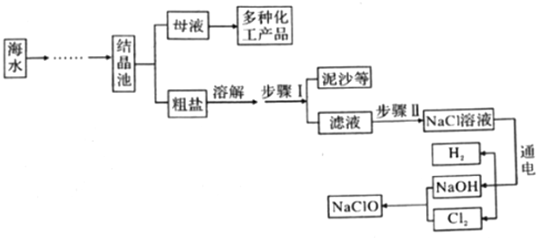
(1)NaOH的俗稱為(寫一種)。
(2)步驟Ⅱ中,通常用碳酸鈉溶液除去濾液中的氯化鈣雜質,請寫出有關反應的化學方程式。
(3)電解水時,一般在水中加入少量NaOH以增強水的導電性,不能加入NaCl的原因是。發布:2025/1/3 8:0:1組卷:6引用:1難度:0.5 -
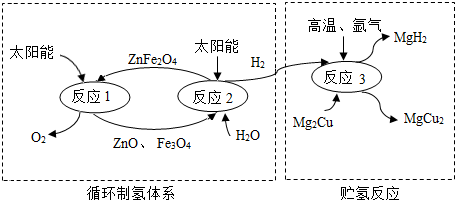 2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )
2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )A.ZnFe2O4中Fe的化合價為+3價 B.循環制氫反應中無需加入ZnFe2O4 C.反應1和反應2的總方程式為:2H2O 2H2↑+O2↑通電D.M與足量稀鹽酸反應生成的H2質量大于反應2產生的H2質量 發布:2024/12/31 8:0:1組卷:48引用:2難度:0.5 -
3.某種家用的消毒液的主要成分是次氯酸鈉(NaClO),制取NaClO的化學方程式為:Cl2+2NaOH=NaClO+NaCl+H2O,下列說法錯誤的是( )
A.NaClO中氯元素的化合價為-1 B.反應中用到的NaOH俗稱燒堿 C.該化學方程式中涉及到兩種鹽 D.反應前后氯元素化合價既升高又降低 發布:2025/1/3 8:0:1組卷:71引用:1難度:0.7


