 1L某混合溶液,可能含有的離子如表所示:
1L某混合溶液,可能含有的離子如表所示:
| 可能大量含有的陽離子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的陰離子 | Cl-、Br-、I-、CO32-、AlO2- |
Mg2+、Fe2+、Fe3+、CO32-、AlO2-
Mg2+、Fe2+、Fe3+、CO32-、AlO2-
。(2)V1、V2、V3、V4之間的關系為
V2-V1=3(V4-V3)
V2-V1=3(V4-V3)
。(3)經檢測,該溶液中還含有大量的Cl-、Br-、I-,若向1L該混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物質的量與通入Cl2的體積(標準狀況)的關系如表所示,分析后回答下列問題:
| Cl2的體積(標準狀況) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | a mol | 0 | 0 |
Cl2+2I-═I2+2Cl-
Cl2+2I-═I2+2Cl-
。②原溶液中Cl-、Br-、I-的物質的量濃度之比為
10:15:4
10:15:4
。【答案】Mg2+、Fe2+、Fe3+、CO32-、AlO2-;V2-V1=3(V4-V3);Cl2+2I-═I2+2Cl-;10:15:4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:12引用:2難度:0.6
相似題
-
1.用1L 1.0mol/LNaOH溶液吸收0.8molCO2,所得溶液中的
和CO2-3的物質的量濃度之比約是( )HCO-3A.2:3 B.1:2 C.1:3 D.3:2 發布:2024/12/3 7:30:1組卷:83引用:6難度:0.7 -
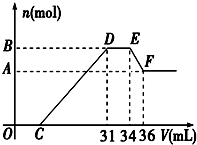 2.已知硝酸與金屬發生氧化還原反應的時候,一般硝酸濃度越稀,對應的還原產物中氮的化合價越低.現有一定量的鋁、鐵合金與一定量稀HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的體積(V)與產生沉淀的物質的量(n)關系如圖所示.則:
2.已知硝酸與金屬發生氧化還原反應的時候,一般硝酸濃度越稀,對應的還原產物中氮的化合價越低.現有一定量的鋁、鐵合金與一定量稀HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的體積(V)與產生沉淀的物質的量(n)關系如圖所示.則:
(1)試寫出DE段、EF段所發生反應的離子方程式:
DE段EF段
(2)合金中鋁的物質的量為mol
(3)合金中金屬的物質的量共為mol
(4)求出C點的值為ml.發布:2024/11/18 8:0:1組卷:18引用:1難度:0.3 -
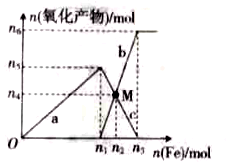 3.在1L 2mol?L-1稀硝酸溶液中逐漸加入鐵粉,反應中氧化產物的物質的量與加入鐵粉的物質的量的關系如圖所示。回答下列問題:
3.在1L 2mol?L-1稀硝酸溶液中逐漸加入鐵粉,反應中氧化產物的物質的量與加入鐵粉的物質的量的關系如圖所示。回答下列問題:
(1)與曲線a對應的離子方程式為。
(2)曲線b代表的微粒為;n2的值為。
(3)若M點時再加入VL2mol?L-1的稀硝酸,恰好反應完全,則V為。
(4)研究表明硝酸的濃度越小,反應后氮的化合價越低。在極稀的硝酸溶液中加入少量鐵粉,生成NH4+的離子方程式為。發布:2024/11/18 8:0:1組卷:9引用:1難度:0.5


